
| ��� | ʵ������ | ʵ��Ŀ�� |
| A | �ڵ��з�̪��Na2CO3��Һ�У��μ���BaC12��Һ����Һ��ɫ����ȥ | ֤��Na2CO3��Һ�д���ˮ��ƽ�� |
| B | ��Al������Ũ�����У������� | ֤��Al��Ũ�����Ӧ |
| C | ��������ȫ��ͬ�ҳ���NO2���ܱ���ƿ���ֱ��������ˮ����ˮ�� | ̽���¶ȶԻ�ѧƽ��״̬��Ӱ�� |
| D | ��ͬ���ͬŨ�ȵ�H2O2��Һ�У��ֱ����1mLͬŨ�ȵ�CuSO4��FeCl3��Һ | �Ƚ�Cu2+��Fe3+��H2O2�ֽ����ʵ�Ӱ�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
���� A��̼����ˮ��ʼ��ԣ�����BaC12��Һ������̼�ᱵ������
B��Al�����汻HNO3�������γ����ܵ�����Ĥ��
C�����ڻ�ѧƽ��2NO2?N2O4���¶ȵͣ���ɫdz�����¶�ƽ�������ƶ���
D��ͬŨ��H2O2��Һ������CuSO4��FeCl3��Һ�������Ӳ�ͬ��
��� �⣺A��̼����ˮ��ʼ��ԣ�����BaC12��Һ������̼�ᱵ������ƽ�����淽���ƶ�������Һ��ɫ����˵��Na2CO3��Һ�д���ˮ��ƽ�⣬��A��ȷ��
B��Al�����汻HNO3�������γ����ܵ�����Ĥ��������û�з�Ӧ����B����
C�����ڻ�ѧƽ��2NO2?N2O4���¶ȵͣ���ɫdz�����¶�ƽ�������ƶ�����÷�ӦΪ���ȷ�Ӧ����̽���¶ȶԻ�ѧƽ��״̬��Ӱ�죬��C��ȷ��
D��ͬŨ��H2O2��Һ������CuSO4��FeCl3��Һ�������Ӳ�ͬ������˵�������Ӷ�H2O2�ֽ����ʵ�Ӱ�죬��D����
��ѡBD��
���� ���⿼�黯ѧʵ�鷽�������ۼ�ʵ��װ���ۺϣ�Ϊ��Ƶ���㣬�漰����ˮ�⼰pH�����ʵķ�Ӧ����ѧƽ�⼰Ӱ�췴Ӧ���ʵ����صȣ��������ʵ����ʡ���Ӧԭ����ʵ�鼼��Ϊ���Ĺؼ������ط�����ʵ�������Ŀ��飬ѡ��DΪ�����״��㣬��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ����I��Ӧ��2NH4HCO3+Na2SO4�T2NaHCO3��+��NH4��2SO4 | |
| B�� | ������ҺB�������ӵ��Լ�����BaCl2��Һ | |
| C�� | ��ʡ�Թ���II��������������Լ�С | |
| D�� | ���������Һ����μ���NaOH��Һ�Ⱥ�۲쵽���̼��������ݳ�����ɫ�������ɡ���ɫ������ʧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| CO | H2O | CO2 | H2 |
| 0.5mol | 8.5mol | 2.0mol | 2.0mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 +4NaOH$��_{��}^{����Һ}$NaOOCC��CCOONa+2NaBr+4H2O��
+4NaOH$��_{��}^{����Һ}$NaOOCC��CCOONa+2NaBr+4H2O���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �û�ͭ����Ҫ�ɷ���CuFeS2��������ͭ�ķ�Ӧԭ�����£�
�û�ͭ����Ҫ�ɷ���CuFeS2��������ͭ�ķ�Ӧԭ�����£��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
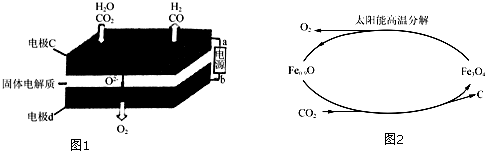

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͬ��Ԫ�ص��������ض���ͬ | |
| B�� | ��ͬԪ��ԭ�ӵ��������ض���ͬ | |
| C�� | ԭ�Ӻ˶��������Ӻ����ӹ��ɵ� | |
| D�� | ���Ǻ����������ͬ�����ض�����ͬһԪ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��1��COC12�׳ƹ�����������Cԭ�Ӳ�ȡsp2�ӻ��ɼ����������ӵĽṹʽΪ
��1��COC12�׳ƹ�����������Cԭ�Ӳ�ȡsp2�ӻ��ɼ����������ӵĽṹʽΪ ������̼��ԭ��֮�乲�ۼ���c������ţ���
������̼��ԭ��֮�乲�ۼ���c������ţ��� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3Zn+8HNO3��ϡ���T3 Zn ��NO3��2+2NO��+4H2O | |
| B�� | CuO+2 HNO3 ��ϡ���TCu��NO3��2+H2O | |
| C�� | C+4HNO3 ��Ũ���TCO2+4 NO2��+2H2O | |
| D�� | 3Ag+4 HNO3 ��ϡ���T3 Ag NO3+NO��+2H2O |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com