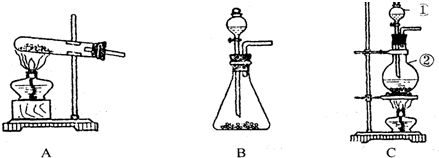
在实验室常用下面的方法制备氢氧化铁胶体:用洁净的烧杯取少量的蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入1mol/LFeCl3溶液,至液体呈透明的红褐色.请按要求回答下列问题:
(1)反应的化学方程式为______;
(2)氢氧化铁胶体中微粒直径的范围是______;
(3)判断胶体制备成功的方法是______;
(4)若向此分散系中逐滴加入盐酸稀溶液,会发生一系列变化:
①先出现红褐色沉淀,原因是______;
②随后沉淀会溶解,溶液呈黄色,写出此反应的离子方程式______.
解:(1)制备氢氧化铁胶体用的水眼泪水解的知识,加热条件下FeCl3的水解生成胶体,因此方程式中要写明条件(加热),特别注意的是:生成的是胶体而不是沉淀,化学方程式为FeCl3+3H2O?Fe(OH)3(胶体)+3HCl,故答案为:FeCl3+3H2O?Fe(OH)3(胶体)+3HCl;
(2)氢氧化铁胶体是胶体分散系中的一种,胶体粒子直径大小在1nm~100nm,故答案为:1nm~100nm;
(3)胶体区别于溶液的关键在于:溶液粒子直径小于1nm,胶体粒子直径大小在1nm~100nm,即溶液不产生丁达尔效应,而氢氧化铁胶体能产生丁达尔效应,因此答案为:用一束光线照射,能产生一条光亮的通路,故答案为:用一束光线照射,能产生一条光亮的通路(也可利用胶体的其他性质进行检验,但要注意表达规范);
(4)①能使胶体聚沉的方法有:加入带相反电荷胶粒的胶体、加热、加入电解质溶液.氢氧化铁胶体胶体遇到盐酸(电解质溶液)会发生聚沉,
故答案为:加电解质,使胶体聚沉;
②氢氧化铁胶体聚沉后会产生氢氧化铁沉淀,继续加入盐酸,会发生酸碱中和反应,生成氯化铁和水,故答案为:Fe(OH)3+3H+=Fe3++3H2O.
分析:本题要根据氢氧化铁胶体胶体的制备、性质(丁达尔效应、聚沉)和胶体微粒直径的大小解答.
点评:本题要求熟练掌握胶体的制备知识,特别是氢氧化铁胶体的制备方程式是常考常错的内容,胶体的聚沉以及沉淀的溶解一直是具有一定综合性的热点.