

分析 F为常见的红棕色油漆颜料的主要成分,则F为Fe2O3,F溶于盐酸得G为FeCl3,试剂X应为KSCN溶液,C与溴水反应生成D,D能与氯化钡生成沉淀,B为非金属单质,A与B反应生成C,C与B反应生成I,I与水反应生成D,且A、C、D、E中含有同一种元素,则可推知B为O2,C为SO2,D为H2SO4,I为SO3,E为BaSO4,1molA参加反应,假设各步反应均完全,生成E的质量为466.0g即为2mol,生成F的质量为80.0g即为0.5mol,根据元素守恒可知A为FeS2,据此答题.
解答 解:F为常见的红棕色油漆颜料的主要成分,则F为Fe2O3,F溶于盐酸得G为FeCl3,试剂X应为KSCN溶液,C与溴水反应生成D,D能与氯化钡生成沉淀,B为非金属单质,A与B反应生成C,C与B反应生成I,I与水反应生成D,且A、C、D、E中含有同一种元素,则可推知B为O2,C为SO2,D为H2SO4,I为SO3,E为BaSO4,1molA参加反应,假设各步反应均完全,生成E的质量为466.0g即为2mol,生成F的质量为80.0g即为0.5mol,根据元素守恒可知A为FeS2,
(1)根据上面的分析可知,A为FeS2,反应①的化学方程式为:4 FeS2+11O2=8SO2+2Fe2O3,
故答案为:FeS2;4 FeS2+11O2=8SO2+2Fe2O3;
(2)反应②的化学方程式为Br2+SO2+2H2O=2HBr+H2SO4,因为有酸产生,所以反应一段时间后所得溶液的PH值将减少,反应③的离子方程式为Fe2O3+6H+=2Fe3++3H2O,
故答案为:Br2+SO2+2H2O=2HBr+H2SO4;减少;Fe2O3+6H+=2Fe3++3H2O;
(3)在高温条件下,向一个密闭容器中投入1molSO2 和2molO2,反应⑥进行一段时间后达到平衡状态,测得SO2的转化率为86.0%,放出热量为a KJ,则当有2molSO2 完全反应时应放出热量为2.3aKJ,所以此条件下C与B反应的热化学方程式为 2SO2 (g)+O2(g) $?_{△}^{催化剂}$ 2SO3(g)△H=-2.3aKJ•mol-1,这时容器内二氧化硫的物质的量为0.14mol,氧气的物质的量为1.57mol,三氧化硫的物质的量为0.86mol,所以混合气体的平均相对分子质量为$\frac{64+32×2}{0.14+1.57+0.86}$g/mol=49.8g/mol,
故答案为:2SO2 (g)+O2(g) $?_{△}^{催化剂}$ 2SO3(g)△H=-2.3aKJ•mol-1;49.8g/mol;
(4)在实际工业生产中反应 不是用水吸收三氧化硫制硫酸,而是用98.3%的浓硫酸吸收,
故答案为:不是;98.3%的浓硫酸.
点评 题考查无机物的推断题目难度较大,解答本题时注意抓住物质的特出性质和用途作为突破口采用正推和逆推相结合的方法推断.


科目:高中化学 来源: 题型:选择题
| A. | Na2CO3比NaHCO3易溶于水 | B. | Na2CO3比NaHCO3稳定 | ||
| C. | Na2CO3和NaHCO3都能与盐酸反应 | D. | Na2CO3俗名:小苏打 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
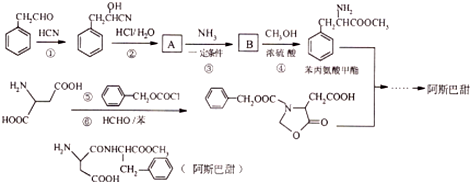
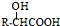 $→_{一定条件}^{NH_{3}}$
$→_{一定条件}^{NH_{3}}$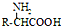
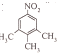 、
、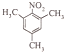 ;
;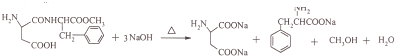 ;
;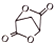 的合成路线流程(无机试剂任选).合成路线流程示例如下 CH2═CH3$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$ CH3CH2OH:
的合成路线流程(无机试剂任选).合成路线流程示例如下 CH2═CH3$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$ CH3CH2OH: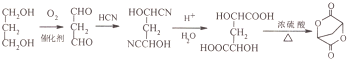 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入BaCl2溶液生成白色沉淀,加稀硝酸沉淀不消失,则原溶液中一定含有SO42- | |
| B. | 加入AgNO3溶液生成白色沉淀,则原溶液中一定含有Cl- | |
| C. | 加入KSCN溶液时,溶液不变红色,再滴入氯水溶液变为红色,则原溶液中一定含有Fe2+ | |
| D. | 加入盐酸,生成的气体能使成清石灰水变浑浊,则原溶液中一定含有CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “雾霾天气”、“温室效应”、“光化学烟雾”的形成都与氮的氧化物无关 | |
| B. | 乙醇溶液、臭氧、双氧水、高锰酸钾溶液均可用于消毒杀菌,且原理不同 | |
| C. | 生石灰、铁粉、硅胶是食品包装中常用的干燥剂 | |
| D. | 纯碱是焙制糕点所用的发酵粉的主要成分之一,也可用纯碱除去物品表面的油污 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 按照系统命名法,烃分子 的名称为2,3-二甲基-3-乙基戊烷 的名称为2,3-二甲基-3-乙基戊烷 | |
| B. | 鸡蛋白、大豆蛋白等蛋白质可溶于水,在这些蛋白质溶液中加入(NH4)2SO4或Na2SO4的浓溶液,可使蛋白质的溶解度降低而析出 | |
| C. | 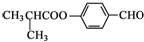 可发生加成反应、取代反应、氧化反应 可发生加成反应、取代反应、氧化反应 | |
| D. | 有机物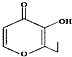 (俗称“一滴香”)的一种含苯环的同分异构体能发生银镜反应 (俗称“一滴香”)的一种含苯环的同分异构体能发生银镜反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用广泛pH试纸测得 0.1mol/L NH4Cl溶液的pH=5.2 | |
| B. | 酸碱中和滴定时锥形瓶用蒸馏水洗涤后,再用待测液润洗后装液进行滴定 | |
| C. | 将碘水倒入分液漏斗,加入适量苯振荡后静置,从分液漏斗下口放出碘的苯溶液 | |
| D. | 常温常压下,将15g NO和8g O2混合,所得混合气体分子总数小于0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO中混有CO2(NaOH溶液) | B. | H2中混有HCl(NaOH溶液) | ||
| C. | NO中混有NO2(水) | D. | CO2中混有HCl(饱和Na2CO3溶液) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
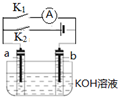
| A. | 断开K2,闭合K1一段时间,溶液的pH要变大 | |
| B. | 断开K1,闭合K2时,b极上的电极反应式为 2H++2e-═H2↑ | |
| C. | 断开K1,闭合K2时,OH-向b极移动 | |
| D. | 断开K2,闭合K1时,a极上的电极反应式为:4OH--4e-═O2↑+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com