
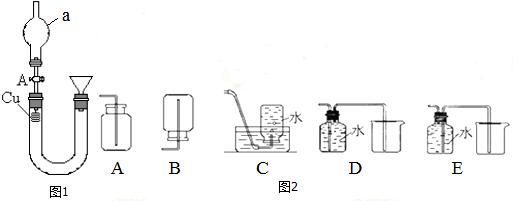
·ÖĪö £Ø1£©×°ÖĆÖŠaŅĒĘ÷µÄĆū³ĘĪŖŹĒĒņŠĪøÉŌļ¹Ü£»
£Ø2£©¼ÓČėĻõĖįµÄ²Ł×÷£ŗÓ¦ĻČ“ņæŖ»īČūA±£Ö¤UŠĪ¹ÜÄŚŃ¹ĒæĘ½ŗā£¬ĒŅÅųöĘųĢå£¬Č»ŗó“ÓÓŅ¹ÜµÄĀ©¶·ÖŠĻņUŠĪ¹ÜÖŠÖš½„×¢ČėĻ”ĻõĖį£®µ±×¢Āśŗó£¬Ó¦¹Ų±Õ»īČūA£¬ĶŗĶĻ”ĻõĖį·“Ӧɜ³ÉĻõĖįĶŗĶĪŽÉ«ĘųĢåŅ»Ńõ»ÆµŖ£¬ĻõĖįĶĪŖĄ¶É«£»“ż·“Ó¦Ņ»»įŗóČō“ņæŖ»īČūA£¬æÕĘų½ųČė£¬Ņ»Ńõ»ÆµŖ±»Ńõ»Æ³É¶žŃõ»ÆµŖ£»
£Ø3£©Ņ»Ńõ»ÆµŖÓŠ¶¾ĒŅŅ×ŗĶŃõĘų·“Ӧɜ³É¶žŃõ»ÆµŖ£¬Ņ»Ńõ»ÆµŖ²»ŗĶĖ®·“Ó¦£¬ĖłŅŌ²»ÄÜÓĆÅÅĖ®·ØŹÕ¼Æ£¬Ó¦øĆÓĆÅÅĖ®·ØŹÕ¼Æ£»
£Ø4£©1.92gµÄĶµÄĪļÖŹµÄĮæn£ØCu£©=$\frac{1.92g}{64g/mol}$=0.03mol£¬»ģŗĻĖįÖŠn£ØH+£©=0.4mol/L”Į0.1L+0.1mol/L”Į2”Į0.1L=0.06mol£¬n£ØNO3-£©=0.4mol/L”Į0.1L=0.04mol£¬
·¢Éś3Cu+8H++2NO3-=3Cu2++2NO”ü+4H2O£¬ÅŠ¶Ļ¹żĮæŗóŅŌ²»×ćĮæ“śČė¼ĘĖć£»
£Ø5£©ĻõĖį²»ĪČ¶Ø·Ö½ā²śÉśµÄ¶žŃõ»ÆµŖČܽāĘäÖŠ³Ź»ĘÉ«£»
£Ø6£©øł¾ŻČÜŅŗÅØ¶Č±ä»ÆµÄÓ°ĻģŅņĖŲŗĶĘųĢåµÄČܽā¶ČÓ°ĻģŅņĖŲ½ā“š£®
½ā“š ½ā£ŗ£Ø1£©×°ÖĆÖŠaŅĒĘ÷ŗ¬ÓŠµäŠĶµÄĒņÅŻĢŲÕ÷£¬ĪŖĒņŠĪøÉŌļ¹Ü£¬
¹Ź“š°øĪŖ£ŗĒņŠĪøÉŌļ¹Ü£»
£Ø2£©¼ÓČėĻõĖįµÄ²Ł×÷£ŗÓ¦ĻČ“ņæŖ»īČūA±£Ö¤UŠĪ¹ÜÄŚŃ¹ĒæĘ½ŗā£¬Ķ¬Ź±°ŃUŠĪ¹Ü×ó²ąµÄæÕĘųÅųö£¬ĶĖæŗĶĻõĖį·“Ó¦£¬ĖłŅŌµ±×¢Āśŗó£¬Ó¦¹Ų±Õ»īČūA£¬ĶŗĶĻ”ĻõĖį·“Ӧɜ³ÉĻõĖįĶŗĶĪŽÉ«ĘųĢåŅ»Ńõ»ÆµŖ£¬ĻõĖįĶĪŖĄ¶É«£¬ĖłŅŌ“ĖŹ±¹Ū²ģµ½µÄĻÖĻóĪŖUŠĶ¹Ü×ó¹ÜÖŠ£¬Ķ±ķĆęÓŠĪŽÉ«ĘųĢåÉś³É£¬ŅŗĆęĻĀ½µ£¬ČÜŅŗÖš½„±äĪŖĄ¶É«£¬“ż·“Ó¦Ņ»»įŗóČō“ņæŖ»īČūA£¬æÕĘų½ųČė£¬ŌŚøÉŌļ¹ÜÖŠĪŽÉ«µÄŅ»Ńõ»ÆµŖ±»Ńõ»Æ³Éŗģ×ŲÉ«µÄ¶žŃõ»ÆµŖ£¬×ó¹ÜŅŗĆęÉĻÉż£¬
¹Ź“š°øĪŖ£ŗ“ņæŖ£»¹Ų±Õ£»UŠĶ¹Ü×ó¹ÜÖŠ£¬Ķ±ķĆęÓŠĪŽÉ«ĘųĢåÉś³É£¬ŅŗĆęĻĀ½µ£¬ČÜŅŗÖš½„±äĪŖĄ¶É«£»ŌŚøÉŌļ¹Ü֊擵½ĘųĢå±äĪŖŗģ×ŲÉ«£¬×ó¹ÜŅŗĆęÉĻÉż£»
£Ø3£©Ņ»Ńõ»ÆµŖÓŠ¶¾ĒŅŅ×ŗĶŃõĘų·“Ӧɜ³É¶žŃõ»ÆµŖ£¬Ņ»Ńõ»ÆµŖ²»ŗĶĖ®·“Ó¦£¬ĖłŅŌ²»ÄÜÓĆÅÅĖ®·ØŹÕ¼Æ£¬Ó¦øĆÓĆÅÅĖ®·ØŹÕ¼Æ£¬ÅÅĖ®×°ÖĆÖŠ£¬ĘųĢåµÄ½ų³öæŚ·ūŗĻ”°¶Ģ½ų³¤³ö”±µÄŌŌņ£¬¹ŹCE·ūŗĻ£¬
¹Ź“š°øĪŖ£ŗC”¢E£»
£Ø4£©1.92gµÄĶµÄĪļÖŹµÄĮæn£ØCu£©=$\frac{1.92g}{64g/mol}$=0.03mol£¬»ģŗĻĖįÖŠn£ØH+£©=0.4mol/L”Į0.1L+0.1mol/L”Į2”Į0.1L=0.06mol£¬n£ØNO3-£©=0.4mol/L”Į0.1L=0.04mol£¬
ÓÉ3Cu+8H++2NO3-=3Cu2++2NO”ü+4H2OæÉÖŖ£¬CuÓėNO3-¹żĮ棬H+²»×ć£¬ĒāĄė×ÓµÄĪļÖŹµÄĮæ½ųŠŠ¼ĘĖć£¬
Éč²śÉśµÄĶĄė×ÓµÄĪļÖŹµÄĮæĪŖx moL£¬
3Cu+8H++2NO3-=3Cu2++2NOӟ+4H2O
8 3
0.06 x
$\frac{8}{0.06}$=$\frac{3}{x}$£¬x=0.0225mol£¬
c£ØCu2+£©=$\frac{0.0225mol}{0.1L}$=0.225mol/L£¬
¹Ź“š°øĪŖ£ŗ0.225mol/L£»
£Ø5£©ÅØĻõĖį²»ĪČ¶Ø£¬ŹÜČČ»ņ¼ū¹ā·Ö½ā²śÉśµÄŗģ×ŲÉ«¶žŃõ»ÆµŖČܽāĘäÖŠ³Ź»ĘÉ«£¬·“Ó¦·½³ĢŹ½ĪŖ4HNO3£ØÅØ£©$\frac{\underline{\;¹āÕÕ\;}}{\;}$4NO2”ü+O2”ü+2H2O£¬
¹Ź“š°øĪŖ£ŗÅØĻõĖįŹÜČČ»ņ¼ū¹āŅ×·Ö½ā²śÉśŗģ×ŲÉ«µÄ¶žŃõ»ÆµŖĘųĢå£Ø4HNO3$\frac{\underline{\;¹āÕÕ\;}}{\;}$4NO2”ü+O2”ü+2H2O£©£¬øĆĘųĢåČÜÓŚÅØĻõĖįÖŠ£¬¶ųŹ¹ČÜŅŗ±äĪŖ»ĘÉ«£»
£Ø6£©¼ÓČČĀĢÉ«ČÜŅŗ£¬ĘųĢåµÄČܽāĮæ¼õŠ”£¬ÄÜøıäČÜŅŗÖŠČܽāĘųĢåµÄĮ棬¹Ź¢ŁÕżČ·£¬¶ų¼ÓĖ®Ļ”ŹĶĀĢÉ«ČÜŅŗ£¬ÓÉÓŚČÜŅŗÅØ¶Č±äŠ”£¬ČÜŅŗµÄŃÕÉ«»į±ä»Æ£¬¶ųĒŅ¼ÓĖ®ŗóĘųĢåµÄČܽāĮæ¼Ó“ó£¬ČÜŅŗµÄŃÕÉ«Ņ²»į·¢Éś±ä»Æ£¬¹Ź²»ÄܽųŠŠÅŠ¶Ļ£¬¹Ź¢Ś“ķĪó£¬ĻņøĆĀĢÉ«ČÜŅŗÖŠĶØČėµŖĘų£¬µŖĘųÄŃČÜÓŚĖ®£¬ĶØČėµŖĘųæÉŅŌ“ų×߶žŃõ»ÆµŖĘųĢ壬ÓÉÓŚČÜŅŗÅØ¶Č±äŠ”£¬ČÜŅŗµÄŃÕÉ«»į±ä»Æ£¬æÉŅŌÖ¤Ć÷øĆČÜŅŗÖŠŹĒ·ńĪŖČܽāĮĖNO2ĘųĢåĖłÖĀ£¬¹Ź¢ŪÕżČ·£¬
¹Ź“š°øĪŖ£ŗ¢Ł¢Ū£®
µćĘĄ ±¾Ģāæ¼²éĮĖĻõĖįµÄŠŌÖŹŹµŃéĢ½¾æ£¬²ąÖŲÓŚµŖŃõ»ÆĪļµÄŠŌÖŹµÄ漲飬ĪŖøßĘµæ¼µć£¬°ŃĪÕĪļÖŹµÄŠŌÖŹ¼°·¢ÉśµÄ·“Ó¦ĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėÓ¦ÓĆÄÜĮ¦µÄ漲飬עŅāĻõĖįµÄŠŌÖŹ£¬ĢāÄæÄѶČÖŠµČ£®


 ĒįĖɶį¹ŚČ«ÄÜÕĘæŲ¾ķĻµĮŠ“š°ø
ĒįĖɶį¹ŚČ«ÄÜÕĘæŲ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ļ”ĮņĖįµĪŌŚĶʬÉĻ£ŗCu+2H+ØTCu2++H2”ü | |
| B£® | ĮņĖįÄĘČÜŅŗÓėĀČ»Æ±µČÜŅŗ»ģŗĻ£ŗBa2++SO42-ØTBaSO4”ż | |
| C£® | ŃĪĖįµĪŌŚŹÆ»ŅŹÆÉĻ£ŗCaCO3+2H+ØTH2CO3+Ca2+ | |
| D£® | Ńõ»ÆĶÓėĮņĖį»ģŗĻ£ŗCu2++SO42-ØTCuSO4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Fe £ØOH £©3£»Fe2O3 | B£® | Fe £ØOH£©2£» FeO”¢Fe £ØOH£©2 | ||
| C£® | Fe £ØOH£©3£»Fe3O4 | D£® | Fe2O3£»Fe £ØOH£©3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀČĘųµÄĖ®ČÜŅŗµ¼µēŠŌĮ¼ŗĆ£¬ĖłŅŌĀČĘųŹĒĒæµē½āÖŹ | |
| B£® | NaClČÜŅŗŌŚµēĮ÷×÷ÓĆĻĀµēĄė³ÉNa+ŗĶCl- | |
| C£® | ijŌŖĖŲÓÉ»ÆŗĻĢ¬±äĪŖÓĪĄėĢ¬£¬ŌņĖüŅ»¶Ø±»»¹Ō | |
| D£® | ÓŠµ„ÖŹ²Ī¼ÓµÄ»Æѧ·“Ó¦²»Ņ»¶Ø¶¼ŹĒŃõ»Æ»¹Ō·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Cl2”¢SO2¾łÄÜŹ¹Ę·ŗģČÜŅŗĶŹÉ«£¬ĖµĆ÷¶žÕß¾łÓŠŃõ»ÆŠŌ | |
| B£® | ·Ö±š³äĀśHCl”¢NH3µÄÉÕĘæµ¹ÖĆÓŚĖ®ÖŠŗóŅŗĆę¾łŃøĖŁÉĻÉż£¬ĖµĆ÷¶žÕß¾łŅ×ČÜÓŚĖ® | |
| C£® | FeÓėĻ”HNO3ČÜŅŗ”¢Ļ”H2SO4ČÜŅŗ·“Ó¦¾łÓŠĘųÅŻ²śÉś£¬ĖµĆ÷Į½·“Ó¦¾łĪŖÖĆ»»·“Ó¦ | |
| D£® | ¼ÓČČ·Ö±šŹ¢ÓŠĀČ»Æļ§ŗĶµāµÄĮ½Ö§ŹŌ¹Ü£¬ŹŌ¹Üµ×²æ¹ĢĢå¾ł¼õÉŁ£¬ĖµĆ÷¶žÕß¾ł·¢ÉśÉż»Ŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | ²Ł×÷ | ĻÖĻó | ½įĀŪ |
| A | ĻņAgNO3ČÜŅŗÖŠµĪ¼Ó¹żĮæ°±Ė® | ČÜŅŗ³ĪĒå | Ag+ÓėNH3?H2OÄÜ“óĮæ¹²“ę |
| B | ³£ĪĀĻĀ½«Alʬ·ÅČėÅØĻõĖįÖŠ | ĪŽĆ÷ĻŌ±ä»Æ | AlÓėÅØĻõĖį²»·“Ó¦ |
| C | ½«Ņ»Š”æéNa·ÅČėĪŽĖ®ŅŅ“¼ÖŠ | ²śÉśĘųÅŻ | NaÄÜÖĆ»»³ö“¼ōĒ»łÖŠµÄĒā |
| D | ½«Ė®ÕōĘųĶعż×ĘČȵÄĢś·Ū | ·ŪÄ©±äŗģ | ĢśÓėĖ®ŌŚøßĪĀĻĀ·¢Éś·“Ó¦ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ļ“µÓ³ĮµķŹ±£¬Ó¦ÓĆ²£Į§°ōĒįĒį½Į°č£¬Ź¹µĆ³Įµķ±ķĆęÉĻµÄŌÓÖŹČÜÓŚĖ®ÖŠ | |
| B£® | ½«Į½æéĪ“²ĮČ„Ńõ»ÆĤµÄĀĮʬ·Ö±šĶ¶Čė1mol?L-1CuSO4ČÜŅŗ”¢1mol?L-1CuCl2ČÜŅŗÖŠ£¬Ņ»¶ĪŹ±¼äŗó£¬ĀĮʬ±ķĆę¶¼¹Ū²ģ²»µ½Ć÷ĻŌµÄ·“Ó¦ĻÖĻó | |
| C£® | ÓɊ攢Ķ”¢Ļ”ĮņĖį¹¹³ÉµÄŌµē³ŲČÜŅŗÖŠ¼ÓČėŹŹĮæµÄH2O2ÄÜĢįøßµē³ŲµÄ·ÅµēŠ§ĀŹ | |
| D£® | ŌŚµķ·ŪČÜŅŗÖŠ¼ÓČėŹŹĮæĻ”ĮņĖįĪ¢ČČ£¬ŌŁ¼ÓÉŁĮæŠĀÖĘĒāŃõ»ÆĶ×ĒŅŗ¼ÓČČ£¬ČōĪŽ×©ŗģÉ«³Įµķ²śÉś£¬Ōņµķ·ŪĪ“·¢ÉśĖ®½ā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŅĻ©Ź¹äåĖ®ĶŹÉ«£»ŅŅ“¼Ź¹øßĆĢĖį¼ŲČÜŅŗĶŹÉ« | |
| B£® | ÓĶÖ¬µÄŌķ»Æ·“Ó¦£»ŅŅĻ©ÖĘŅŅ“¼ | |
| C£® | ÕįĢĒĖ®½ā£»ŅŅ“¼ŗĶŅŅĖįÖĘŅŅĖįŅŅõ„ | |
| D£® | ±½ÖĘäå±½£»±½ŗĶĒāĘųÖĘ»·¼ŗĶé |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com