
| A�� | ������O2���ڵIJ��缫���� | |
| B�� | O2���ڵIJ��缫��������ԭ��Ӧ | |
| C�� | �õ�صĸ�����ӦʽΪCH3CH2OH+3H2O-12e-=2CO2��+12H+ | |
| D�� | ������ͨ����������С����������������оƾ��ĺ����� |
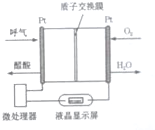
���� ��װ���к������ӽ���Ĥ����������ҺΪ���ԣ����������£��Ҵ�ȼ�ϵ���У��������Ҵ�ʧ���ӷ���������Ӧ���������������õ��ӵĻ�ԭ��Ӧ������ͼʾ�ó�����ȼ�ϵ�صķ�Ӧ���������ٸ���ԭ���ԭ��д���õ�صķ�Ӧʽ���жϣ�
��� �⣺A���Ҵ�ȼ�ϵ���У��������Ҵ�ʧ���ӷ���������Ӧ���������������õ��ӵĻ�ԭ��Ӧ����������������������O2���ڵIJ��缫�����·������һ�缫����A��ȷ��
B���Ҵ�ȼ�ϵ���У��������������õ��ӵĻ�ԭ��Ӧ��O2���ڵIJ��缫��������ԭ��Ӧ����B��ȷ��
C���õ�صĸ������Ҵ�ʧ���ӷ���������Ӧ����װ��ͼ��֪�ƾ��ڸ�����������������������Ӧ���ɴ��ᣬCH3CH2OH-4e-+H2O=4H++CH3COOH����C����
D������������ͨ����������С���Եó�����ת�Ƶ����ʵ��������ݵ缫��Ӧʽ���Լ�������������оƾ��ĺ�������D��ȷ��
��ѡC��
���� �������Ҵ�Ϊȼ�Ͽ�����ȼ�ϵ�أ��ѶȲ���ע���������ϵ缫��Ӧʽ����дҪ��ϵ������Һ������ԣ���ʹȼ�Ϻ���������ͬ������������Һ��ͬ���缫��ӦʽҲ��ͬ��


 53���ò�ϵ�д�
53���ò�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HCl���к�ǿ�����ԣ�������Ԫ�صķǽ����Ժ�ǿ | |
| B�� | ${\;}_{17}^{35}$Cl��${\;}_{17}^{37}$ClΪ��ͬ�ĺ��أ��в�ͬ�Ļ�ѧ���� | |
| C�� | 1.12LCl2����1.7NA�����ӣ�NA ��ʾ�����ӵ������� | |
| D�� | �����ɴ�KI��Һ���û���I2��˵���ȵķǽ����Աȵ�ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ������ ��� | V��0.20mol/L H2C2O4��Һ��/mL | �� | V��O��O1mol/L KMnO4��Һ��/mL | M��MnSO4���壩/g | T/�� | �� |
| �� | 2.0 | 0 | 4.0 | 0 | 5.0 | |
| �� | 2.0 | 0 | 4.0 | 0 | 2.5 | |
| �� | 1.0 | a | 4.0 | 0 | 2.5 | |
| �� | 2.0 | 0 | 4.0 | 0.1 | 2.5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
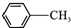 $��_{��}^{KMnO_{4}/H+}$
$��_{��}^{KMnO_{4}/H+}$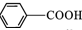

 ��
��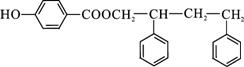 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ũ���������ˮ�ԣ������ʹ����̼�� | |
| B�� | ��SO2ͨ��Ʒ����Һ����Һ��ɫ����Ȼָ�ԭɫ����SO2ͨ����ˮ����ˮ��ɫ�����Ҳ�ָܻ�ԭɫ | |
| C�� | �ڷ�ӦSO2+2H2S�T3S+2H2O��SO2�������� | |
| D�� | ����ڹ����Ĵ�����ȼ�տ�������SO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϡ�����м���ͭ�ۣ�ͭ�۲��ܽ⣻�ټ���NaNO3���壬ͭ���Բ��ܽ� | |
| B�� | ��������Һ�м��˹���NaOH��Һ�����������ɫ���� | |
| C�� | ��ȥFeCl3��������FeCl2�����˹���ϡ���� | |
| D�� | Ũ���ᡢŨ�����ڼ����������ܽ�ľ̿����Ϊ������̼ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| �� | CH3COOH | HCN | HF | H2CO3 |
| ���볣�� | 1.8��10-5 | 4.9��10-10 | 6.6��10-4 | Ka1=4.3��10-2Ka2=5.6��10-11 |
| A�� | 5��������ҺpH��С��ϵpH��Na2CO3����pH��NaCN����pH��NaHCO3����pH��CH3COONa����pH��NaF�� | |
| B�� | 2mol•L-1HCN��1mol•L-1NaOH��Һ�������Ϻ����Һ�У�c��CN-����c��Na+����c��HCN�� | |
| C�� | ��Na2CO3��Һ�еμӹ�����HCN��Һ��2HCN+Na2CO3=2NaCN+CO2��+H2O | |
| D�� | �������ʵ�����Na2CO3��NaHCO3�Ļ��Һ�У�2c��Na+��=3c��CO32-��+3C��HCO3-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �÷�Ӧ��������ֻ��CuSO4 | |
| B�� | SO42-�Ȳ�����������Ҳ���ǻ�ԭ���� | |
| C�� | 1mol CuS04 ��ԭ��$\frac{1}{4}$mol S | |
| D�� | ����ԭ��S�ͱ�������S��������Ϊ7��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
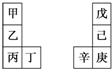 �ס�����Ԫ�������ڱ��е����λ��������������ԭ���������3�����һ�ֵ�������Ȼ��Ӳ���������ʣ���������ͬ����Ԫ�أ������ж���ȷ���ǣ�������
�ס�����Ԫ�������ڱ��е����λ��������������ԭ���������3�����һ�ֵ�������Ȼ��Ӳ���������ʣ���������ͬ����Ԫ�أ������ж���ȷ���ǣ�������| A�� | �������ԭ���������3 | |
| B�� | ��̬�⻯������ȶ��ԣ��죾������ | |
| C�� | ����������Ԫ���У�������ӵİ뾶��� | |
| D�� | �ҵĵ����ڿ�����ȼ�����ɵĻ�����ֻ�����Ӽ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com