
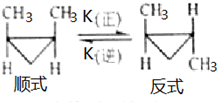 Ė³-1£¬2-¶ž¼×»ł»·±ūĶéŗĶ·“-1£¬2-¶ž¼×»ł»·±ūĶéæÉ·¢ÉśČēĶ¼×Ŗ»Æ£ŗ
Ė³-1£¬2-¶ž¼×»ł»·±ūĶéŗĶ·“-1£¬2-¶ž¼×»ł»·±ūĶéæÉ·¢ÉśČēĶ¼×Ŗ»Æ£ŗ·ÖĪö øł¾Żv£ØÕż£©=k£ØÕż£©c£ØĖ³£©£¬k£ØÕż£©=0.006s-1£¬ŅŌ¼°v£ØÄę£©=k£ØÄę£©c£Ø·“£©£¬k£ØÄę£©=0.002s-1£¬½įŗĻ»ÆŃ§Ę½ŗāדĢ¬Ź±ÕżÄę·“Ó¦ĖŁĀŹĻąµČ£¬æÉĮŠ³öÕż”¢·“ÅØ¶Č¹ŲĻµ£¬øĆ·“Ó¦µÄ»ī»ÆÄÜEa£ØÕż£©Š”ÓŚEa£ØÄę£©£¬ĖµĆ÷¶Ļ¼üĪüŹÕµÄÄÜĮæŠ”ÓŚ³É¼üŹĶ·ÅµÄÄÜĮ棬¼“øĆ·“Ó¦ĪŖ·ÅČČ·“Ó¦£®
½ā“š ½ā£ŗøł¾Żv£ØÕż£©=k£ØÕż£©c£ØĖ³£©£¬k£ØÕż£©=0.006s-1£¬Ōņv£ØÕż£©=0.006c£ØĖ³£©£¬v£ØÄę£©=k£ØÄę£©c£Ø·“£©£¬k£ØÄę£©=0.002s-1£¬Ōņv£ØÄę£©=0.002c£Ø·“£©£¬»ÆŃ§Ę½ŗāדĢ¬Ź±ÕżÄę·“Ó¦ĖŁĀŹĻąµČ£¬Ōņ0.006c£ØĖ³£©=0.002c£Ø·“£©£¬C£Ø·“-1£¬2-¶ž¼×»ł»·±ūĶ飩£ŗC£ØĖ³-1£¬2-¶ž¼×»ł»·±ūĶ飩=3£ŗ1£¬øĆ·“Ó¦µÄ»ī»ÆÄÜEa£ØÕż£©Š”ÓŚEa£ØÄę£©£¬ĖµĆ÷¶Ļ¼üĪüŹÕµÄÄÜĮæŠ”ÓŚ³É¼üŹĶ·ÅµÄÄÜĮ棬¼“øĆ·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬Ōņ”÷HŠ”ÓŚ0£¬
¹Ź“š°øĪŖ£ŗ3£ŗ1£» Š”ÓŚ£®
µćĘĄ ±¾Ģāæ¼²é»ÆŃ§Ę½ŗāµÄ¼ĘĖć£¬²ąÖŲӌѧɜµÄ·ÖĪö”¢¼ĘĖćÄÜĮ¦µÄ漲飬עŅā°ŃĪÕ»ÆŃ§Ę½ŗāĢŲÕ÷£¬½ā“šŹ±×¢ŅāĢå»įĶ¼ĻóµÄŗŅ壬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
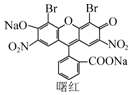
| A£® | ²»ÄÜÓėŃĪĖį·¢Éś·“Ó¦ | |
| B£® | ·Ö×ÓÖŠŗ¬1øöŹÖŠŌĢ¼Ō×Ó | |
| C£® | ÄÜ·¢ÉśČ”“ś”¢¼Ó³É”¢ĻūČ„·“Ó¦ | |
| D£® | 1 molŹļŗģ×ī¶ąÄÜÓė4 mol NaOH·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
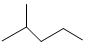 ±ķŹ¾µÄ·Ö×ÓŹ½C6H14£»ĻµĶ³ĆüĆū·ØµÄĆū³ĘŹĒ2-¼×»łĪģĶ飮
±ķŹ¾µÄ·Ö×ÓŹ½C6H14£»ĻµĶ³ĆüĆū·ØµÄĆū³ĘŹĒ2-¼×»łĪģĶ飮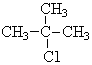 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | SO3+H2O”śH2SO4 | B£® | 2K+2H2O”ś2KOH+H2”ü | ||
| C£® | 2F2+2H2O”ś4HF+O2 | D£® | 2Na2O2+2H2O”ś4NaOH+O2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĘųĢ¬Ēā»ÆĪļµÄČČĪČ¶ØŠŌ£ŗb£¼c | B£® | ŗ¬dŌŖĖŲµÄŃĪČÜŅŗæÉÄܳŹ¼īŠŌ | ||
| C£® | Ō×Ó°ė¾¶£ŗd£¾c£¾b£¾a | D£® | a”¢bŗĶcČżÖÖŌŖĖŲÄÜŠĪ³ÉĄė×Ó»ÆŗĻĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1 molĒāĘųŗ¬ÓŠµÄŌ×ÓŹżĪŖNA | |
| B£® | NAøöĖ®·Ö×ÓÖŠŗ¬ÓŠĒāŌ×ÓµÄĪļÖŹµÄĮæĪŖ2 mol | |
| C£® | 1 mol ŃõĘųÖŠŗ¬ÓŠµÄ·Ö×ÓŹżĪŖ2NA | |
| D£® | 1 molČĪŗĪĪļÖŹ¶¼ŗ¬ÓŠNAøö·Ö×Ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| »Æѧ¼ü | Cl-Cl | O=O | O-H | H-Cl |
| ¼üÄÜ£ØkJ£®mol-1£© | 247 | 498 | 463 | 431 |
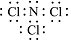 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±½·ÓÕ“ŌŚĘ¤·ōÉĻÓĆ“óĮæĖ®³åĻ“ | |
| B£® | ½šŹōÄĘ×Å»šŹ±£¬Į¢¼“ÓĆɳ×ÓøĒĆš | |
| C£® | ÖʱøĀČĘųŹ±£¬Ó¦ÓĆNaOHČÜŅŗĪüŹÕ¶ąÓąµÄĀČĘų | |
| D£® | ÖʱøŅŅĻ©Ź±ĻņŅŅ“¼ŗĶÅØĮņĖįµÄ»ģŗĻŅŗÖŠ¼ÓĖé“Éʬ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com