
分析 (1)水的电离是吸热反应,升高温度促进水电离,则溶液的离子积常数增大,通过比较(t℃)时和25℃时Kww的值判断;
(2)该温度下,中性溶液中c(H+)=1×10-6mol•L-1;水电离出来的氢离子浓度等于水电离出来的氢氧根的浓度;
(3)纯水中c(H+)=c(OH-),根据Kw=c(H+)×c(OH-)计算.
解答 解:(1)水的电离是吸热反应,升高温度促进水电离,氢离子和氢氧根离子浓度增大,则水的离子积常数增大,25℃时纯水中c(H+)=c(OH-)=10-7 mol/L,Kw=c(H+)•c(OH-)=10-14 ,某温度(T℃)时,水的离子积常数Kw=1×10-12>10-14,则该温度大于25℃,
故答案为:>;温度升高,水的电离程度增大,氢离子和氢氧根离子浓度增大;
(2)该温度下,中性溶液中c(H+)=1×10-6mol•L-1,则c(H+)=1×10-7mol•L-1的溶液呈碱性;溶液中水电离出来的氢离子浓度等于水电离出来的氢氧根的浓度,则NaOH溶质,由H2O电离出来的c(OH-)=1×10-7mol•L-1;
故答案为:碱性;1×10-7;
(3)纯水中c(H+)=c(OH-),某温度下纯水中c(H+)=2×10-7mol•L-1,则c(OH-)=2×10-7mol•L-1;Kw=c(H+)×c(OH-)=(2×10-7)2=4×10-14,
则c(OH-)=$\frac{4×1{0}^{-14}}{5×1{0}^{-6}}$=8×10-9mol•L-1;
故答案为:2×10-7mol•L-1;8×10-9mol•L-1.
点评 本题考查了水的电离、离子积常数的有关计算,侧重于对学生计算能力和分析能力的考查,注意离子积只和温度有关.题目难度中等.


 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:选择题
| A. | 2gH2中含有的分子数为NA | |
| B. | 标准状况下,22.4LH2O中含有的分子数为NA | |
| C. | 1mol/L K2SO4的溶液中含有钾离子数为2NA | |
| D. | 1mol钠原子中含有的电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铁和稀硝酸反应 | B. | 氢氧化钡和稀盐酸反应 | ||
| C. | 氢氧化钾溶液中通入硫化氢气体 | D. | 氢氧化钡溶液和稀硫酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 苯与溴水混合振荡,水层颜色变浅 | |
| B. | 裂化汽油与溴水混合振荡,水层颜色变浅 | |
| C. | 乙烯与水在一定条件下反应制取乙醇 | |
| D. | 乙烷与氯气在一定条件下反应制取的一氯乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入催化剂,反应速率加快,平衡常数也会随之变化 | |
| B. | 增加D的量,化学平衡逆向移动 | |
| C. | 增加A的量,B的转化率提高 | |
| D. | 平衡常数的表达式为K=$\frac{c(C)•c(D)}{c(A)^{2}•c(B)}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| T/℃ | 25 | 80 | 230 |
| K | 5×104 | 1 | 2×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
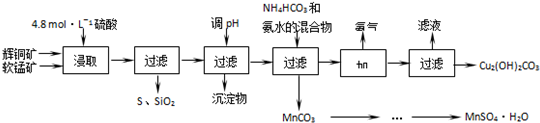
| 开始沉淀的pH | 沉淀完全的pH | |
| Fe3+ | 1.1 | 3.2 |
| Mn2+ | 8.3 | 9.8 |
| Cu2+ | 4.4 | 6.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 4 3 2 2 6 | B. | 0 2 1 0 1 2 | ||
| C. | 2 0 1 2 0 2 | D. | 2 2 2 2 1 4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com