
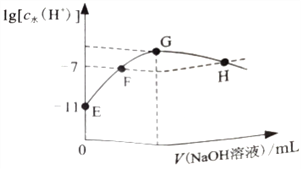
【题目】常温下,在新制氯水中滴加NaOH 溶液,溶液中水电离出来的c水(H+)的对数与NaOH 溶液体积之间的关系如图所示。下列推断正确的是
A. 用pH试纸测定E点对应的溶液,其pH=3
B. F、H点对应的溶液中都存在c(Na+)=c(Cl-)+c(ClO-)
C. 加水稀释H点对应的溶液,溶液的pH增大
D. G点对应的溶液中c(Na+)>c(Cl-)>c(ClO-)>c(OH-)>c(H+)
【答案】D
【解析】A. E点溶液为氯水,具有漂白性,pH试纸褪色,不能用pH试纸测定E点对应的溶液的pH,故A错误;B.根据电荷守恒,c(Na+)+ c(H+)=c(Cl-)+c(ClO-)+ c(OH-),F溶液中含有次氯酸钠、氯化钠和次氯酸,H点溶液中含有次氯酸钠、氯化钠和氢氧化钠,尽管溶液中由水电离的c(H+)相等,但溶液中溶质的浓度不等,溶液的pH不等,因此c(H+)≠ c(OH-),F点为中性,H点为碱性,因此H点溶液中不存在c(Na+)=c(Cl-)+c(ClO-),故B错误;C. 加水稀释H点对应的溶液,溶液的碱性减弱,pH减小,故C错误;D. G点对应的溶液为次氯酸钠溶液和氯化钠,且物质的量浓度相等,水的电离程度最大,次氯酸钠水解,溶液显碱性, c(Na+)>c(Cl-)>c(ClO-)>c(OH-)>c(H+),故D正确;故选D。


科目:高中化学 来源: 题型:
【题目】表是25℃时四种酸的电离平衡常数:
化学式 | CH3COOH | HA | HNO2 | H2CO3 |
Ka | Ka=1.8×10﹣5 | Ka=4.9×10﹣10 | Ka=4.6×10﹣4 | Ka1 =4.1×10﹣7 |
(1)用离子方程式表示NaNO2溶液呈碱性的原因
(2)25℃时,向向0.1molL﹣1 CH3COOH溶液中滴加NaOH溶液至c(CH3COOH):c(CH3COO﹣)=5:9,此时溶液pH=
(3)写出NaA溶液中通少量CO2的离子方程式
(4)25℃时,等物质的量浓度的HA、NaA混合溶液呈碱性,溶液中各离子浓度的大小顺序为
(5)已知HNO2不稳定,在稀溶液中也易分解生成NO与NO2 , 某同学分别取少量NaCl溶液与NaNO2溶液于试管中,分别滴加浓醋酸,以此来鉴别失去标签的NaCl溶液和NaNO2溶液,该方法(填“可行”或“不可行”),理由是
(6)已知NaHCO3溶液中存在HCO3H++CO32﹣ , 加水稀释时溶液中的c(H+)将(填“增大”或“减小”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质分类完全正确的一组是
选项 | 纯净物 | 混合物 | 电解质 | 非电解质 |
A | 纯净的空气 | 盐酸 | 硫酸 | 硫酸钡 |
B | 胆矾 | 肥皂水 | 氧化铝 | 干冰 |
C | 纯碱 | 玻璃 | 铝 | 蔗糖 |
D | 生石灰 | Fe(OH)3胶体 | 氯化钠 | 氯气 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是 ( )
A.丙烷分子中3个碳原子一定在同一条直线上
B.甲苯分子中7个碳原子都在同一平面上
C.3—甲基—1—丁炔分子中所有碳原子都在同一平面上
D.2-丁烯分子中4个碳原子有可能在同一条直线上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质在水溶液中的电离方程式书写错误的是( )
A.HCl=H++Cl-B.H2SO4=2H++SO42-
C.CaCl2=Ca2++2Cl-D.NaOH=Na++O2- +H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在固定体积的密闭容器中发生反应:2HI(g)![]() H2(g)+I2(g)△H>0,0~15s内c(HI)由0.lmol/L降到0.07mol/L,则下列说法正确的是
H2(g)+I2(g)△H>0,0~15s内c(HI)由0.lmol/L降到0.07mol/L,则下列说法正确的是
A. 当HI、H2、I2浓度之比为2:1:1时,说明该反应达平衡
B. c(HI)由0.07mol/L降到0.05mol/L所需的反应时间小于10s
C. 升高温度正反应速率加快,逆反应速率减慢
D. 0~15s内用I2表示的平均反应速率为:v(I2)=0.001mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用如图所示装置进行化学反应X+2Y![]() 2Z能量变化情况的研究。当往试管中滴加试剂Y时,看到U形管中液面甲处降、乙处升。关于该反应的下列叙述中正确的是
2Z能量变化情况的研究。当往试管中滴加试剂Y时,看到U形管中液面甲处降、乙处升。关于该反应的下列叙述中正确的是

①该反应为放热反应;②该反应为吸热反应;③生成物的总能量比反应物的总能量更高;④反应物的总能量比生成物的总能量更高;⑤该反应过程可以看成是“贮存“于X、Y内部的部分能量转化为热能而释放出来。
A. ①④⑤ B. ①④ C. ①③ D. ②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温下,将8molX与12molY的混合气体通入一个体釈内2L的密闭容器中,发生如下反应:X(g)+3Y(g)![]() 2Z(g),10min后反应达到平衡,其中Z的含量(体积分数)为25%。
2Z(g),10min后反应达到平衡,其中Z的含量(体积分数)为25%。
(1)平衡吋,Y的物貭的量浓度为_______。
(2)10min内,Z的平均反应速率为_______ 。
(3)达到平衡时,容器内起始吋与平衡吋的圧強之比是_______ 。
(4)不能証明该反应达到化学平衡状态的标志是_______ (填字母)
A.圧強不再发生変化 B.混合气体的相对分子貭量不再发生変化
C.X、Y、Z的分子数之比内1:3:2 D.混合气体的密度不変
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com