
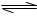 H2(g)+I2(g),体系中n(HI)随时间变化情况如下表:
H2(g)+I2(g),体系中n(HI)随时间变化情况如下表:| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| n(HI)/mol | 0.180 | 0.164 | 0.152 | 0.144 | 0.140 | 0.140 |
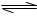 2HI(g)的平衡常数K的值为 。
2HI(g)的平衡常数K的值为 。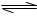 H2(g)+I2(g)的平衡常数,可采取的措施是 (选填字母)。
H2(g)+I2(g)的平衡常数,可采取的措施是 (选填字母)。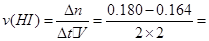 0.004mol/(L·min),由各物质的系数比可推出,
0.004mol/(L·min),由各物质的系数比可推出,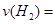 0.002mol/(L·min);
0.002mol/(L·min);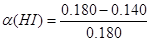 =22.2%
=22.2% H2(g)+I2(g)降温时碘蒸气浓度减小,平衡左移,正反应为吸热反应
H2(g)+I2(g)降温时碘蒸气浓度减小,平衡左移,正反应为吸热反应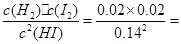 1/49
1/49

 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
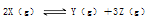
 向___(填“左”“右”或“不”,下同)移动;若将达到(1)的平衡体系中移走部分混合气体,则平衡向___移动。
向___(填“左”“右”或“不”,下同)移动;若将达到(1)的平衡体系中移走部分混合气体,则平衡向___移动。| A.无法确定 | B.前者一定大于后者 |
| C.前者一定等于后者 | D.前者一定小于后者 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 pC(g),在密闭容器中进行,下图表示在不同反应时间t、温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析,下列判断正确的是
pC(g),在密闭容器中进行,下图表示在不同反应时间t、温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析,下列判断正确的是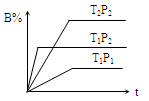
| A.T1<T2、P1>P2、m+n>p,⊿H <0; |
| B.T1>T2、P1<P2、m+n>p,⊿H >0; |
| C.T1>T2、P1<P2、m+n<p,⊿H >0; |
| D.T1<T2、P1>P2、m+n<p,⊿H <0; |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2SO3(g),在已达到平衡后的反应容器中充入少量18O2,一段时间后18O存在于:
2SO3(g),在已达到平衡后的反应容器中充入少量18O2,一段时间后18O存在于:| A.O2 | B.O2和SO2 | C.O2和SO3 | D.SO2、O2和SO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3(g)+CO2(g) 在不同温度下,该反应平衡状态部分数据见表。下列说法正确的是
2NH3(g)+CO2(g) 在不同温度下,该反应平衡状态部分数据见表。下列说法正确的是 | 温度 | 平衡浓度/ (mol L-1) | |
| c(NH3) | c(CO2) | |
| T1 | 0.1 | |
| T2 | | 0.1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 H2(g)+I2(g)达到平衡后,下列说法中,正确的是:
H2(g)+I2(g)达到平衡后,下列说法中,正确的是:
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2SO3(g)是制备硫酸的重要反应。下列叙述正确的是
2SO3(g)是制备硫酸的重要反应。下列叙述正确的是| A.催化剂V2O5增加该反应的正反应速率而不改变逆反应速率 |
| B.增大反应体系的压强,反应速率一定增大 |
| C.进入接触室的SO2和空气必须进行净化,且该反应不需要在高压下进行 |
| D.该反应是放热反应,降低温度将缩短反应达到平衡的时间 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L 。
7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L 。 2SO3(g) ΔH =" -" 196.6 kJ· mol-1
2SO3(g) ΔH =" -" 196.6 kJ· mol-1 2NO2(g) ΔH =" -" 113.0 kJ· mol-1
2NO2(g) ΔH =" -" 113.0 kJ· mol-1 SO3(g)+NO(g)的ΔH = kJ· mol-1。
SO3(g)+NO(g)的ΔH = kJ· mol-1。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com