
(18分)工业上从电解精炼铜的阳极泥(含金、银、铜、硒等单质)中提取硒的湿法工艺流程如下:
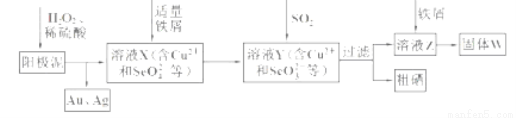
(1)向溶液X中加入铁屑的作用是______ ,此操作中不能加入过量铁粉的原因是______。
(2)检验溶液Z中阴离子的操作方法是______。
(3)过滤操作中要用到玻璃棒,请另举两例用到玻璃棒的实验或操作:______。
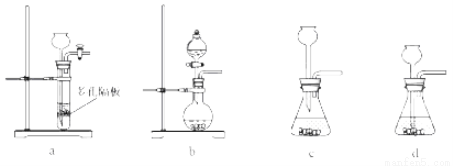
(4)实验室中制取SO2的原理为: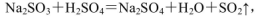 ,此处应使用______(填“较浓的硫酸”或“稀硫酸”),原因是 ______。制取SO2的装置,最好选用下图中的______。
,此处应使用______(填“较浓的硫酸”或“稀硫酸”),原因是 ______。制取SO2的装置,最好选用下图中的______。
(5)粗硒中硒的含量可用如下方法测定: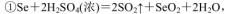
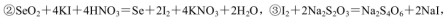 通过用Na2S2O3标准溶液(显碱性)滴定反应②中生成的I2来计算硒的含量。滴定操作中用到的玻璃仪器有_______。实验中准确称量0.1200g粗硒样品,滴定中消耗0.2000mol
通过用Na2S2O3标准溶液(显碱性)滴定反应②中生成的I2来计算硒的含量。滴定操作中用到的玻璃仪器有_______。实验中准确称量0.1200g粗硒样品,滴定中消耗0.2000mol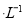 的Na2S2O3溶液27.60mL,则粗硒样品中硒的质量分数为 。
的Na2S2O3溶液27.60mL,则粗硒样品中硒的质量分数为 。
(18分)
(1)将SeO42-还原为SeO32-(2分) 过量铁粉会将Cu2+、SeO32-均还原为单质,不利于硒的分离(2分)
(2)取溶液Z少许置于试管中,滴加盐酸酸化的BaCl2溶液,有白色沉淀生成,说明溶液中含有SO42-(2分)
(3)粗盐提纯、一定物质的量浓度溶液的配制、物质的溶解、溶液的蒸发、浓硫酸的稀释等(2分,只要正确合理即给分)
(4)较浓的硫酸(2分) SO2易溶于水,用较浓的硫酸有利于 SO2的逸出(2分)
b(2分)
(5)锥形瓶、碱式滴定管(2分) 90.85%(2分)
【解析】
试题分析:(1)H2O2为强氧化剂,可将阳极泥中的Se单质氧化为SeO42-,根据流程图,加入适量铁屑后生成SeO32-,所以铁屑的作用是:将SeO42-还原为SeO32-;如果铁过量,会继续和Cu2+、SeO32-反应,均被还原为单质,不利于硒的分离。
(2)溶液Z含有的阴离子为SO42?,检验方法为:取溶液Z少许置于试管中,滴加盐酸酸化的BaCl2溶液,有白色沉淀生成,说明溶液中含有SO42-。
(3)粗盐提纯、溶液的蒸发,用玻璃棒搅拌,使溶液均匀受热;一定物质的量浓度溶液的配制,用玻璃棒搅拌、引流;物质的溶解、浓硫酸的稀释等。
(4)因为SO2易溶于水,用较浓的硫酸有利于 SO2的逸出,所以制取SO2用较浓的硫酸;a、多孔隔板适用于块状或颗粒比较大的固体与液体反应,Na2SO3为粉末状,不适合;b、分液漏斗适合粉末状固体与液体反应分液漏斗可控制液体的加入量;c、长颈漏斗的导管口在液面以上,气体从长颈漏斗逸出,不适合;d、长颈漏斗不能控制液体的加入量,所以最合适的为b项。
(5)Na2S2O3标准溶液为碱性,用碱性滴定管盛放,待测液用锥形瓶盛放;根据题目所给3个化学方程式可得对应关系:Se ~ SeO2 ~ 2I2 ~ 4Na2S2O3,则粗硒样品中硒的质量分数=0.0276L×0.2000mol/L×1/4×79g/mol÷0.1200g×100%=90.85%
考点:本题考查实验基本仪器、基本操作、实验方案的设计与分析、化学计算。


科目:高中化学 来源:2013-2014山东省烟台市高三5月适应性测试一理综化学试卷(解析版) 题型:填空题
(12分)【化学——化学与技术】
海水占地球总储水量的97.2%。若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源。
(1)多级闪蒸法是目前“海水淡化”的主要技术。该法是在一定条件下将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水。由此可判断多级闪蒸法是 (填“物理变化” 或“化学变化”)。
(2)利用海水晒盐的原理是 ;分离食盐晶体后的母液中含有KCl、MgCl2,经过分离、提纯后,可用于 。
(3)“氯碱工业”利用电解饱和食盐水制得重要化工产品。在氯碱工业中,隔膜法电解(如图甲所示)工艺逐渐被离子交换膜电解(如图乙所示)技术取代。

①写出两电极的反应式:阳极 ,阴极 。
②石棉隔膜的作用是 。离子交换膜电解槽中⑥、⑦分别是 、 。
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省潍坊市下学期期中考试高二化学试卷(解析版) 题型:选择题
分子式为C5H11Cl的同分异构体共有(不考虑立体异构)
A.6种B.7种C.8种D.9种
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省潍坊市下学期期中考试高一化学试卷(解析版) 题型:选择题
氢气在氯气中燃烧时产生苍白色火焰。在反应过程中,断裂1 mol H2中的化学键消耗
的能量为Q1kJ,断裂1 mol Cl2中的化学键消耗的能量为Q2 kJ,形成1 mol HCl中的化学
键释放的能量为Q3 kJ。下列关系式中一定正确的是
A.Q1+Q2<Q3 B.Q1+Q2>2Q3
C.Q1+Q2=2Q3D.Q1+Q2<2Q3
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省潍坊市下学期期中考试高一化学试卷(解析版) 题型:选择题
月球土壤中吸附着数百万吨的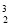 He,每百吨
He,每百吨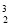 He核聚变所释放出的能量相当于目前人类一年消耗的能量。下列关于
He核聚变所释放出的能量相当于目前人类一年消耗的能量。下列关于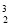 He的说法正确的是
He的说法正确的是
A.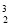 He原子核内含有2个中子 B.
He原子核内含有2个中子 B.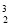 He原子核内含有3个质子
He原子核内含有3个质子
C.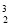 He原子核外有3个电子 D.
He原子核外有3个电子 D.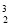 He和
He和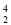 He是两种不同的核素
He是两种不同的核素
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省淄博市高三第三次模拟考试理综化学试卷(解析版) 题型:选择题
下列有关实验操作或现象的描述正确的是
A.制备Fe(OH)3胶体时,溶液呈红褐色停止加热
B.分馏实验中,温度计的水银球必须置于液面以下
C.向饱和CuSO4溶液中加入少量浓硫酸,析出白色固体
D.乙酸乙酯的制备实验中,将蒸气通到饱和NaOH溶液液面之上
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省淄博市高三二模理综化学试卷(解析版) 题型:填空题
(12分)【化学—化学与技术】
硫酸是工业生产中最为重要的产品之一,在化学工业的很多领域都要用到浓硫酸。
(1)在硫酸工业生产中,我国采用黄铁矿为原料生产SO2,反应的化学方程式为 ,该反应在 中进行(填设备名称)。
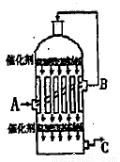
(2)为了有利于SO2转化为SO3,且能充分利用热能,采用了多层催化剂且有热交换器的 (填设备名称)中进行反应。在如图所示的装置中,C处流出的气体有 ;SO3进入 (填设备名称)用____ 吸收,得到浓硫酸或发烟硫酸。
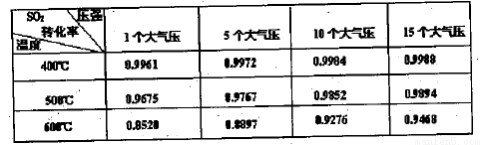
(3)实验测得SO2反应生成SO3的转化率与温度、压强有关,请根据下表信息,结合工业生产实际,选择最合适的生产条件是 。
(4)吸收塔排出的尾气中SO2的含量如果超过500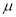 L/L,就要加以处理后才能排出,处理方法之一是用氨水洗涤烟气脱硫,用方程式表示氨水洗涤吸收塔排除的尾气的化学方程式
L/L,就要加以处理后才能排出,处理方法之一是用氨水洗涤烟气脱硫,用方程式表示氨水洗涤吸收塔排除的尾气的化学方程式
。
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省淄博市高一下学期期末考试化学试卷(解析版) 题型:选择题
下列分类不正确的是( )
A.纯碱、烧碱均属碱类 B.CO2、SiO2、SO2均属酸性氧化物
C.醋酸、硫酸、硝酸均属酸类 D.Na2CO3、Na2SO3、NaCl都属钠盐
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省济宁市3月质量检测高二化学试卷(解析版) 题型:选择题
仔细分析下列表格中烃的排列规律,判断排列在第16位烃的分子式是 ( )
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | …… |
C2H2 | C2H4 | C2H6 | C3H4 | C3H6 | C3H8 | C4H6 | C4H8 | C4H10 |
|
A.C6H12 B.C6H14 C.C7H12 D.C7H14
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com