
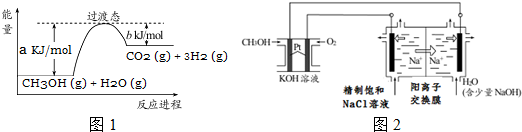
分析 (1)反应能量图中生成物的总能量大于反应物的总能量,则为吸热反应,结合热化学方程式的书写规则分析;
(2)依据已知热化学方程式,利用盖斯定律进行计算;
(3)①CH3OH燃料电池中通入甲醇的一极为负极,通入氧气的一极为正极,正极上氧气得电子生成氢氧根离子;
②由题意可知,氯离子放电生成ClO2,由元素守恒可知,有水参加反应,同时生成氢离子;在阴极发生2H++2e-=H2↑,设生成的氢气为xmol,由电子守恒可知,ClO2的物质的量为$\frac{2}{5}$xmol,已知从阴极处收集到的气体比阳极处收集到气体多 6.72L,即x-$\frac{2}{5}$x=$\frac{6.72L}{22.4L/mol}$;通过阳离子交换膜的阳离子为+1价离子,电子转移守恒计算阳离子的物质的量;
③电解时H+浓度减小,使得H2O?OH-+H+的平衡向右移动.
解答 解:(1)反应能量图中生成物的总能量大于反应物的总能量,则为吸热反应,由图可知,1mol 甲醇和1mol 水蒸气反应生成CO2和氢气吸收的热量为(a-b)kJ,反应热化学方程式为CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+(a-b)kJ/mol;
故答案为:CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+(a-b)kJ/mol;
(2)①CH3OH(g)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)△H=c kJ/mol;
②CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+(a-b)kJ/mol;
③H2O(g)═H2O(l)△H=d kJ/mol
依据盖斯定律计算(①×6-②×4+③×4)得到2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-(4a-4b-6c-4d)kJ/mol;
故答案为:2CH3OH(g)+3O2(g)=2 CO2(g)+4 H2O(l)△H=-(4a-4b-6c-4d)kJ/mol;
(3)①CH3OH燃料电池中通入甲醇的一极为负极,通入氧气的一极为正极,正极上氧气得电子生成氢氧根离子,溶液中氢氧根离子浓度增大,所以pH增大;
故答案为:增大;
②由题意可知,氯离子放电生成ClO2,由元素守恒可知,有水参加反应,同时生成氢离子;在阴极发生2H++2e-=H2↑,设生成的氢气为xmol,由电子守恒可知,ClO2的物质的量为$\frac{2}{5}$xmol,已知从阴极处收集到的气体比阳极处收集到气体多 6.72L,即x-$\frac{2}{5}$x=$\frac{6.72L}{22.4L/mol}$,解得x=0.5mol;故交换膜的阳离子的物质的量为0.5mol×2=1mol;
故答案为:1;
由题意可知,氯离子放电生成ClO2,由元素守恒可知,有水参加反应,同时生成氢离子,电极反应式为:Cl--5e-+2H2O=ClO2↑+4H+,
在阴极发生2H++2e-=H2↑,氢气的物质的量为$\frac{0.112L}{22.4L/mol}$=0.005mol,通过阳离子交换膜的阳离子为+1价离子,故交换膜的阳离子的物质的量为0.005mol×2=0.01mol,
故答案为:Cl--5e-+2H2O=ClO2↑+4H+;0.01;
③在阴极发生2H++2e-=H2↑,H+浓度减小,使得H2O?OH-+H+的平衡向右移动,OH-浓度增大,pH增大;
故答案为:在阴极发生2H++2e-=H2↑,H+浓度减小,使得H2O?OH-+H+的平衡向右移动,OH-浓度增大,pH增大.
点评 本题考查较为综合,题目难度中等,题目涉及盖斯定律的应用、电解原理、化学计算等,电解反应是难点、易错点,是对学生综合能力的考查,需要学生具有扎实的基础与分析解决问题的能力.


科目:高中化学 来源: 题型:选择题
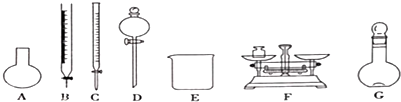
| A. | 需要称量NaClO固体的质量为144.0g | |
| B. | 定容摇匀后,若溶液液面低于容量瓶刻度线.不必再加水定容 | |
| C. | 除从如图所示的仪器中选择需要的以外.还-种玻填仪器 | |
| D. | 容量瓶用蒸馏水洗净后应烘干才能用于溶液配制.否則结果偏低 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 化工工业中常用乙苯脱氢的方法制备苯乙烯.
化工工业中常用乙苯脱氢的方法制备苯乙烯. (g)→
(g)→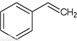 (g)+H2(g),△H=+117.6kJ/mol;①②的化学反应平衡常数分别为K1、K2,
(g)+H2(g),△H=+117.6kJ/mol;①②的化学反应平衡常数分别为K1、K2, (g)+CO(g)+H2O(g) △H=+158.8 kJ/mol该反应的化学平衡常数K=K1•K2(用K1、K2表示)
(g)+CO(g)+H2O(g) △H=+158.8 kJ/mol该反应的化学平衡常数K=K1•K2(用K1、K2表示)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu Al2O3 NaHCO3 | B. | Mg Al(OH)3 Na2CO3 | ||
| C. | Fe Al2O3,Al(OH)3 | D. | Al NaHCO3 Al2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高铁酸盐(含FeO42-离子)是新型、高效、多功能水处理剂,既能消毒杀菌又能净水 | |
| B. | 用硫酸清洗锅炉中的水垢 | |
| C. | 为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术 | |
| D. | 使用Na2S作沉淀剂,可有效除去废水中Cu2+和Hg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3种 | B. | 5种 | C. | 4种 | D. | 6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某吸热反应能自发进行,因此该反应是熵增反应 | |
| B. | 2NO(g)+2CO(g)═N2(g)+2CO2(g)在常温下能自发进行,则该反应的△H>0 | |
| C. | 反应NH3(g)+HCl(g)═NH4Cl(s)在室温下可自发进行,则该反应的△H<0 | |
| D. | CaCO3(s)═CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯中含苯酚杂质:加入溴水,过滤 | |
| B. | 乙醇中含氯乙烷杂质:加入水,萃取分液 | |
| C. | 乙醛中含乙酸杂质:加入碳酸钠溶液洗涤,分液 | |
| D. | 乙酸丁酯中含乙酸杂质:加入NaOH溶液洗涤,分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com