
【题目】NA为阿伏加德罗常数,下列物质所含分子数最少的是( )
A. 含NA个氢分子的氢气 B. 标准状况下22.4L氨气
C. 8g甲烷(甲烷的摩尔质量为16g·mol-1) D. 0.8mol二氧化碳
 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
【题目】(多选)在标准状况下,m g气体A与n g气体B的分子数相同,下列说法中不正确的是( )
A.两种气体A与B的相对分子质量之比为m:n
B.同质量气体A与B的分子数之比为m:n
C.同温同压下,A,B两气体的密度之比为n:m
D.相同状况下,同体积A,B两气体的质量之比为m:n
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向容积为2 L的密闭容器中充人2 mol A气体和1 mol B气体,在一定条件下发生如下反应:2A(g)+B(g) ![]() 3C(g);经2 s后达到平衡,测得C气体的浓度为0.6 mol·L-1。下列说法中正确的是
3C(g);经2 s后达到平衡,测得C气体的浓度为0.6 mol·L-1。下列说法中正确的是
①用物质A表示该反应的平均反应速率为0.2 mol·L-1·s-1
②用物质B表示该反应的平均反应速率为0.2 mol·L-1·s-1
③平衡时物质A与B的转化率相等
④平衡时物质B的浓度为0.2 mol·L-1
A. ①②③ B. ①③ C. ②④ D. ①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中和滴定中用已知浓度的稀盐酸滴定未知浓度的稀氨水,计算式与滴定氢氧化钠溶液类似:c1V1=c2V2,则( )
A.终点溶液偏碱性
B.终点溶液中c(NH4+)=c(Cl-)
C.终点溶液中氨过量
D.合适的指示剂是甲基橙而非酚酞
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂用软锰矿(主要为MnO2,含杂质Al2O3和闪锌矿(主要为ZnS,含杂质FeS) 共同生产干电池的原料Zn和MnO2,同时获得一些副产品,工艺流程如下:
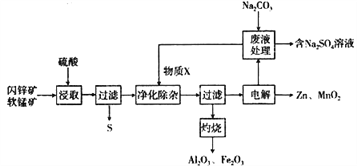
已知:硫酸浸取液的主要成分为ZnSO4、MnSO4、Fe2(SO4)3、Al2(SO4)3
(1)“浸取”时发生的反应中,还原产物为_______________ (填化学式)。
(2)①“净化除杂”时,加入的物质X可能为______________(填选项字母)。
A.MnCO3 B. Zn2(OH)2CO3 C.NaOH D. KOH
②相关离子开始沉淀和完全沉淀的pH如下表所示,加入X后,溶液pH应调整到________。
离子 | 开始沉淀pH | 完全沉淀pH |
Fe3+ | 2.3 | 3.2 |
A13+ | 4.2 | 5.4 |
Zn2+ | 7.2 | 8.0 |
Mn2+ | 8.3 | 9.8 |
(3)只用一种试剂,即可从 “灼烧”所得的Fe2O3和Al2O3混合物中分离得到Fe2O3。该反应
的离子方程式为____________________________________。
(4)“电解”时,发生反应的化学方程式为____________________________________。
(5)从Na2SO4溶液中得到芒硝晶体(Na2SO4 10H2O),需要进行的实验操作有______、_____、过滤、洗涤、干燥等.
(6)Zn和MnO2的传统生产工艺主要经历矿石焙烧、硫酸浸出、电解等过程,与传统工艺相比,该工艺流程的优点为________________________________。
(7)用生产的Zn和MnO2制成干电池,在碱性条件下工作时有MnOOH生成,则该电池正极的电极反应式为________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应mA(固)+nB(气)![]() pC(气)△H<O在一定温度下B的体积分数(B%)与压强变化的关系如图所示,下列叙述中正确的是
pC(气)△H<O在一定温度下B的体积分数(B%)与压强变化的关系如图所示,下列叙述中正确的是
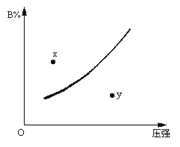
①m+n>P;②x点表示该反应的正反应速率大于逆反应速率;
③n>p;④x点比y点时的反应速率慢。
A. 只有① B. 只有②④ C. 只有①②④ D. 只有①和③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M、Q、R、X、Y为原子序数依次增大的短周期主族元素。M原子核外电子有6种运动状态,R和X同主族。Z、W是第四周期过渡元素,Z2+的外围电子数是W+的外围电子数的一半,W+没有未成对电子。请回答下列问题:
(1)W+的外围电子排布图为__________。
(2)M、Q和R第一电离能由小到大的顺序是________(用元素符号表示)。
(3)Q的气态氢化物极易溶于R的常见氢化物,其原因有__________________。该浓液显碱性,请用结构表示出两者的主要结合方式_________。
(4)在上述元素形成的微粒中,和MR2互为等电子体的有________(分子和离子各写一种),Q与Y形成的QY3分子的空间构型是__________。
(5)MR2晶体和W晶体的晶胞如图表示(●表示一个MR2分子或一个W原子)。
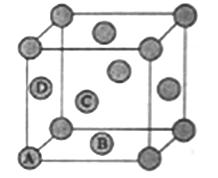
①在MR2晶体中,最近的分子间距为a㎝,则晶体密度为____g/㎝3(阿伏加德罗常数的值用NA表示,不必计算结果)。
②W晶体中A、B、C、D围成正四面体空隙,该晶胞中正四面体空隙的数目为_____。某种Z的硫化物晶体中S2-以W晶体中W原子的方式堆积,Z2+填充在正四面体空隙中,则Z2+的填充率(填充Z2+的正四面体空隙数和正四面体空隙总数之比)为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com