
| �¶� | 25�桫550�桫600�桫700�� |
| ��Ҫ�ɷ� | WO3 W2O5 WO2 W |
���� ��1����ѧƽ�ⳣ������ָ��һ���¶��£����淴Ӧ�ﵽƽ��ʱ��������Ũ�ȵĻ�ѧ���������ݵij˻����Ը���Ӧ��Ũ�ȵĻ�ѧ���������ݵij˻����õıȣ�ע����塢��Һ�岻��Ҫд����
��2���ɷ�Ӧ����ʽ֪�����ĵ�H2�����ɵ�ˮ�����ʵ�����ȣ��ٶ�H2��ˮ���������ʵ����ֱ�Ϊ2mol��3mol���ٸ���ת���ʶ�����㣻
���¶ȵ����ߣ�H2��ˮ����������ȼ�С��˵��ƽ��������Ӧ�ƶ���
��3���ɱ�����Ҫ�ɷ����¶ȹ�ϵ��֪����һ�η�ӦΪWO3��H2��Ӧ��W2O5��ͬʱ������H2O����ƽ��д����ʽ�����������εķ���ʽ���м�������������H2���ʵ���֮�ȣ�
��4����֪����WO2��s��+2H2��g���TW��s��+2H2O ��g����H=+66.0kJ•mol-1
��WO2��g��+2H2��g���TW��s��+2H2O ��g����H=-137.9kJ•mol-1
���ݸ�˹���ɣ���-�ڿɵã�WO2��s���TWO2��g������Ӧ��Ҳ������Ӧ�����㣻
��5���ɻ�ѧ����ʽ֪���ӷ���W��I2����γ���̬WI4�����������˶��Ľ����WI4���뻹û�лӷ���W�Ӵ����ڸ�����WI4�ֽ����ɵ�W�����ڻ�û�лӷ���W�ϣ��ƹܱ��¶Ƚϵͣ�WI4����ֽ⣬�����¶ȣ����淴Ӧ���ʶ��ӿ죮
��� �⣺��1��WO3��s��+3H2��g��$\stackrel{����}{?}$ W��s��+3H2O��g����ƽ�ⳣ��k=$\frac{{c}^{3}��{H}_{2}O��}{{c}^{3}��{H}_{2}��}$���ʴ�Ϊ��$\frac{{c}^{3}��{H}_{2}O��}{{c}^{3}��{H}_{2}��}$��
��2���ɷ�Ӧ����ʽ֪�����ĵ�H2�����ɵ�ˮ�����ʵ�����ȣ���H2��ƽ��ת����Ϊ$\frac{3mol}{2mol+3mol}$��100%=60%��
�����¶ȣ�H2��ˮ����������ȼ�С��˵������ʱƽ�������ƶ���������ӦΪ���ȷ�Ӧ��
�ʴ�Ϊ��60%�����ȣ�
��3���ɱ�����Ҫ�ɷ����¶ȹ�ϵ��֪����һ�η�ӦΪWO3��H2��Ӧ��W2O5��ͬʱ������H2O����Ӧ����ʽΪ��2WO3+H2$\frac{\underline{\;����\;}}{\;}$W2O5+H2O���ٶ���2molWO3����2WO3+H2$\frac{\underline{\;����\;}}{\;}$W2O5+H2O��W2O5+H2?$\frac{\underline{\;����\;}}{\;}$2WO2+H2O��WO2+2H2?$\frac{\underline{\;����\;}}{\;}$ W+2H2O��֪�����������ĵ����������ʵ���֮��Ϊ1mol��1mol��2mol��2=1��1��4��
�ʴ�Ϊ��2WO3+H2$\frac{\underline{\;����\;}}{\;}$W2O5+H2O��1��1��4��
��4����֪����WO2 ��s��+2H2 ��g��?W ��s��+2H2O ��g������H=+66.0kJ•mol-1
��WO2 ��g��+2H2?W ��s��+2H2O ��g������H=-137.9kJ•mol-1
��-�ڵ���WO2 ��s��?WO2 ��g�����ʡ�H=66.0kJ•mol-1-��-137.9kJ•mol-1��=+203.9 kJ•mol-1��
�ʴ�Ϊ��+203.9 kJ•mol-1��
��5����������ѧ����ʽ֪���ӷ���W��I2����γ���̬WI4�����������˶��Ľ����WI4���뻹û�лӷ���W�Ӵ����ڸ�����WI4�ֽ����ɵ�W��I2������W�����ڻ�û�лӷ���W�ϣ��ƹ��ڵ�I2��ѭ��ʹ�ã���a��b�ԣ��ƹܱ��¶Ƚϵͣ�WI4����ֽ⣬��c���������¶ȣ�Ҳ�ܼӿ�W��I2�ķ�Ӧ���ʣ���d����
�ʴ�Ϊ��a��b��
���� ���⿼���Ϊ�ۺϣ�Ϊ��Ƶ���㣬��Ŀ�漰��ѧƽ�ⳣ������д����Ӧ�ȵļ��㡢��ѧƽ���ƶ�ԭ������ѧƽ�����ȣ���Ŀѡ����زıȽ�İ�����Կ���ѧ��������Ϊ�����Ѷ��еȣ�


 �ƸԹھ��ο���ϵ�д�
�ƸԹھ��ο���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017�켪��ʡ�����ϵڶ���ģ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
���и���������ָ���������ܴ����������
A����c��CO32����=0.1 mol��L��1����Һ�У� K+��AlO2����Cl����NO3��
B���ڳ�������ˮ�������c��OH����=1��10��12 mol��L��1����Һ�У�Fe2+��ClO����Na+��SO42��
C���ڼ��뱽�ӻ�����ɫ����Һ�У� NH4+��Cl����Na+��SCN��
D������ʹ��ɫʯ����ֽ������Һ�У�S2O32����CO32����Na+��K+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ������ʡ��һ9���¿���ѧ���������棩 ���ͣ�ѡ����
��һ�������£�RO3n-�ͷ����ɷ������·�Ӧ��RO3n- + F2 + 2OH- == RO4- + 2F- + H2O���Ӷ���֪��RO3n-�У�Ԫ��R�Ļ��ϼ���
A��+4 B��+5 C��+6 D��+7

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
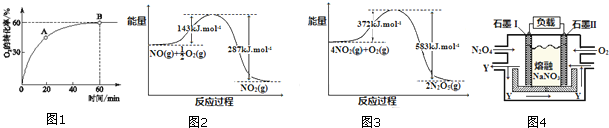
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
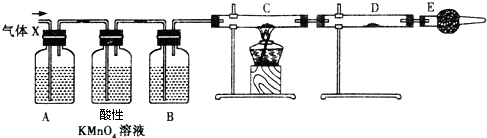
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
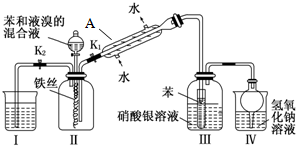
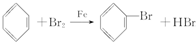
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
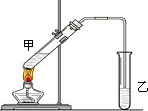 ��˵�����¾��ϴ��ر��㡱����ԭ���Ǿ��ڴ������������������ζ��������������ʵ����������Ҳ��������ͼ��ʾ��װ����ģ��ù��̣���ش��������⣺
��˵�����¾��ϴ��ر��㡱����ԭ���Ǿ��ڴ������������������ζ��������������ʵ����������Ҳ��������ͼ��ʾ��װ����ģ��ù��̣���ش��������⣺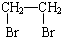 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com