
A.KMnO4 B.Ca(ClO)
科目:高中化学 来源: 题型:阅读理解
 化学在能源开发与利用中起着十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.
化学在能源开发与利用中起着十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.
| ||
时间(h) 物质的量(mol) |
0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0 | 0.20 | N2 | 1.00 | 1.00 |
| 4 |
| 27 |
| 4 |
| 27 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时约pH | |
| Fe3+ Fe2+ Cu2+ |
1.9 7.0 4.7 |
3.2 9.0 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
信息、材料、能源被称为新科技革命的“三大支柱”。其中无机非金属材料科学的发展和新型材料的实际应用能大大推动人类社会生活、科技和社会经济的发展。
⑴高温金属陶瓷广泛应用于火箭和导弹技术中。将铝粉、石墨和二氧化钛按一定比例混合均匀,涂在金属表面,在高温下煅烧:4Al + 3TiO2 + 3C![]() 2Al2O3 + 3TiC,留在金属表面的涂层是一种高温金属陶瓷。下列有关该反应说法正确的是
2Al2O3 + 3TiC,留在金属表面的涂层是一种高温金属陶瓷。下列有关该反应说法正确的是
A.TiO2是氧化剂,C、Al 是还原剂 B.TiC中钛元素为-4价
C.TiC不属于新型无机非金属材料 D.每生成1mol TiC转移电子4mol
⑵硅酸盐的成分较复杂,常改写成氧化物的形式(改写时注意金属氧化物写在前,非金属氧化物写在后,低价在前,高价在后,H2O一般写在最后)。
①将下列硅酸盐改写成氧化物的形式:镁橄榄石(Mg2SiO4)_______,②高岭石[(Al2(Si2O5)(OH)4]_____。
②许多含氧酸及其盐类均可以类似地改写为氧化物形式,请继续改写以下物质: HNO3______;HCOOH________;KAl(SO4)2?12H2O_________。通过以上改写可知,HNO3的酸酐为________,HCOOH与浓硫酸反应可制得________气体。
③已知在一定条件下,Fe在Cl2中燃烧可以生成Fe3Cl8,它可以看作是FeCl2?2FeCl3,类似地,碘与铁在一定条件下可得到Fe3I8,则它可以看作是__________。
⑶请指出在建筑行业中出现的“豆腐渣”工程可能的因素。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年北京市房山区高三上学期期末考试化学试卷(解析版) 题型:填空题
利用含锰废水(主要含Mn2+、SO42-、H+、Fe2+、Al3+、Cu2+)可制备高性能磁性材料碳酸锰(MnCO3)。其中一种工业流程如下:
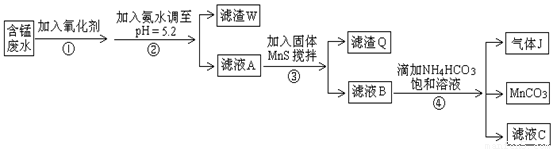
已知某些物质完全沉淀的pH值如下表:
|
沉淀物 |
Fe(OH)3 |
Al(OH)3 |
Cu(OH)2 |
Mn(OH)2 |
CuS |
MnS |
MnCO3 |
|
沉淀完全时的PH |
3.7 |
5.2 |
6.4 |
9.8 |
≥0 |
≥7 |
≥7 |
回答下列问题:
(1)若下列物质均能把Fe2+氧化为Fe3+,则过程①中可选择加入的氧化剂是 。
a.Cl2 b.MnO2 c.浓HNO3 d.H2O2
(2)过程②中,所得滤渣的成分是 。
(3)过程③中,搅拌的目的是 ,发生反应的离子方程式是 。
(4)过程④中,若生成的气体J可使澄清石灰水变浑浊,则生成MnCO3反应的离子方程式是___________。
(5)由MnCO3可制得重要的催化剂MnO2,MnCO3 + O2
→ MnO2 + CO2。
O2
→ MnO2 + CO2。
现在空气中加热 460.0 g的MnCO3,得到332.0 g产品,若产品中杂质只有MnO,则该产品中MnO2的质量分数是 。(摩尔质量/g·:MnCO3 115 MnO2 87 MnO 71)
查看答案和解析>>
科目:高中化学 来源:2012-2013学年浙江省瑞安十校高三上学期期末联考理综化学试卷(解析版) 题型:填空题
化学在能源开发与利用中起着十分关键的作用。氢气是一种新型的绿色能源,又是一种重要的化工原料。
I.氢氧燃料电池能量转化率高,具有广阔的发展前景。现用氢氧燃料电池进行如图实验(图中所用电极均为惰性电极):

(1)对于氢氧燃料电池中,下列表达不正确的是________
A.a电极是负极,OH-移向正极
B.b电极的电极反应为:O2+2H2O+4e-=4OH-
C.电池总反应式为:2H2+O2 2H2O
2H2O
D.电解质溶液的pH保持不变
E.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
(2)上图装置中盛有100mL、0.1mol·L—1AgNO3溶液,当氢氧燃料电池中消耗氢气112mL(标准状况下)时,则此时上图装置中溶液的pH=________(溶液体积变化忽略不计)
II.氢气是合成氨的重要原料。工业上合成氨的反应是:
N2(g)+3H2(g) 2NH3(g)
ΔH=-92.20 kJ·mol-1。
2NH3(g)
ΔH=-92.20 kJ·mol-1。
(1)下列事实中,不能说明上述可逆反应已达到平衡的是________
①单位时间内生成2n mol NH3的同时生成3n mol H2
②单位时间内生成n mol N—H的同时生成n mol N≡N
③用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1︰3︰2
④N2、H2、NH3的体积分数不再改变
⑤混合气体的平均摩尔质量不再改变
⑥混合气体的总物质的量不再改变
(2)已知合成氨反应在某温度下2L的密闭容器中进行,测得如下数据:
|
时间(h) 物质的量(mol) |
0 |
1 |
2 |
3 |
4 |
|
N2 |
1.50 |
n1 |
1.20 |
n3 |
1.00 |
|
H2 |
4.50 |
4.20 |
3.60 |
n4 |
3.00 |
|
NH3 |
0 |
0.20 |
n2 |
1.00 |
1.00 |
根据表中数据计算:
反应进行到2小时时放出的热量为________
0~1小时内N2的平均反应速率________mol·L-1·h-1;
③此条件下该反应的化学平衡常数K=________(保留两位小数)
④反应达到平衡后,若往平衡体系中再加入N2、H2和NH3各1.00mol,化学平衡将向________ 方向移动(填“正反应”或“逆反应”、“不移动”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com