
【题目】某温度时,两个恒容密闭容器中仅发生反应2NO2(g)2NO(g) +O2(g) ΔH > 0。实验测得:υ正(NO2)=k正c2(NO2),υ逆(NO)=k逆c2(NO)·c(O2),k正、k逆为化学反应速率常数,只受温度影响。
容器 编号 | 起始浓度(mol·L1) | 平衡浓度(mol·L1) | ||
c(NO2) | c(NO) | c(O2) | c(O2) | |
Ⅰ | 0.6 | 0 | 0 | 0.2 |
Ⅱ | 0.6 | 0.1 | 0 | |
下列说法不正确的是
A.Ⅰ中NO2的平衡转化率约为66.7%
B.Ⅱ中达到平衡状态时,c(O2)<0.2mol·L1
C.该反应的化学平衡常数可表示为![]()
D.升高温度,达到平衡状态时 Ⅰ中c(O2)<0.2mol·L1
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案科目:高中化学 来源: 题型:
【题目】钻钼系催化剂主要用于石油炼制等工艺,从废钴钼催化剂(主要含有![]() 、CoS和
、CoS和![]() )中回收钴和钼的工艺流程如图:
)中回收钴和钼的工艺流程如图:

已知:浸取液中的金属离子主要为![]() 、
、![]() 、
、![]() 。
。
(1)钼酸铵![]() 中
中![]() 的化合价为________,
的化合价为________,![]() 在空气中高温焙烧产生两种氧化物:
在空气中高温焙烧产生两种氧化物:![]() 和________(填化学式)。
和________(填化学式)。
(2)为了加快酸浸速率,可采取的措施为________(任写一条)。
(3)若选择两种不同萃取剂按一定比例(协萃比)协同萃取![]() 和
和![]() ,萃取情况如图所示,当协萃比
,萃取情况如图所示,当协萃比![]() ________,更有利于
________,更有利于![]() 的萃取。
的萃取。

(4)操作Ⅰ的名称为________。
(5)向有机相1中滴加氨水,发生的离子方程式为________。
(6)![]() 萃取的反应原理为
萃取的反应原理为![]() ,向有机相2中加入
,向有机相2中加入![]() 能进行反萃取的原因是________(结合平衡移动原理解释)。
能进行反萃取的原因是________(结合平衡移动原理解释)。
(7)水相2中的主要溶质除了![]() ,还有________(填化学式)。
,还有________(填化学式)。
(8)![]() 可用作电极,若选用
可用作电极,若选用![]() 电解质溶液,通电时可转化为
电解质溶液,通电时可转化为![]() ,其电极反应式为________。
,其电极反应式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由于电影《我不是药神》中对抗癌药物格列卫的关注,我国政府在2018年已经将格列卫等部分抗癌药物纳入医保用药,解决了人民群众用药负担。格列卫在其合成过程中的一种中间产物结构表示如下: 。下列有关该中间产物的说法不正确的是()
。下列有关该中间产物的说法不正确的是()
A. 该药物中间体属于芳香烃
B. 该药物中间体中含有三种官能团
C. 该药物中间体的所有碳原子可能共面
D. 该药物中间体可以发生加成反应和取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,是实验室制备乙酸乙酯的装置。a试管中加入3 mL 95%的乙醇、2 mL 浓硫酸、2 mL 冰醋酸;b试管中是饱和碳酸钠溶液。连接好装置,用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验。

(1)在a试管中除了加入乙醇、浓硫酸和乙酸外,还应放入____________,目的是____________。
(2)试管b中观察到的主要现象是__________________________。
(3)实验中球形干燥管除起冷凝作用外,另一个重要作用是_________________。
(4)饱和Na2CO3溶液的作用是__________________________________________。
(5)反应结束后,将试管中收集到的产品倒入分液漏斗中,然后分液,得到乙酸乙酯。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,对应的操作、现象及实验原理或结论均正确的是
实验目的 | 操作和现象 | 实验原理或结论 | |
A | 验证AgI和 AgCl的 Ksp大小 | 向1mL 1mol·L-1NaCl溶液中滴加2滴 2mol·L-1 AgNO3溶液,生成白色沉淀;再滴加 2滴1mol·L-1KI溶液,白色沉淀变成黄色沉淀 | AgCl(s)+I-(aq) |
B | 比较HClO和 HF溶液的酸性 | 室温下,用pH试纸分别测定浓度为0.1mol·L-1NaClO 溶液、0.1mol·L-1NaF 溶液的pH | 酸越弱,酸根离子水解程度越大,其盐溶液碱性越强 |
C | 提纯混有少量硝酸钾的氯化钠固体 | 在较高温度下制得浓溶液再冷却结晶、过滤、干燥 | 氯化钠溶解度随温度升高变化不大,而硝酸钾溶解度随温度升髙显著增大 |
D | 检验某溶液中是否含有CO32- | 先滴加盐酸产生气泡,将该气体通入澄清石灰水中,有白色沉淀生成 | 该溶液中一定含有CO32- |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,有机化合物 Y 可发生重排反应:

下列说法不正确的是( )
A.X、Y、Z互为同分异构体
B.1 mol X最多能与3 mol H2发生加成反应
C.1 mol Y最多能与2 mol NaOH发生反应
D.通过调控温度可以得到不同的目标产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)Ge在周期表中的位置__________,基态Ge原子的核外电子排布式为[Ar] _______,有 __________个未成对电子。
(2)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Ge、O两元素电负性由大至小的顺序是 _________。
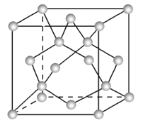
(3)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为 ________,微粒之间存在的作用力是___________。
(4)晶胞参数,描述晶胞的大小和形状,已知Ge单晶的晶胞参数a=565.76 pm(1pm=10-12m),其密度为_______g·cm-3(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Na2CO3、NaHCO3混合液中逐滴加入稀盐酸,生成气体的量随稀盐酸加入量的变化关系如图,则下列离子组在对应的溶液中一定能大量共存的是

A.a点对应的溶液中:Ca2+、Mg2+、Br-、NO3-
B.b点对应的溶液中:Al3+、Fe3+、MnO4-、NO3-
C.c点对应的溶液中:Na+、Ca2+、NO3-、Cl-
D.d点对应的溶液中:F-、NO3-、Fe2+、Ag+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】防治污染要坚决打好蓝天、碧水、净土三大保卫战。某工厂拟综合处理含NH4+废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:

下列说法正确的是( )
A.固体1的成分是CaCO3、CaSO3
B.向气体1中通入的空气需要过量
C.捕获剂所捕获的气体主要是CO
D.处理含NH4+废水时,发生的反应为NH4++5NO2-+4H+=6NO↑+4H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com