
【题目】25℃时,将氨水逐滴加入到稀硫酸中,当溶液的pH=7时,下列关系正确的是( )
A. [NH4+]=[SO42-] B. [NH4+]>[SO42-]
C. [NH4+]<[SO42-] D. [OH-]+[SO42-]=[H+]+[NH4+]
科目:高中化学 来源: 题型:
【题目】关于浓硫酸的性质,下列说法错误的是( )
A.浓硫酸的吸水性是化学变化B.浓硫酸有酸性和强氧化性
C.浓硫酸有吸水性和脱水性D.浓硫酸能做干燥剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定容积的密闭容器中进行反应;N2(g)+3H2(g)![]() 2NH3(g)。己知反应过程中某一时刻N2、H2、NH3的浓度分别为0.1mol/L、0.3mol/L、0.2mol/L。当反应达到平衡时,可能存在的数据是
2NH3(g)。己知反应过程中某一时刻N2、H2、NH3的浓度分别为0.1mol/L、0.3mol/L、0.2mol/L。当反应达到平衡时,可能存在的数据是
A. N2为0.2mol/L;H2为0.6mol/L B. N2为0.15mol/L
C. N2、H2均为0.18 mol/L D. NH3为0.4mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用盐酸作标准液滴定待测浓度的NaOH溶液,若用甲基橙作指示剂,当滴定达终点时,消耗盐酸V1mL;若用酚酞作指示剂,当滴定达终点时,消耗盐酸V2mL;则两种情况下消耗盐酸的体积关系是( )
A. V1>V2 B. V1=V2 C. V1<V2 D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜及其合金是人类最早使用的金属材料,铜的化合物在现代生活和生产中有着广泛的应用。
(1)请写出铜的基态原子核外电子排布式:___________。
(2)铜的熔点比钙的高,其原因是____________。
(3)金属铜的堆积方式为下图中的______(填字母序号)。

(4)科学家通过 X 射线推测,胆矾的结构如下图所示。

胆矾的阳离子中心原子的配位数为______,阴离子的空间构型为_______。胆矾中所含元素的电负性从大到小的顺序为_________(用元素符号作答)。
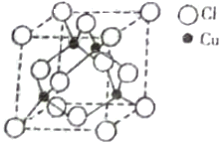
(5)铜与Cl原子构成晶体的晶胞结构如右图所示,该晶体的化学式为______,已知该晶体的密度为 4.14g/cm3,则该晶胞的边长为_______pm(写计算式)。将该物质气化后实验测定其蒸汽的相对分子质量为 198,则其气体的分子式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学工业中Mn可用作氧化剂、助燃剂、活性电极材料、催化剂、油漆和油墨的干燥剂等,碳酸锰矿可作为制备MnO2原料
(1)已知25℃,101kPa时有如下的三个热化学方程式
①MnCO3(s) ![]() MnO(s)+CO2(g) △H1=+116 6kJ/mol
MnO(s)+CO2(g) △H1=+116 6kJ/mol
②2MnO(s)+O2(g) ![]() 2MnO2(s) △H2=-272.0kJ/mol
2MnO2(s) △H2=-272.0kJ/mol
③2MnCO3(s)+O2(g) ![]() 2Mn2(s)+2CO2(g) △H3
2Mn2(s)+2CO2(g) △H3
则△H3=_________;反应②在________条件下(填“高温”、“低温”或“任何温度”)能自发进行。
(2)在密闭容器中投入足量的 MnCO3,在一定条件下发生反应:MnCO3(s) ![]() Mno(s)+CO2(g) △H1=+116.6kJ/mol。一定温度下,达到平衡状态时p(CO2)=bMPa
Mno(s)+CO2(g) △H1=+116.6kJ/mol。一定温度下,达到平衡状态时p(CO2)=bMPa
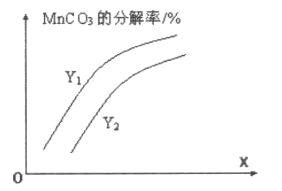
①温度、压强对碳酸锰平衡分解率的影响如图所示。图中Y1____Y2(填“>”、“<”或“=”)。
②保持温度不变,将体积扩大至原来的3倍,则容器内压强p(CO2)的变化范围为_______。
③若温度不变,将容器体积压缩至原来的一半,达到新平衡时,与原平衡状态相比,下列物理量一定不变的是________ (填字母)
A.CO2的质量 B. MnCO3的质量 C.MnCO3的分解率
D.化学平平衡常数 E.CO2的物质的量浓度
(3)在4L恒容密闭容器中,充入足量量的MnCO3(s)和a molO2(g),在一定温度下发生反应:MnCO3(s)+O2(g) ![]() 2MnO2(s)+2CO2(g),经过5min该反应刚好达到平衡状态,且该段时间内CO2的化学反应速率为0.2molL-1·min-1若该条件该反应的化学平衡常数K=0.5,则a=____。
2MnO2(s)+2CO2(g),经过5min该反应刚好达到平衡状态,且该段时间内CO2的化学反应速率为0.2molL-1·min-1若该条件该反应的化学平衡常数K=0.5,则a=____。
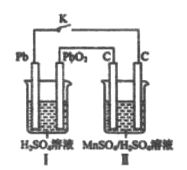
(4)现以铅蓄电池为电源,用石墨为电极,电解MnSO4和H2SO4混合液来制备MnO2,装置如图所示,阳极的电极反应式为___________,当蓄电池中有2mol H+被消耗时,则理理论上能生成MnO2________g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【题目】生产上用过量烧碱溶液处理某矿物(含Al2O3、MgO),过滤后得到滤液用NaHCO3溶液处理,测得溶液pH和Al(OH)3生成的量随加入NaHCO3溶液体积变化的曲线如下:

下列有关说法不正确的是
A. 原NaHCO3溶液中c(H2CO3)+c(HCO3-)+c(CO32-)=0.8moL/L
B. a点水的电离程度小于c点水的电离程度
C. a点溶液中存在:c(Na+)+c(H+)=c(AlO2-)+(OH-)
D. 生成沉淀的离子方程式为:HCO3-+AlO2-+H2O=Al(OH)3↓+CO32-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com