
【题目】某实验小组为了证明SO2和Cl2的漂白性,设计了如图所示的实验装置:
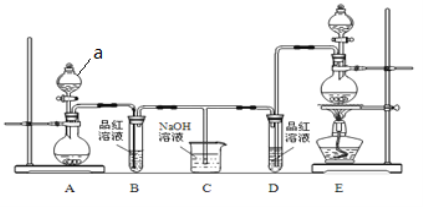
(1)仪器a的名称是____。
(2)利用图中A装置进行实验室制备SO2的化学方程式是____。
(3)反应开始后,发现B、D两个试管中的品红溶液都褪色。停止通气后,给B、D两支试管中的液体加热,试管中现象是:B__;D___。据此,说明SO2的漂白特点是_____。
(4)装置C的作用是_______。
(5)将等物质的量的SO2和Cl2同时通入水中,所得水溶液没有漂白性的原因是(用离子方程式表示)________。要检验此时溶液中生成的负一价阴离子,方法是_____(要求答出具体实验操作、现象及结论)。
【答案】分液漏斗 Na2SO3 +H2SO4=Na2SO4 +SO2↑+H2O 恢复红色 仍为无色 可逆性(受热可复原) 吸收多余SO2、Cl2,防止污染空气 SO2+Cl2+2H2O=4H++SO42-+2Cl- 取样,加入过量的Ba(NO3)2溶液,静置,取上层清液,加入AgNO3溶液,若有白色沉淀生成,则溶液中有Cl-
【解析】
(1)根据仪器的构造可知仪器a的名称是分液漏斗,故答案为:分液漏斗。
(2)实验室中常用亚硫酸钠跟浓硫酸起反应制取二氧化硫,反应的化学方程式是Na2SO3+H2SO4=Na2SO4 +SO2↑+H2O,故答案为:Na2SO3 +H2SO4=Na2SO4 +SO2↑+H2O。
(3)次氯酸的漂白性是利用次氯酸的强氧化性,二氧化硫的漂白性是利用二氧化硫和有色物质生成无色物质,次氯酸的漂白性是永久性的,二氧化硫的漂白性是暂时的;加热时,次氯酸漂白过的溶液无变化,二氧化硫和有色物质生成的无色物质不稳定,加热时能重新变成红色,故答案为:恢复红色,仍为无色,可逆性(受热可复原)。
(4)氯气和二氧化硫均是大气污染物,需要尾气处理,则装置C的作用是吸收多余SO2、Cl2,防止污染空气,故答案为:吸收多余SO2、Cl2,防止污染空气。
(5)氯气有强氧化性,二氧化硫有还原性,二者能按1:1发生氧化还原反应而使气体失去漂白性,反应的离子方程式为SO2+Cl2+2H2O=4H++SO42-+2Cl-;溶液中生成的负一价阴离子为Cl-,检验Cl-的方法为:取样,加入过量的Ba(NO3)2溶液,静置,取上层清液,加入AgNO3溶液,若有白色沉淀生成,则溶液中有Cl-,故答案为:SO2+Cl2+2H2O=4H++SO42-+2Cl-;取样,加入过量的Ba(NO3)2溶液,静置,取上层清液,加入AgNO3溶液,若有白色沉淀生成,则溶液中有Cl-。


科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F均为短周期主族元素,且原子序数依次递增。A的原子核内无中子,B的原子最外层电子数是次外层电于数的2倍,C是地壳中含量最多的元素,D是短周期中金属性最强的元素,E与F位置相邻,F是同周期元素中原子半径最小的元素。
完成下列填空题:
(1)B在元素期表中的位置为_______,1个C原子核外有____个未成对的电子。
(2)D、E、F三种元素形成简单离子其半径由l大到小的顺序是_____________。(用离子符号表示)。
(3)写出D与C形成化合物的电子式______、_______。
(4)常温下,1molA的单质在C的单质中完全燃烧生成液态化合物,并放出286kJ的热量,该反应的热化学方程式为______________。
(5)非金属性的强弱:E_____F(填“强于”、“弱于”、“无法比较”),试从原子结构的角度解释其原因________________。
(6)Na2SO3可用作漂白织物时的去鼠剂。Na2SO3溶液及收Cl2后,溶液的酸性增强。写出该反应的离子方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g)![]() 2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。请回答下列问题:
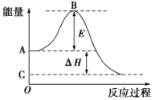
(1)图中A点表示:________________________________________;C点表示:________________。E的大小对该反应的反应热________(填“有”或“无”)影响。
(2)图中ΔH=________kJ·mol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH1=-Q1
②H2(g)+![]() O2(g)===H2O(g) ΔH2=-Q2
O2(g)===H2O(g) ΔH2=-Q2
③H2(g)+![]() O2(g)===H2O(l) ΔH3=-Q3
O2(g)===H2O(l) ΔH3=-Q3
常温下取体积比为4∶1的甲烷和氢气的混合气体11.2 L(已折合成标准状况)经完全燃烧恢复到常温,放出的热量为
A. 0.4Q1+0.05Q2 B. 0.4Q1+0.1Q2
C. 0.4Q1+0.05Q3 D. 0.4Q1+0.1Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢是宇宙中含量最高的元素,占宇宙总质量的75%,应用前景十分广阔。
(1)氢有1H、2H、3H三种常见的核素,它们互称为____;氢元素的相对原子质量约为1.008,则三种核素中丰度(百分含量)最高的是____。
(2)2H2O可用作核反应堆的减速剂,1个 2H2O分子中所含中子的个数为___。
(3)H可与N形成多种分子,其中某分子含18个e-、6个原子,则该分子的结构式为__。
(4)工业上用C和H2O制取H2。已知:
①C(s) + H2O(g) = H2(g) + CO(g) ΔH1 ②C(s) + 2H2O(g) = 2H2(g) + CO2(g) ΔH2
则CO(s) + H2O(g) = H2(g) + CO2(g) ΔH =__(用ΔH1、ΔH2表示)。
(5)NaBH4是一种重要的储氢载体。
①B在元素周期表中的位置为___。
②NaBH4(s)与H2O (l)反应生成NaBO2(s)和一种气体,在25℃,101kPa下,已知每消耗3.8g NaBH4放热21.6kJ,则该反应的热化学方程式为________;反应前后B的化合价不变,则反应消耗1molNaBH4时转移的电子数目为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,体积一定的容器内发生可逆反应3X(g)+Y(g)![]() 4Z(g),达到平衡的标志是 ( )
4Z(g),达到平衡的标志是 ( )
A. 密度不随时间的变化
B. 3v(正,X)=v(逆,Y)
C. 单位时间内生成3n mol X,同时消耗n mol Y
D. 压强不随时间变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 碱金属的单质中,锂的还原性最强
B. 第ⅠA族元素比第ⅡA族元素的金属性强
C. 最外层电子数为6的原子都是非金属原子
D. 随着核电荷数的递增,卤素元素的气态氢化物的稳定性逐渐减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列观点正确的是( )
A. 化合物电离时,生成的阴离子是氢氧根离子的是碱
B. 某化合物的熔融状态能导电,该化合物中一定有离子键
C. 某化合物的水溶液能导电,该化合物可能是非电解质
D. 某纯净物在常温下为气体,则组成该物质的微粒一定含有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶液中只可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物貭的量之向的关系如图所示。则下列説法正确的是( )

A. 溶液中的阳离子一定含有H+、Mg2+、Al3+,可能含有Fe3+
B. 溶液中一定不含CO32-和NO3-,一定含有SO42-
C. 溶液中C(NH4+)=0.2mol/L
D. c(H+):c(Al3+):c(Mg2+)=l:1:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com