
| A£® | 1£¬3-¶”¶žĻ© | B£® | »·¶”¶žĻ© | C£® | 2-¶”Č² | D£® | 1-¶”Č² |
·ÖĪö 1molijĢž×ī¶ąÄÜÓė2molHCl·¢Éś¼Ó³É·“Ó¦£¬æÉÖŖŗ¬1øöĢ¼Ģ¼Čż¼ü»ņ2øöĢ¼Ģ¼Ė«¼ü£¬Éś³ÉµÄ²śĪļ×ī¶ąÄÜÓė8mol Cl2·¢ÉśČ”“ś·“Ó¦£¬ŌņÉś³ÉĪļÖŠŗ¬8øöH£¬Ō²»±„ŗĶĢžÖŠ8-2=6øöH£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗ1molijĢž×ī¶ąÄÜÓė2molHCl·¢Éś¼Ó³É·“Ó¦£¬æÉÖŖŗ¬1øöĢ¼Ģ¼Čż¼ü»ņ2øöĢ¼Ģ¼Ė«¼ü£¬Éś³ÉµÄ²śĪļ×ī¶ąÄÜÓė8mol Cl2·¢ÉśČ”“ś·“Ó¦£¬ŌņÉś³ÉĪļÖŠŗ¬8øöH£¬Ō²»±„ŗĶĢžÖŠ8-2=6øöH£¬¶ųC3H6²»ŗ¬1øöĢ¼Ģ¼Čż¼ü»ņ2øöĢ¼Ģ¼Ė«¼ü£¬Ö»ÓŠC4H6·ūŗĻ£¬A”¢C”¢DµÄ·Ö×ÓŹ½¾łĪŖC4H6£¬BµÄ·Ö×ÓŹ½ĪŖC4H4£¬
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļ·Ö×ÓŹ½¼ĘĖćµÄČ·¶Ø£¬ĪŖøßĘµæ¼µć£¬°ŃĪռӳɷ“Ó¦”¢Č”“ś·“Ó¦ÖŠ»Æѧ¼ü¼°HŌ×ÓøöŹżµÄ±ä»ÆĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėÓ¦ÓĆÄÜĮ¦µÄ漲飬עŅāĢžÖŠ²»±„ŗĶ¶ČµÄÅŠ¶Ļ£¬ĢāÄæÄŃ¶Č²»“ó£®


 ÄÜæ¼ŹŌĘŚÄ©³å“Ģ¾ķĻµĮŠ“š°ø
ÄÜæ¼ŹŌĘŚÄ©³å“Ģ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ĢśøśĻ”ĮņĖį·“Ó¦£ŗFe+2H+ØTFe2++H2”ü | |
| B£® | Ca£ØHCO3£©2ČÜŅŗŗĶŃĪĖį·“Ó¦£ŗCa£ØHCO3£©2+2H+ØTCa2++2H2O+2CO2”ü | |
| C£® | CaCO3øśĻ”ĮņĖį·“Ó¦£ŗCaCO3+H++SO42-ØTCaSO4+H2O+CO2”ü | |
| D£® | “×ĖįøśĒāŃõ»Æ¼ŲČÜŅŗ·“Ó¦£ŗCH3COOH+OH-ØTCH3COO-+H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ĢĒĄą | ÓĶÖ¬ | µ°°×ÖŹ | ĘäĖū | |
| »ØÉśĆ× | 24% | 39% | 26% | 11% |
| Š”Āó | 76% | 2% | 11% | 11% |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
| ŃōĄė×Ó | H+”¢Na+”¢A13+”¢Ag+”¢Ba2+ |
| ŅõĄė×Ó | OH-”¢C1-”¢CO32-”¢NO3-”¢SO42- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚĶ¬ĪĀĶ¬Ń¹ĻĀ£¬ĻąĶ¬Ģå»żµÄČĪŗĪĘųĢåµ„ÖŹĖłŗ¬µÄ·Ö×ÓŹżÄæŅ»¶ØĻąĶ¬ | |
| B£® | 1L 0.5mol/L FeCl3ČÜŅŗĶźČ«×Ŗ»ÆæɵĆ0.5NAøöFe£ØOH£©3½ŗĮ£ | |
| C£® | ±ź×¼×“æöĻĀ£¬22.4L±½ŗ¬ÓŠµÄ·Ö×ÓŹżĪŖ1NA | |
| D£® | ŌŚ³£ĪĀ³£Ń¹ĻĀ£¬11.2 LµŖĘųĖłŗ¬µÄŌ×ÓŹżÄæĪŖNA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
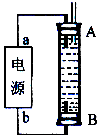 Ģ¼ŗĶĢ¼µÄ»ÆŗĻĪļŌŚÉś²ś”¢Éś»īÖŠµÄÓ¦ÓĆ·Ē³£¹ć·ŗ£¬ŌŚĢį³«½”æµÉś»īŅŃ³É³±Į÷µÄ½ńĢģ£¬”°µĶĢ¼Éś»ī”±²»ŌŁÖ»ŹĒŅ»ÖÖĄķĻė£¬øüŹĒŅ»ÖÖÖµµĆĘŚ“żµÄŠĀµÄÉś»ī·½Ź½£®
Ģ¼ŗĶĢ¼µÄ»ÆŗĻĪļŌŚÉś²ś”¢Éś»īÖŠµÄÓ¦ÓĆ·Ē³£¹ć·ŗ£¬ŌŚĢį³«½”æµÉś»īŅŃ³É³±Į÷µÄ½ńĢģ£¬”°µĶĢ¼Éś»ī”±²»ŌŁÖ»ŹĒŅ»ÖÖĄķĻė£¬øüŹĒŅ»ÖÖÖµµĆĘŚ“żµÄŠĀµÄÉś»ī·½Ź½£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 8 | B£® | 6 | C£® | 4 | D£® | 2 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com