
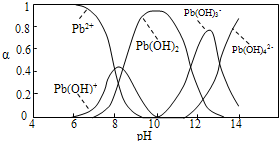
水体中重金属铅的污染问题备受关注。水溶液中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)2、Pb(OH)3-、Pb(OH)42-,各形态的浓度分数α随溶液pH变化的关系如下图所示:

(1)Pb(NO3)2溶液中, ________2(填“>”“=”或“<”);往该溶液中滴入氯化铵溶液后,
________2(填“>”“=”或“<”);往该溶液中滴入氯化铵溶液后, 增加,可能的原因是________________________________。
增加,可能的原因是________________________________。
(2)往Pb(NO3)2溶液中滴入稀NaOH溶液,pH=8时溶液中存在的阳离子(Na+除外)有__________,pH=9时主要反应的离子方程式为_______________________。
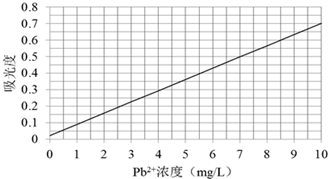
(3)某课题组制备了一种新型脱铅剂,能有效去除水中的痕量铅,实验结果如下表:
|
离子 |
Pb2+ |
Ca2+ |
Fe3+ |
Mn2+ |
Cl- |
|
处理前浓度/(mg·L-1) |
0.100 |
29.8 |
0.120 |
0.087 |
51.9 |
|
处理后浓度/(mg·L-1) |
0.004 |
22.6 |
0.040 |
0.053 |
49.8 |
上表中除Pb2+外,该脱铅剂对其他离子的去除效果最好的是________。
(4)如果 该脱铅剂(用EH表示)脱铅过要发生的反应程中主为:2EH(s)+Pb2+ E2Pb(s)+2H+则脱铅的最合适pH范围为(
)
E2Pb(s)+2H+则脱铅的最合适pH范围为(
)
A.4~5 B.6~7 C.9~10 D.11~12
(1)> Pb2+与Cl-反应,Pb2+浓度减少
(2)Pb2+、Pb(OH)+、H+ Pb(OH)++OH- Pb(OH)2
Pb(OH)2
(3)Fe3+ (4)B
【解析】
试题分析:(1)因为Pb(NO3)2是一种强酸弱碱盐,在水溶液中存在如下水解平衡:2H2O+Pb2+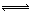 Pb(OH)2+2H+,使c(Pb2+)减小,所以
Pb(OH)2+2H+,使c(Pb2+)减小,所以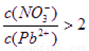 ;滴入氯化铵溶液后,Pb2+与Cl‾反应生成难溶的PbCl2,所以Pb2+浓度减少。
;滴入氯化铵溶液后,Pb2+与Cl‾反应生成难溶的PbCl2,所以Pb2+浓度减少。
(2)pH=8时,曲线上1、2、3表示的物质共存,所以此时溶液中存在的阳离子(Na+除外)有Pb2+、Pb(OH)+和H+。pH=9时,曲线2、3表示的物质共存,由图可知Pb(OH)2的浓度分数比Pb(OH)+的大,所以主要反应是生成Pb(OH)2,离子方程式为:Pb(OH)++OH- Pb(OH)2。
Pb(OH)2。
(3)分析比较表中所给数据可知Cu2+、Mn2+、Cl-的浓度都降低不到原浓度的1/2,而Fe3+却降低为原浓度的1/3,故对Fe3+的去除效果最好。
(4)由所给平衡可知,要使脱铅效果好,铅应以Pb2+的形式存在,pH<7,而c(H+)增大时2EH(s)+Pb2+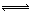 E2Pb(s)+2H+又会向逆反应方向移动,c(H+)不宜过大,所以脱铅最适宜的pH为6~7。
E2Pb(s)+2H+又会向逆反应方向移动,c(H+)不宜过大,所以脱铅最适宜的pH为6~7。
考点:本题考查盐类的水解、离子及其浓度的判断、离子方程式的书写、试剂的选择。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:

| c(NO3-) |
| c(Pb2+) |
| c(NO3-) |
| c(Pb2+) |
| 离子 | Pb2+ | Ca2+ | Fe3+ | Mn2+ | Cl- |
| 处理前浓度/(mg?L-1) | 0.100 | 29.8 | 0.120 | 0.087 | 51.9 |
| 处理后浓度/(mg?L-1) | 0.004 | 22.6 | 0.040 | 0.053 | 49.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 2NH3(g)
2NH3(g)| t/K | 298 | 398 | 498 | … |
| K/(mol?L-1)2 | 4.1×106 | K1 | K2 | … |
 [N2H5?H2O]++H+
[N2H5?H2O]++H+ [N2H5?H2O]++H+
[N2H5?H2O]++H+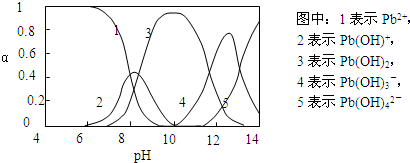
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(Pb2+) |
| c(NO3-) |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源:2011届浙江省温州中学高三三月月考(理综)化学部分 题型:填空题
Ⅰ.氮是地球上含量丰富的一种元 素,氮及其化合物在工农业生产、生活中有着重要作用。请回答:
素,氮及其化合物在工农业生产、生活中有着重要作用。请回答: (1)在一定体积的恒容密闭容器中,进行如下化学反应: N2(g)+3H2(g) 2NH3(g)
(1)在一定体积的恒容密闭容器中,进行如下化学反应: N2(g)+3H2(g) 2NH3(g)
其化学平衡常数K与温度t的关系如下表:
| t/K | 298 | 398 | 498 | … |
| K/(mol·L-1)2 | 4.1×106 | K1 | K2 | … |
 下列问题:
下列问题: 度的排列顺序正确的是 (填序号)。
度的排列顺序正确的是 (填序号)。 |
 。
。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com