
| A. | 铝 | B. | 铁 | C. | 镁 | D. | 锌 |
分析 假设该金属失去两个电子变为带两个单位正电荷的阳离子,根据转移电子守恒计算金属的物质的量,再根据M=$\frac{m}{n}$进行计算其摩尔质量,根据金属的相对原子质量确定该元素.
解答 解:假设该金属失去两个电子变为带两个单位正电荷的阳离子,n(Cl2)=$\frac{7.1g}{71g/mol}$=0.1mol,金属和氯气化合导致金属质量增加,则增加的质量为氯气的质量,根据转移电子守恒得n(金属)×2=0.1mol×2×[0-(-1)],n(金属)=0.1mol,金属的摩尔质量=$\frac{1.8g}{0.1mol}$=18g/mol,摩尔质量在数值上等于其相对原子质量,所以该金属的相对原子质量为18×$\frac{3}{2}$=27,Al的相对原子质量为27,
故选A.
点评 本题考查了物质的量的有关计算,根据转移电子守恒计算金属的物质的量,再根据物质的量、质量、摩尔质量及摩尔质量和相对原子质量关系进行计算,题目难度不大,注意:金属失去两个电子时,钠的相对原子质量、铝的相对原子质量要进行改变,为易错点.


科目:高中化学 来源: 题型:选择题
| A. |  实验室制取乙烯 | B. | 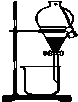 利用酒精萃取碘水中的I2单质 | ||
| C. | 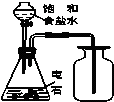 实验室制取乙炔并收集 | D. | 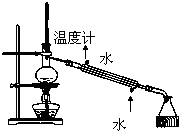 石油的分馏实验 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学研究会造成严重的环境污染,最终人类将毁灭在化学物质中 | |
| B. | 人们可以利用化学变化制造出新的分子和原子 | |
| C. | 门捷列夫提出的原子学说,为现代化学的发展奠定了坚实的基础 | |
| D. | 化学科学在未来还将继续推动材料科学的发展,使各种新功能材料的生产成为可能 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | 加热NaHCO3制CO2 | B. | 用Cu与稀硝酸反应制NO | ||
| C. | 用NH4Cl与浓NaOH溶液反应制NH3 | D. | 用锌与稀硫酸反应制H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该混盐的水溶液呈碱性 | |
| B. | 该混盐溶液中加人BaCl2溶液,可以生成白色沉淀 | |
| C. | 该混盐与稀硫酸反应产生1mol S时转移2NA个电子 | |
| D. | 该混盐中的硫元素的化合价为-2和+4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加水 | B. | CH3COONa固体 | C. | 升温 | D. | NaCl固体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com