
分析 (1)有机化合物对空气的相对密度是3.66,可知有机物相对分子质量为3.66×29=106;
(2)结合1.792L(标准状况)CO2和0.90g H2O,根据C原子、H原子守恒,计算出1.06g有机物A中C元素、H元素的质量,判断有机物A是否含有O元素,据此计算有机物A中各元素的原子个数比,即求出有机物A的实验式;根据有机物A的相对分子质量,结合有机物A的实验式,求出有机物A的分子式;
(3)有机物A不能与溴水发生反应,说明分子中不含不饱和键,且能使酸性高锰酸钾溶液褪色,它发生硝化反应引入1个硝基时,产物只有1种硝基化合物,结合(2)中有机物A的分子式,写出符合条件的有机物A可能的结构简式.
解答 解:(1)有机化合物对空气的相对密度是3.66,可知有机物相对分子质量为3.66×29=106;
答:该有机物的相对分子质量为106;
(2)1.792L(标准状况)CO2的物质的量为$\frac{1.79L}{22.4L/mol}$=0.08mol,所以1.06g有机物A中n(C)=n(CO2)=0.08mol.
0.90g H2O的物质的量为$\frac{0.90g}{18g/mol}$=0.05mol,所以1.06g有机物A中n(H)=2n(H2O)=0.05mol×2=0.1mol.
所以,1.06g有机物A中C元素的质量为0.08mol×12g/mol=0.96g,
1.06g有机物A中H元素的质量为0.1mol×1g/mol=0.1g.
C元素与H元素的总质量为0.96g+0.1g=1.06g,等于有机物A的质量,所以有机物A只含C、H两种元素,为烃.
C原子与H原子个数比为0.08mol:0.1mol=4:5,所以有机物A的实验式为C4H5.
有机物A的相对分子质量为106,
令有机物A的分子式为(C4H5)x,所以(12×4+1×5)x=106,解得x=2,所以有机物A的分子式为C8H10.
答:有机物A的分子式为C8H10;
(3)有机物A的分子式为C8H10,不饱和度为$\frac{8×2+2-10}{2}$=4,且有机物A不能与溴水发生反应,说明分子中不含不饱和键,能使酸性高锰酸钾溶液褪色,分子组成符合苯的同系物通式,应为苯的同系物,侧链为一个乙基或两个甲基.
若侧链为一个乙基,它发生硝化反应引入1个硝基时,产物有邻、间、对3种硝基化合物;
若侧链为两个甲基,则对应有机物A可能为邻二甲苯、间二甲苯、对二甲苯.当为邻二甲苯,它发生硝化反应引入1个硝基时,产物有2种;当为间二甲苯,它发生硝化反应引入1个硝基时,产物有3种;当为对二甲苯,它发生硝化反应引入1个硝基时,产物有1种.所以有机物A为对二甲苯,结构简式为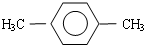
答:有机物A的结构简式为 .
.
点评 本题考查有机物分子式的确定、限制条件同分异构体的书写,为高频考点,侧重于学生的分析、计算能力的考查,题目中等,注意把握题中信息.判断有机物中是否含有氧元素容易忽略.


科目:高中化学 来源: 题型:解答题
| 实验步骤 | 解释或实验结论 |
| (1)取9.0g有机物A加热使其气化,测得其密度是相同条件下H2的45倍 | (1)由此可知A的相对分子质量为90. |
| (2)将9.0gA在足量O2中充分燃烧,其产物依次缓缓通过浓硫酸、碱石灰,两者分别增重5.4g和13.2g. | (2)由此可知A的分子式为C3H6O3. |
| (3)另取A9.0g,跟足量的NaHCO3粉末反应,生成CO2气体2.24L;9.0gA若与足量金属钠反应生成H2也是2.24L(气体体积皆为标准状况下测得). | (3)由此可知A中含有官能团有.(填结构简式)-COOH、-OH |
(4)A的核磁共振氢谱如下图: | (4)由此可知A中含有4种不同性质的氢原子 (5)综上,A的结构简式为  . . |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
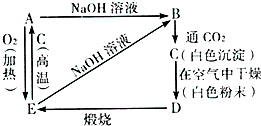 根据如图反应及其变化,回答有关问题.
根据如图反应及其变化,回答有关问题.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH≡CH | B. | CH≡C-CH3 | C. | CH2═CH2 | D. | CH2═C(CH3)CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 不能通过自身反应形成高分子化合物 | |
| B. | 不能使酸性KMnO4溶液褪色 | |
| C. | 能发生加成、取代、消去、氧化反应 | |
| D. | 1 mol该物质最多可与4 mol NaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 取一张用饱和NaCl溶液浸湿的pH试纸,两根铅笔芯作电极,接通直流电源,一段时间后,发现 a电极与试纸接触处出现一个双色同心圆,内圈为白色,外圈呈浅红色.则下列说法正确的是( )
取一张用饱和NaCl溶液浸湿的pH试纸,两根铅笔芯作电极,接通直流电源,一段时间后,发现 a电极与试纸接触处出现一个双色同心圆,内圈为白色,外圈呈浅红色.则下列说法正确的是( )| A. | 电解过程中水是还原剂 | B. | 电解过程中Cl-被还原 | ||
| C. | a 电极与电源负极相连 | D. | b电极附近溶液的碱性增强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com