
| ||
| ||
|
|


科目:高中化学 来源: 题型:
| A、盐酸溶液与氢氧化钠溶液反应:H++OH-=H2O |
| B、新制氯水与溴化钾溶液反应:Cl2+2Br一=2Cl一+Br2 |
| C、碳酸钙与稀盐酸反应:CaCO3+2H+=Ca2++H2O+CO2↑ |
| D、铝与烧碱溶液反应:Al+2H2O+OH-=AlO2-+2H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
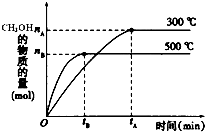 一定条件下,在体积为3L的密闭容器中反应CO(g)+2H2(g)?CH3OH(g)达到化学平衡状态.
一定条件下,在体积为3L的密闭容器中反应CO(g)+2H2(g)?CH3OH(g)达到化学平衡状态.| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)A、B、C均为短周期元素,其中A元素的单质是自然界最轻的气体,B元素原子的次外层电子数为最外层电子数和最内层电子数之和,C元素与B元素位于同一主族,且可形成BC2型化合物.
(1)A、B、C均为短周期元素,其中A元素的单质是自然界最轻的气体,B元素原子的次外层电子数为最外层电子数和最内层电子数之和,C元素与B元素位于同一主族,且可形成BC2型化合物.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、稀盐酸与氢氧化钠反应:NaOH+H+=Na++H2O |
| B、铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
| C、碳酸钙与盐酸反应:CaCO3+2H+=Ca2++H2O+CO2↑ |
| D、氯水滴入氯化亚铁溶液中:Fe2++Cl2=Fe3++2Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com