
| A���Ȼ�粒�������ʯ�ҷ�Ӧ�Ʊ�������NH4++OH-=NH3��+H2O | ||||
B����ʯī�����缫��ⱥ��ʳ��ˮ��Cl-+Na+
| ||||
| C����������Һ�������ˮ��Ӧ�����ӷ���ʽ��Al3++3NH3?H2O=Al��OH��3��+3NH4+ | ||||
| D����ϡ����ϴ���Թ��ڱڵ�������Ag+2H++NO3-=Ag++NO��+H2O |
| ||
| ||


 ��ͼͼ�麮����ҵ������ҵ���ִ�ѧ������ϵ�д�
��ͼͼ�麮����ҵ������ҵ���ִ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʱ��/min | 1 | 2 | 3 | 4 | 5 |
| ���/mL | 50 | 120 | 232 | 290 | 310 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ij���ʵ���ҺpH��7���������һ�������ǿ�������� | ||
| B��pH=4.5�ķ���֭��c��H+����pH=6.5��ţ����c��H+����102�� | ||
| C������ʱ��ij��Һ����ˮ���������c��H+����c��OH-���ij˻�Ϊ1��10-24������Һ��һ�����Դ�������K+��Na+��AlO2-��SO42- | ||
D������ʱ��0.1mol/L HA��Һ��pH��1��0.1mol/L BOH��Һ��
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��c ��Na+��=c ��HCO3-��+c ��CO32-��+c ��H2CO3�� |
| B��c ��Na+��+c ��H+��=c ��HCO3-��+c ��CO32-��+c ��OH-�� |
| C��HCO3- �ĵ���̶ȴ���HCO3-��ˮ��̶� |
| D�����ڵĵ���ƽ���У�HCO3-?H++CO32-��H2O?H++OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������£�11.2L��CHCl3���з�����Ϊ0.5NA�� |
| B�������£�14g��ϩ�ͱ�ϩ�Ļ��������ԭ����Ϊ3NA�� |
| C��1mol����ϩ�к��е�̼̼˫����Ϊ4NA�� |
| D��0.1mol CnH2n+2�к��е�̼̼������Ϊ0.1nNA�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Ksp��AB2��С��Ksp��CD������AB2���ܽ��С��CD���ܽ�� |
| B����AgCl�ij����ܽ�ƽ����ϵ�У���������ˮ��AgCl��Ksp���� |
| C����AgI�ij����ܽ�ƽ����ϵ�У�����K2S���壬AgI������ת��ΪAg2S���� |
| D����CaCO3�ij����ܽ�ƽ����ϵ�У�ͨ��CO2���壬�ܽ�ƽ�ⲻ�ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.1mol/L NaOH |
| B������ˮ |
| C��0.1mol/LBa��OH��2 |
| D��0.1mol/LCaCl2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
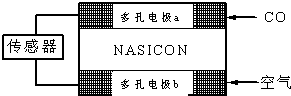 ��Դ����������ͷ�չ����Ҫ֧�����о���ѧ��Ӧ�����е������仯����Դ��ȱ�Ľ��������Ҫ���������壮��֪�����Ȼ�ѧ����ʽ
��Դ����������ͷ�չ����Ҫ֧�����о���ѧ��Ӧ�����е������仯����Դ��ȱ�Ľ��������Ҫ���������壮��֪�����Ȼ�ѧ����ʽ| 1 |
| 2 |
| 1 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��֪2NO2��g���TN2O4��g����H=-52.7kJ?mol-1��������NO2Ϊ����ɫ���壬N2O4Ϊ��ɫ���壮ij����С��Ϊ��̽���¶Ⱥ�ѹǿ�Ի�ѧƽ���Ӱ�죬�����£�1����2������ʵ�飺
��֪2NO2��g���TN2O4��g����H=-52.7kJ?mol-1��������NO2Ϊ����ɫ���壬N2O4Ϊ��ɫ���壮ij����С��Ϊ��̽���¶Ⱥ�ѹǿ�Ի�ѧƽ���Ӱ�죬�����£�1����2������ʵ�飺�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com