
医学上常用酸性高锰酸钾溶液和草酸溶液的反应用于测定血钙的含
量。回答下列问题:
 ___H+ + ___MnO4- + ___H2C2O4 → ___CO2↑+___Mn2+ +____ ( )
___H+ + ___MnO4- + ___H2C2O4 → ___CO2↑+___Mn2+ +____ ( )
 (1).配平以上离子方程式,并在 ( ) 中填上所需的微粒。
(1).配平以上离子方程式,并在 ( ) 中填上所需的微粒。
 (2).该反应中的还原剂是
(2).该反应中的还原剂是
 (3).反应转移了0.4mol电子,则消耗KMnO4的物质的量为 mol。
(3).反应转移了0.4mol电子,则消耗KMnO4的物质的量为 mol。
 (4).测定血钙的含量的方法是:取2mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
(4).测定血钙的含量的方法是:取2mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
 ①稀硫酸溶解CaC2O4沉淀的化学方程式是
①稀硫酸溶解CaC2O4沉淀的化学方程式是
 ②溶解沉淀时 (能或不能)用浓盐酸,原因是
②溶解沉淀时 (能或不能)用浓盐酸,原因是
 ③若消耗了1.0×10-4mol/L的KMnO4溶液20.00mL,则100mL该血液中含钙 g
③若消耗了1.0×10-4mol/L的KMnO4溶液20.00mL,则100mL该血液中含钙 g
 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
下列制备金属单质的方法或原理正确的是 ( )
A.在高温条件下,用H2还原MgO制备单质Mg
B.在通电条件下,电解熔融Al2O3制备单质Al
C.在通电条件下,电解饱和食盐水制备单质Na
D.加强热,使CuO在高温条件下分解制备单质Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
硫代硫酸钠在工业生产中用途非常广泛。
(1) 溶液是定量实验中的常用试剂。实验室需用480mL一定浓度的
溶液是定量实验中的常用试剂。实验室需用480mL一定浓度的 溶液,配制该溶液所需玻璃仪器除烧杯、量筒、玻璃棒外,还需__________________。
溶液,配制该溶液所需玻璃仪器除烧杯、量筒、玻璃棒外,还需__________________。
(2) 可以用作氰化物的解毒剂,工业上常用硫化碱法制备
可以用作氰化物的解毒剂,工业上常用硫化碱法制备 ,反应原理为:
,反应原理为:

某研究小组在实验室模拟该工业原理制备 ,部分实验装置如下:
,部分实验装置如下:

①装置B的作用是检验装置A中 的吸收效率,则B中试剂是________________,
的吸收效率,则B中试剂是________________,
表明 吸收效率低的实验现象是B中溶液________________________。
吸收效率低的实验现象是B中溶液________________________。
②实验结束时,测得装置C中的溶液含有两种溶质,其中一种为NaOH,则实验过程中该装置内发生反应的化学方程式是_________________________;若两种溶质的物质的量相等,则该溶液所含离子浓度的大小顺序为__________________________________。
③假设本实验所用的 含少量NaC1、NaOH,设计实验方案进行检验。请完成下表。
含少量NaC1、NaOH,设计实验方案进行检验。请完成下表。
已知:室温时CaCO3饱和溶液的pH=10.2。
限选试剂及仪器:稀硝酸、AgNO3溶液、CaC12溶液、酚酞溶液、蒸馏水、pH计,烧杯、试管、胶头滴管。

查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验均发生了化学反应:①将铁钉放入CuSO4溶液中;②向FeSO4溶液中
滴加浓HNO3;③将铜丝放入FeCl3溶液中。下列判断中,正确的是
A.上述实验证明了氧化性:Fe3+>Fe2+>Cu2+
B.上述实验证明了Fe3+既有氧化性又有还原性
C.实验①、③中的化学反应都是置换反应
D.向三个实验后的溶液中加入足量NaOH溶液,最终都有Fe(OH)3生成
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,将CO和O2的混合气体26g充入一体积固定不变的密闭容器(容器内有足量的Na2O2固体),此时容器的压强为p1,用电火花不间断的点燃,使其充分反应,恢复至原温,结果固体增重14g,此时容器的压强为p2,则p1/p2为
A.9:4 B.7:3 C.7:6 D.6:7
查看答案和解析>>
科目:高中化学 来源: 题型:
已知空气—锌电池的电极反应为:锌片:Zn+2OH--2e- = ZnO+H2O;
碳棒:1/2 O2+H2O+2e- = 2OH-,据此判断,锌片是
A.正极,并被还原 B.正极,并被氧化 C.负极,并被还原 D.负极,并被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【化学——选修3物质结构与性质】(15分)
A、B、C、D、E、F为周期表中前四周期的六种元素,它们的原子序数依次增大,且均不同族。A、B、C三种元素的基态原子具有相同的能层和能级,且第一电离能I1(A)<I1(C)<I1(B),BC2+与AC2互为等电子体;D、E为同周期相邻元素;F元素位于周期表中1~18列中的第11列。请回答下列问题(答题时请用相应的元素符号表示相应元素):
⑴A元素的价层电子排布图为 ;BC2+的电子式为 ; 基态F原子的核外电子排布简式 。
⑵E元素的电离能情况如图1所示。E元素在周期表中位于 ; D元素单质形成的
晶体晶胞类型属于 堆积。
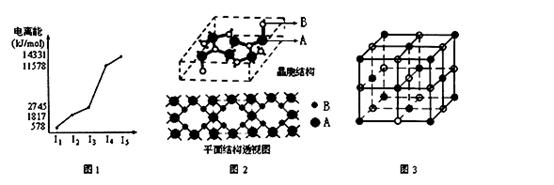
⑶A、B两元素所形成的化合物甲是首屈一指的超硬新材料,其晶胞结构如图2所示,由此可知,化合物
甲的晶体类型为 ,其硬度超过金刚石的原因是 。化合物甲的晶体中B原子的杂化方式为 。
⑷D、C两元素可形成的化合物乙。
①现证实化合物乙的晶体结构如图3所示,晶胞中D离子的配位数为 ;
②设D离子半径分别为a,C离子半径分别为b,则其晶体的空间利用率为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com