
五种短周期元素A、B、C、D、E的原子序数依
次增大,A和C同族,B和D 同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共
价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物在水中呈中性。回答下列问题:
(1)五种元素中,原子半径最大的是 ,非金属性最强的是 (填元素符号);
(2)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是 (用化学式表示);
(3)A和E形成的化合物与A和B形成的化合物反应,产物的化学式为 ,其中存在的化学键类型为 ;
(4)D最高价氧化物的水化物的化学式为 ;
(5)单质D在充足的单质E中燃烧,反应的化学方程式为 ;D在不充足的E中燃烧,生成的主要产物的化学式为 ;
(6)单质E与水反应的离子方程式为 。
科目:高中化学 来源: 题型:
一种新型熔融盐燃料电池具有高发电效率.现用Li2CO3和Na2CO3的熔融盐混合物作电解质,一极通CO
气体,另一极通O2和CO2混合气体,其总反应为:2CO+O2===2CO2.则下列说法中正确的是 ( )
A.通CO的一极是电池的正极
B.负极发生的电极反应是:O2+2CO2+4e-===2CO
C.负极发生的电极反应是:CO+CO -2e-===2CO2
-2e-===2CO2
D.正极发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
近年来,我国在超导体材料研究方面居于世界领先地位,铊(Tl)是超导体的组成成分之一,铊位于第六
周期第ⅢA族。下列对铊的可能性质的推导正确的是( )
①是易导电的银白色金属 ②Tl(OH)3是两性氢氧化物
③Tl3+氧化能力比Al3+强 ④单质能与稀硝酸反应
④单质能与稀硝酸反应 生成硝酸盐
生成硝酸盐
A.①④ B.②③
C.只有① D.只有④
查看答案和解析>>
科目:高中化学 来源: 题型:
今年是门捷列夫诞辰180周年。下列事实不能用元素周期律解释的只有
A.碱性:KOH>NaOH  B.相对分子质量:Ar>K
B.相对分子质量:Ar>K
C.酸性:HClO4>H2SO4 D.元素的金属性:Mg>Al
查看答案和解析>>
科目:高中化学 来源: 题型:
“玉兔”号月球车用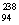 Pu作为热源材料。下列关于
Pu作为热源材料。下列关于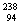 Pu的说法正确的是
Pu的说法正确的是
A.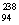 Pu与
Pu与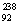 U互为同位素 B.
U互为同位素 B.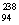 Pu与
Pu与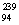 Pu互为同素异形体
Pu互为同素异形体
C.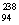 Pu与
Pu与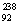 U具有完全相同的化学性质 D.
U具有完全相同的化学性质 D.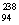 Pu与
Pu与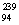 Pu具有相同的最外层电子数
Pu具有相同的最外层电子数
查看答案和解析>>
科目:高中化学 来源: 题型:
原子的核电荷数小于18的某元素X,其原子的电子层数为n,最外层电子数为2n+1,原子核内质子数为2n2-1。下列有关X的说法中不正确的是 ( )
A.X能形成化学式为X(OH)3的碱
B.X能与某些金属元素形成化合物
C.X原子的最外层电子数和核电荷数肯定为奇数
D.X可能形成化学式为KXO3的盐
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E分别代表5种微粒,每种微粒中都含有18个电子,其中A和C都是由单原子形成的阴离子,B、D和E都是分子;又知在水溶液中A跟B反应可生成C和D;E具有强氧化性且为双原子分子。请回答:
(1)用化学符号表示上述5种微粒:
A__________,B__________,C__________,D__________,E__________。
(2)在水溶液中A跟B反应的离子方程式是:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
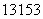 I是常规核裂变产物之一,可以通过测定大气或水中
I是常规核裂变产物之一,可以通过测定大气或水中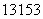 I的含量变化来监测核电站是否
I的含量变化来监测核电站是否
发生放射性物质泄漏。下列有关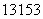 I的叙述中错误的是 ( )
I的叙述中错误的是 ( )
A. 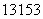 I的化学性质与
I的化学性质与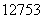 I相同
I相同
B. 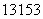 I的原子序数为53
I的原子序数为53
C. 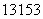 I的原子核外电子数为78
I的原子核外电子数为78
D. 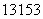 I的原子核内中子数多于质子数
I的原子核内中子数多于质子数
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于碱金属的电子结构和性质的叙述中不正确的是( )
A.碱金属原子最外层都只有一个电子,在化学反应中容易失去
B.都是强还原剂
C.都能在O2中燃烧生成过氧化物
D.都能与水反应生成碱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com