
ĻĀĮŠø÷×éĪļÖŹ²»ŹōÓŚĶ¬·ÖŅģ¹¹ĢåµÄŹĒ£Ø£©
A£® 2£¬2﹣¶ž¼×»ł±ū“¼ŗĶ2﹣¼×»ł¶”“¼
B£® ĮŚĀČ¼×±½ŗĶ¶ŌĀČ¼×±½
C£® 2﹣¼×»ł¶”ĶéŗĶĪģĶé
D£® ŅŅ“¼ŗĶŅŅĆŃ
æ¼µć£ŗ Ķ¬·ÖŅģ¹¹ĻÖĻóŗĶĶ¬·ÖŅģ¹¹Ģ壮
×ØĢā£ŗ Ķ¬·ÖŅģ¹¹ĢåµÄĄąŠĶ¼°ĘäÅŠ¶Ø£®
·ÖĪö£ŗ ·Ö×ÓŹ½ĻąĶ¬£¬½į¹¹²»Ķ¬µÄ»ÆŗĻĪļ»„ĪŖĶ¬·ÖŅģ¹¹Ģ壮¾Ż“ĖÅŠ¶Ļ£®
½ā“š£ŗ ½ā£ŗA£®2£¬2﹣¶ž¼×»ł±ū“¼ŗĶ2﹣¼×»ł¶”“¼·Ö×ÓŹ½ĻąĶ¬£¬¶¼ŗ¬ÓŠŅ»øöōĒ»ł£¬µ«Ö÷Į“Ģ¼Ō×ÓŹż²»Ķ¬£¬»„ĪŖĶ¬·ÖŅģ¹¹Ģ壬¹Ź AÕżČ·£»
AÕżČ·£»
B£®ĮŚĀČ¼×±½ŗĶ¶ŌĀČ¼×±½£¬·Ö×ÓŹ½ĻąĶ¬£¬ĀČŌ×ÓĪ»ÖĆ²»Ķ¬£¬ŹōÓŚ¹ŁÄÜĶÅĪ»ÖĆŅģ¹¹£¬¹ŹBÕżČ·£»
C£®2﹣¼×»ł¶”ĶéŗĶĪģĶ飬·Ö×ÓŹ½ĻąĶ¬£¬Ö÷Į“Ģ¼Ō×ÓŹż²»Ķ¬£¬Ōņ½į¹¹²»Ķ¬£¬»„ĪŖĶ¬·ÖŅģ¹¹Ģ壬¹ŹCÕżČ·£»
D£®ŅŅ“¼ŗĶŅŅĆŃ·Ö×ÓÖŠĢ¼Ō×ÓŹżÄæ²»Ķ¬£¬Ōņ·Ö×ÓŹ½²»Ķ¬£¬²»ŹĒĶ¬·ÖŅģ¹¹Ģ壬¹ŹD“ķĪó£®
¹ŹŃ”D£®
µćĘĄ£ŗ ±¾Ģāæ¼²éĶ¬·ÖŅģ¹¹ĢåµÄøÅÄī£¬ĢāÄæÄŃ¶Č²»“󣬹Ų¼üŹĒøł¾ŻĆū³ĘŠ“³ö·Ö×ÓŹ½½ųŠŠÅŠ¶Ļ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ijČÜŅŗÖŠ“ęŌŚĪåÖÖĄė×Ó: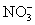 ”¢
”¢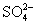 ”¢Fe3+”¢H+ŗĶŅ»ÖÖĪ“ÖŖĄė×Ó(OH-ŗöĀŌ²»¼Ę),ĖüĆĒĪļÖŹµÄĮæÅضČÖ®±ČĪŖ2”Ć3”Ć1”Ć3”Ć1,ŌņĪ“ÖŖĄė×ÓæÉÄÜĪŖ””(””””)
”¢Fe3+”¢H+ŗĶŅ»ÖÖĪ“ÖŖĄė×Ó(OH-ŗöĀŌ²»¼Ę),ĖüĆĒĪļÖŹµÄĮæÅضČÖ®±ČĪŖ2”Ć3”Ć1”Ć3”Ć1,ŌņĪ“ÖŖĄė×ÓæÉÄÜĪŖ””(””””)
A.Fe2+ B.Ba2+ C.Cl- D.Mg2+
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ČēĶ¼ĖłŹ¾£¬ĻĀĮŠŹµŃé²Ł×÷Óė·½·ØÕżČ·µÄŹĒ£Ø””””£©
| ”” | A£® |
| B£® |
|
| ”” | C£® |
| D£® |
|
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓŠK2SO4ŗĶAl2£ØSO4£©3µÄ»ģŗĻČÜŅŗ£¬ŅŃÖŖĘäÖŠAl3+µÄĪļÖŹµÄĮæÅضČĪŖ0.4mol/L£¬SO42﹣µÄĪļÖŹµÄĮæÅضČĪŖ0.7mol/L£¬Ōņ“ĖČÜŅŗÖŠK+µÄĪļÖŹµÄĮæÅضČĪŖ£Ø””””£©
| ”” | A£® | 0.1mol/L | B£® | 0.15mol/L | C£® | 0.2mol/L | D£® | 0.25mol/L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
°Ń200mLÓŠBaCl2ŗĶKClµÄ»ģŗĻČÜŅŗ·Ö³É2µČ·Ż£¬Č”Ņ»·Ż¼ÓČėŗ¬ A molĮņĖį¼ŲµÄČÜŅŗ£¬Ē”ŗĆŹ¹±µĄė×ÓĶźČ«³Įµķ£»ĮķČ”Ņ»·Ż¼ÓČėŗ¬ B molĻõĖįŅųµÄČÜŅŗ£¬Ē”ŗĆŹ¹ĀČĄė×ÓĶźČ«³Įµķ£®Ōņ£ŗĆæ·ŻČÜŅŗÖŠ£ŗn£ØBa2+£©=””””mol£¬n£ØCl﹣£©=””””mol£»
200mLŌ»ģŗĻČÜŅŗÖŠ£ŗc£ØCl﹣£©=””””mol•L﹣1£¬c£ØK+£©=””””mol•L﹣1£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚ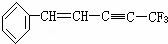 ·Ö×ÓÖŠĪ»ÓŚĶ¬Ņ»Ę½ĆęÉĻµÄŌ×ÓŹż×ī¶ąæÉÄÜŹĒ£Ø£©
·Ö×ÓÖŠĪ»ÓŚĶ¬Ņ»Ę½ĆęÉĻµÄŌ×ÓŹż×ī¶ąæÉÄÜŹĒ£Ø£©
A£® 17øö B£® 18øö C£® 19øö D£® 20øö
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŹŻČā¾«ŌŚŅ½Ń§ÉĻ³ĘĪŖ”°ŃĪĖįæĖĀ×ĢŲĀŽ”±£®ĖüŹĒ°×É«»ņĄą°×É«µÄ½į¾§·ŪÄ©£¬ĪŽ³ō”¢Ī¶æą£¬ČŪµć161”ę£¬ČÜÓŚĖ®”¢ŅŅ“¼£¬Ī¢ČÜÓŚ±ūĶŖ£¬²»ČÜÓŚŅŅĆŃ£¬Źō¦Ā﹣ŠĖ·Ü¼ĮĄą¼¤ĖŲ£®ŹĒŃĻÖŲĪ£ŗ¦ŠóÄĮŅµ½”æµ·¢Õ¹ŗĶŠó²śĘ·°²Č«µÄ¶¾Ę·£®Ęä»Æѧ³É·ÖČēĶ¼£¬ĻĀĮŠÓŠ¹ŲŃĪĖįæĖĀ×ĢŲĀŽĖµ·Ø“ķĪóµÄŹĒ£Ø£©

A£® ·Ö×ÓŹ½ĪŖC12H1 8Cl2N2O
8Cl2N2O
B£® ·Ö×Ó½į¹¹ÖŠÓŠ6øö±„ŗĶĢ¼Ō×Ó
C£® ·Ö×ÓÖŠŗ¬Ńõ¹ŁÄÜĶŵÄĆū³ĘŹĒōĒ»ł
D£® ÄÜČÜÓŚĖłÓŠÓŠ»śČܼĮ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠµ„ÖŹ»ņ»ÆŗĻĪļŠŌÖŹµÄĆčŹöÕżČ·µÄŹĒ( )
A£®NaHSO4Ė®ČÜŅŗĻŌÖŠŠŌ
B£®SiO2ÓėĖį”¢¼ī¾ł²»·“Ó¦
C£®NO2ČÜÓŚĖ®Ź±·¢ÉśŃõ»Æ»¹Ō·“Ó¦
D£®FeŌŚ×ćĮæCl2ÖŠČ¼ÉÕÉś³ÉŗĶFeCl2ŗĶFeCl3
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĮŖ°±(N2H4)¼°ĘäŃÜÉśĪļŹĒŅ»ĄąÖŲŅŖµÄ»š¼żČ¼ĮĻ£¬N2H4ÓėN2O4·“Ó¦Äܷųö“óĮæµÄČČ”£
(1)ŅŃÖŖ£ŗ2NO2(g)====N2O4(g) ¦¤H£½-57.20 kJ”¤mol-1”£Ņ»¶ØĪĀ¶ČĻĀ£¬ŌŚĆܱÕČŻĘ÷ÖŠ·“Ó¦2NO2(g)  N2O4(g)“ļµ½Ę½ŗā”£
N2O4(g)“ļµ½Ę½ŗā”£
ĘäĖūĢõ¼ž²»±äŹ±£¬ĻĀĮŠ“ėŹ©ÄÜĢįøßNO2×Ŗ»ÆĀŹµÄŹĒ______________(Ģī×ÖÄø)”£
A.¼õŠ”NO2µÄÅضČ
B.½µµĶĪĀ¶Č
C.Ōö¼ÓNO2µÄÅضČ
D.ÉżøßĪĀ¶Č
(2)25 ”ꏱ£¬1.00 g N2H4(l)Óė×ćĮæN2O4(l)ĶźČ«·“Ӧɜ³ÉN2(g)ŗĶH2O(l)£¬·Å³ö19.14 kJµÄČČĮ攣Ōņ·“Ó¦2N2H4(l)+N2O4(l)====3N2(g)+4H2O(l)µÄ¦¤H£½____________________kJ”¤mol-1”£
(3)17 ”ę”¢1.01”Į105 Pa£¬ĆܱÕČŻĘ÷ÖŠN2O4ŗĶNO2µÄ»ģŗĻĘųĢå“ļµ½Ę½ŗāŹ±£¬c(NO2)£½0.030 0 mol”¤L-1”¢c(N2O4)£½0.012 0 mol”¤L-1”£¼ĘĖć·“Ó¦2NO2(g)  N2O4(g)µÄĘ½ŗā³£ŹżK”£
N2O4(g)µÄĘ½ŗā³£ŹżK”£
(4)ĻÖÓĆŅ»¶ØĮæµÄCuÓė×ćĮæµÄÅØHNO3·“Ó¦£¬ÖʵĆ1.00 LŅŃ“ļµ½Ę½ŗāµÄN2O4ŗĶNO2µÄ»ģŗĻĘųĢå(17 ”ę”¢1.01”Į105 Pa)£¬ĄķĀŪÉĻÖĮÉŁŠčĻūŗÄCu¶ąÉŁæĖ£æ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com