
大气中可吸入颗粒物PM2.5主要来源为燃煤、机动车尾气等。
(1)若取某PM2.5样本,用蒸馏水处理,测得溶液中含有的离子有:K+、Na+、NH4+、SO42-、NO3-、Cl-,则该溶液为 (填“酸性”或“碱性”)溶液,其原因用离子方程式解释是: 。
(2)“洗涤”燃煤烟气可减轻PM2.5中SO2的危害,下列可适用于吸收SO2的试剂有
A.CaCl2溶液 B.氨水 C.Ca(OH)2悬浊液 D.浓H2SO4
(3)煤烟气中的氮氧化物可用CH4催化还原成无害物质。若常温下,1molNO2与CH4反应,放出477.5kJ热量,该反应的热化学方程式是 。
(4)安装汽车尾气催化转化器也可减轻PM2.5的危害,其反应是:
2NO(g) + 2CO(g)  2CO2(g)+ N2(g);△H<0。
2CO2(g)+ N2(g);△H<0。
①该反应平衡常数表达式K= ;温度升高K值 (填“增大”或“减小” )
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是 。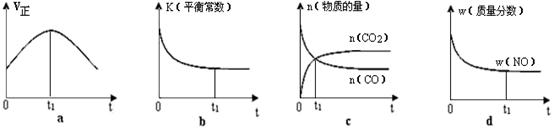
(5)使用锂离子电池为动力汽车,可减少有害气体的排放。锰酸锂离子蓄电池的反应式为: Li1-xMnO4 + LixC
Li1-xMnO4 + LixC LiMnO4 + C
LiMnO4 + C
下列有关说法正确的是
A.充电时电池内部Li+向正极移动
B.放电过程中,电能转化为化学能
C.放电时电池的正极反应式为:Li1-xMnO4+xe—+xLi+=LiMnO4
D.充电时电池的正极应与外接电源的负极相连
(1)酸性,NH4++H2O NH3·H2O+H+ (2)B C
NH3·H2O+H+ (2)B C
(3)2NO2(g)+CH4(g)=N2(g)+CO2(g)+2H2O(l);△H=" -955kJ/mol"
(4)①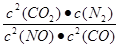 ;减小 ② D (5)C
;减小 ② D (5)C
解析试题分析:(1)取某PM2.5样本,用蒸馏水处理,测得溶液中含有的离子有:K+、Na+、NH4+、SO42-、NO3-、Cl-,则由于K+、Na+、SO42-、NO3-、Cl-都是强酸或强碱的离子,而NH4+则是弱碱根离子。含有强酸弱碱盐。弱碱根离子水解消耗水电离产生的OH-,使溶液显酸性。其原因用离子方程式解释是为NH4++H2O NH3·H2O+H+。(2)SO2溶于水发生反应:SO2+H2O=H2SO3.H2SO3是酸,电离产生大量的H+而使溶液显酸性。所以应该用碱性物质氨水、Ca(OH)2悬浊液来吸收。因此选项为B、C。(3)根据题意可得该反应的热化学方程式为2NO2(g)+CH4(g)=N2(g)+CO2(g)+2H2O(l);△H= -955kJ/mol。(4)①根据化学平衡常数的含义可得该反应平衡常数表达式K=
NH3·H2O+H+。(2)SO2溶于水发生反应:SO2+H2O=H2SO3.H2SO3是酸,电离产生大量的H+而使溶液显酸性。所以应该用碱性物质氨水、Ca(OH)2悬浊液来吸收。因此选项为B、C。(3)根据题意可得该反应的热化学方程式为2NO2(g)+CH4(g)=N2(g)+CO2(g)+2H2O(l);△H= -955kJ/mol。(4)①根据化学平衡常数的含义可得该反应平衡常数表达式K=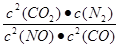 。由于该反应的正反应为放热反应。根据平衡移动原理:温度升高,化学平衡向吸热反应方向移动,对该反应来说升高温度,化学平衡向逆向移动,所以K值减小。②若该反应在绝热、恒容的密闭体系中进行。a.在反应刚开始时,由于温度变化不明显。主要是浓度的影响。随着反应的进行,气体的温度逐渐升高,影响化学反应速率的主要因素是温度。所以化学反应速率逐渐加快;当反应进行到一定程度后,反应物的浓度是影响化学反应速率的主要因素。由于反应物不断消耗,浓度减小,所以速率又逐渐减小。跟反应是否达到平衡无关。错误。B.在刚开始时反应刚发生,还未达到平衡,所以不能说平衡常数。当反应达到平衡后,升高温度,化学平衡逆向移动,K减小。但是从图像并未看出这一点来。错误。C若t点反应达到平衡,则各种反应混合物的浓度不应该发生变化。但是图像显示的c(CO)及c(CO2)任然在变化,因此反应为达到平衡。错误。d.在反应开始时,由于反应是从正反应方向开始,NO的质量最大,质量分数也最大,随着反应的减小,NO不断消耗。其质量分数也逐渐减小,当反应达到平衡后各种物质的质量、物质的量不变,所以其质量分数也不变。正确。(5)A.根据同种电荷相互排斥,异种电荷相互吸引的原则,充电时电池内部Li+向负极移动。错误。B.放电过程中,化学能转化为电能。错误。C.放电时电池正极发生还原反应。正极反应式为:Li1-xMnO4+xe—+xLi+=LiMnO4。正确。D.充电时电池的正极应与外接电源的正极相连。错误。
。由于该反应的正反应为放热反应。根据平衡移动原理:温度升高,化学平衡向吸热反应方向移动,对该反应来说升高温度,化学平衡向逆向移动,所以K值减小。②若该反应在绝热、恒容的密闭体系中进行。a.在反应刚开始时,由于温度变化不明显。主要是浓度的影响。随着反应的进行,气体的温度逐渐升高,影响化学反应速率的主要因素是温度。所以化学反应速率逐渐加快;当反应进行到一定程度后,反应物的浓度是影响化学反应速率的主要因素。由于反应物不断消耗,浓度减小,所以速率又逐渐减小。跟反应是否达到平衡无关。错误。B.在刚开始时反应刚发生,还未达到平衡,所以不能说平衡常数。当反应达到平衡后,升高温度,化学平衡逆向移动,K减小。但是从图像并未看出这一点来。错误。C若t点反应达到平衡,则各种反应混合物的浓度不应该发生变化。但是图像显示的c(CO)及c(CO2)任然在变化,因此反应为达到平衡。错误。d.在反应开始时,由于反应是从正反应方向开始,NO的质量最大,质量分数也最大,随着反应的减小,NO不断消耗。其质量分数也逐渐减小,当反应达到平衡后各种物质的质量、物质的量不变,所以其质量分数也不变。正确。(5)A.根据同种电荷相互排斥,异种电荷相互吸引的原则,充电时电池内部Li+向负极移动。错误。B.放电过程中,化学能转化为电能。错误。C.放电时电池正极发生还原反应。正极反应式为:Li1-xMnO4+xe—+xLi+=LiMnO4。正确。D.充电时电池的正极应与外接电源的正极相连。错误。
考点:考查PM2.5样本的水溶液的酸碱性及原因、热化学方程式的书写、温度对化学平衡常数的影响、化学平衡常数的表达式、化学平衡状态的判断、电化学反应原理的知识。


科目:高中化学 来源: 题型:填空题
(14分)加大对煤燃烧产生的废气、废渣的处理已刻不容缓。
(1) 对燃煤的废气进行脱硝处理时,可利用甲烷催化还原氮氧化物,如:
CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g);ΔH=a kJ·mol-1
CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g);ΔH=b kJ·mol-1
则反应CH4(g)+2NO2(g)===N2(g)+CO2(g)+2H2O(g)的ΔH=________ kJ·mol-1(用含a、b的代数式表示)。
(2) 将燃煤废气中的CO2转化为二甲醚的反应原理为:
2CO2(g)+6H2(g)  CH3OCH3(g)+3H2O(g);ΔH
CH3OCH3(g)+3H2O(g);ΔH
① 该反应平衡常数表达式为K=________。
② 已知在某压强下,该反应在不同温度、不同投料比时,CO2的转化率如右图所示。该反应的ΔH________(填“>”“<”或“=”)0。若温度不变,减小反应投料比[n(H2) /n(CO2)],则K将________(填“增大”“减小”或“不变”)。
③ 二甲醚燃料电池具有启动快,效率高等优点,若电解质为酸性,二甲醚燃料电池的负极反应为____________________________。
(3) 以CO2为原料合成的碳酸酯(仅含碳、氢、氧三种元素)是用途广泛的化学品,某种碳酸酯(DPC)水解产物之一遇氯化铁溶液显紫色,右图为它的核磁共振氢谱图,请写出DPC的结构简式:____________。
(4) 某电厂的粉煤灰含莫来石(主要成分为Al6Si2O13、SiO2)。将其和纯碱在高温下烧结,可制取NaAlSiO4(霞石)、Na2SiO3和NaAlO2,有关化学方程式(反应条件均为高温)为:
Al6Si2O13+3Na2CO3===2NaAlSiO4+4NaAlO2+3CO2↑
Al6Si2O13+5Na2CO3===2Na2SiO3+6NaAlO2+5CO2↑
SiO2+Na2CO3===Na2SiO3+CO2↑
则用1 mol Al6Si2O13和4 mol SiO2通过以上反应制得5 mol NaAlO2,共消耗Na2CO3为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(10分,每空2分) 往一个容积为5L的密闭容器中,通入2molN2和3molH2,在一定条件下,发生反应 N2+3H2 2NH3,2 min后测得容器中生成了1mol NH3,试求:
2NH3,2 min后测得容器中生成了1mol NH3,试求:
(1)2 min时,N2的物质的量 ; (2)2 min时,H2的物质的量浓度 ;
(3)2 min时,H2的转化率 ; (4)2min内,N2的平均反应速率 ;
(5)N2、H2、NH3的反应速率之比 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化为无毒气体。汽车尾气中CO与H2O(g)在一定条件下可以发生反应:
CO(g)+H2O(g) CO2(g)+H2(g)ΔH<0。820 ℃时在甲、乙、丙三个恒容密闭容器中,起始时按照下表进行投料,达到平衡状态,K=1.0。
CO2(g)+H2(g)ΔH<0。820 ℃时在甲、乙、丙三个恒容密闭容器中,起始时按照下表进行投料,达到平衡状态,K=1.0。
| 起始物质的量 | 甲 | 乙 | 丙 |
| n(H2O)/mol | 0.10 | 0.20 | 0.20 |
| n(CO)/mol | 0.10 | 0.10 | 0.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(16分)在一容积为2 L的密闭容器内加入0.2 molA和0.6 molB,在一定条件下发生反应:A(s)+3B(g) 2C(s)+3D(g) 已知该反应在不同温度下的平衡常数如下表:
2C(s)+3D(g) 已知该反应在不同温度下的平衡常数如下表:
| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 64.0 | 50.7 | 42.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(18分)已知可逆反应CO2(g) + H2(g) CO(g) + H2O(g),
CO(g) + H2O(g),
⑴写出该反应的化学平衡常数表达式:K= 。
⑵830K时,若起始时:c (CO2)=2mol/L,c (H2)=3mol/L,平衡时CO2的转化率为60%,氢气的转化率为 ;K值为 。
⑶830K时,若只将起始时c (H2)改为6mol/L,则氢气的转化率为 。
⑷若830K时,起始浓度c (CO2) =" a" mol/L,c (H2) =" b" mol/L,H2O的平衡浓度为c (H2O) =" c" mol/L,则:①a、b、c之间的关系式是 ;②当a = b时,a = c。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
反应A(g) 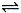 B(g) +C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L。温度T1和T2下A的浓度与时间关系如图所示。回答下列问题:
B(g) +C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L。温度T1和T2下A的浓度与时间关系如图所示。回答下列问题: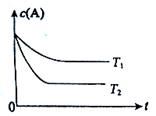
(1)上述反应的温度T1 T2,平衡常数K(T1) K(T2)。(填“大于”、“小于”或“等于”)
(2)若温度T2时,5min后反应达到平衡,A的转化率为70%,则:
①平衡时体系总的物质的量为 。
②反应的平衡常数K= 。
③反应在0~5min区间的平均反应速率v(A)= 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
环境中常见的重金属污染物有:汞.铅.锰.铬.镉。处理工业废水中含有的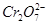 和
和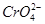 ,常用的方法有两种。
,常用的方法有两种。
方法1 还原沉淀法该法的工艺流程为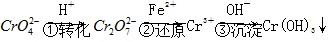 。
。
其中第①步存在平衡2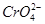 (黄色)+2H+
(黄色)+2H+
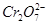 (橙色)+H2O。
(橙色)+H2O。
(1)写出第①步反应的平衡常数表达式_________________________________。
(2)关于第①步反应,下列说法正确的是________。
A.通过测定溶液的pH可以判断反应是否已达平衡状态
B.该反应为氧化还原反应
C.强酸性环境,溶液的颜色为橙色
(3)第②步中,还原0.1 mol 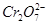 ,需要________mol的FeSO4·7H2O。
,需要________mol的FeSO4·7H2O。
(4)第③步除生成Cr(OH)3外,还可能生成的沉淀为________。在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)  Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=10-32,当c(Cr3+)降至10-5 mol·L-1时,认为c(Cr3+)已经完全沉淀,现将第③步溶液的pH调至4,请通过计算说明Cr3+是否沉淀完全(请写出计算过程):______________________________________________。
Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=10-32,当c(Cr3+)降至10-5 mol·L-1时,认为c(Cr3+)已经完全沉淀,现将第③步溶液的pH调至4,请通过计算说明Cr3+是否沉淀完全(请写出计算过程):______________________________________________。
方法2 电解法
(5)实验室利用如图装置模拟电解法处理含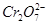 的废水,电解时阳极反应式为________,阴极反应式为________,得到的金属阳离子在阴极区可沉淀完全,从水的电离平衡角度解释其原因是________________________。
的废水,电解时阳极反应式为________,阴极反应式为________,得到的金属阳离子在阴极区可沉淀完全,从水的电离平衡角度解释其原因是________________________。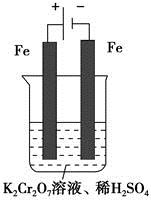
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
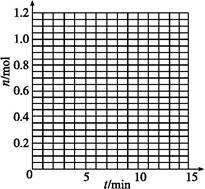
某温度时,在2 L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示。
(1)根据表中数据,在图中画出X、Y、Z的物质的量(n)随时间(t)变化的曲线:
| t/min | X/mol | Y/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 1 | 0.90 | 0.80 | 0.20 |
| 3 | 0.75 | 0.50 | 0.50 |
| 5 | 0.65 | 0.30 | 0.70 |
| 9 | 0.55 | 0.10 | 0.90 |
| 10 | 0.55 | 0.10 | 0.90 |
| 14 | 0.55 | 0.10 | 0.90 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com