
【题目】已知一氧化碳与水蒸气的反应为:CO(g)+H2O(g )![]() CO2(g)+H2(g)在427℃时的平衡常数是9,如果反应开始时,一氧化碳和水蒸气的浓度都为1mol/L,5min达到平衡。计算:
CO2(g)+H2(g)在427℃时的平衡常数是9,如果反应开始时,一氧化碳和水蒸气的浓度都为1mol/L,5min达到平衡。计算:
(1)从反应开始到达到平衡时用H2表示的反应速率__________。
(2)CO的转化率___________。
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】下表是不同温度下水的离子积数据:

试回答以下问题:
(1)若25<t1<t2,则a___1×10-14 (填“>”、“<”或“=”),作此判断的理由是______。
(2)25℃下,某Na2SO4溶液中c(SO42-)=5×10-4 mol·L﹣1,取该溶液1mL加水稀释至10mL,则稀释后溶液中c(Na+):c(OH-)=__________。
(3)在t2℃下,pH=10的NaOH溶液中,水电离产生的OH-为浓度为_________。
(4)t2℃下,将pH=11的NaOH溶液V1L与pH=1的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1:V2=________。
(5)有H+浓度相同、体积相等的三种酸:a、盐酸 b、硫酸 c、醋酸,同时加入足量的锌,则开始反应时速率大小顺序为_____;反应完全后生成H2的质量大小关系为____(用abc表示酸)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液在如下图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃用品是________;
(2)烧杯间填满碎纸条的作用是________________________;
(3)大烧杯上如不盖硬纸板,求得的中和热数值_____(填“偏大”“偏小”“无影响”);
(4)实验中改用60 mL 0.50 mol/L盐酸跟50 mL 0.55 mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量________(填“相等”“不相等”),所求中和热________(填“相等”“不相等”),简述理由______________________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气体分子中的极性键在红外线的照射下,易像弹簧一样做伸缩和弯曲运动,从而产生热量造成温室效应。下列不属于温室效应气体的是
A. CO2B. N2OC. CH4D. N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列7种物质:①NaOH、②NaHCO3、③HCl、④CH3COOH、⑤C2H5OH、⑥Al、⑦食盐水。
(1)上述物质中属于强电解质的是________(填序号),属于弱电解质的是________(填序号),属于非电解质的是________(填序号),既能跟盐酸反应又能跟NaOH溶液反应的是____________(填序号)。
(2)上述②的水溶液呈碱性的原因是(用离子方程式表示) ______________________。
(3)上述④的水溶液呈酸性的原因是(用离子方程式表示)__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 合成硫酸的工业尾气可以直接排入大气
B. 进入接触室的气体,必须先经净化、干燥
C. 从沸腾炉中排出的炉渣可以作为肥料
D. 在高温、高压下由SO2和O2合成SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式中,正确的是( )
A. H2SO4===H2++SO42- B. Ba(OH)2===Ba2++OH﹣
C. NaNO3===Na++NO3- D. CuSO4===Cu+2+SO4-2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,A处通入干燥Cl2 , 关闭B阀时,C处的红色布条看不到明显现象,打开B阀后,C处红色布条逐渐褪色,则D瓶中装的是( ) 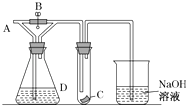
A.浓H2SO4
B.NaOH溶液
C.浓盐酸
D.饱和NaCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用下图实验装置验证通过改变浓度来实现反应2Fe3++2I-=2Fe2++I2中Fe3+与Fe2+的相互转化。K闭合时,电流表指针第一次发生偏转,当指针归零后,向左管滴加0.01mol/L的AgNO3溶液,发现指针第二次偏转,方向相反。下列有关说法不正确的是

A. 指针第一次偏转时,b极反应式为Fe3++e-=Fe2+
B. 加入AgNO3后,a为正极
C. 第二次指针偏转的原因是:I-浓度减小,反应逆向进行
D. 当b极有0.001 mol Fe3+被还原时,则通过盐桥的电子数为0.001 NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com