
【题目】质量分数为a%,物质的量浓度为c1 mol/L的稀硫酸蒸发水后,其质量分数变为2a%,此时物质的量浓度为c2 mol/L,则c1与c2的关系为
A. c2=2c1B. c2<2c1C. c2>2c1D. c1=2c2
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源: 题型:
【题目】某烃的分子式为C10H14 , 它不能使溴水褪色,但可使KMnO4酸性溶液褪色,分子结构中只含有一个烷基,符合条件的烃有( )
A.2种
B.3种
C.4种
D.5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可用来鉴别己烯、甲苯、乙酸乙酯、苯酚溶液的一组试剂是( )
A.FeCl3溶液、溴水
B.碳酸钠溶液、溴水
C.酸性高锰酸钾溶液、溴水
D.酸性高锰酸钾溶液、FeCl3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向500mL稀硝酸中加入一定质量的铁粉,铁粉完全溶解后,放出NO气体5.6L(标准状况),同时溶液质量增加9.3g,下列判断正确的是( )
A.原溶液中投入铁粉物质的量是0.25mol
B.原溶液中的HNO3浓度是2.0mol/L
C.反应后的溶液中还可以溶解9.6g铜
D.反应后的溶液中c(Fe2+):c(Fe3+)=1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】富铁铝土矿(主要含有A12O3、Fe2O3、FeO和SiO2)可制备新型净水剂液体聚合硫酸铝铁[AlaFeb(OH)m(SO4)n].研究发现,当a=b时净水效果最好.工艺流程如下(部分操作和产物略):![]()
(1)A12O3与H2SO4发生反应的离子方程式是 .
(2)测得滤液中 ![]() >1.加入FeSO47H2O和H2O2的作用是(结合化学用语说明) .
>1.加入FeSO47H2O和H2O2的作用是(结合化学用语说明) .
(3)将溶液A电解得到液体聚合硫酸铝铁.装置如图所示(阴离子交换膜只允许阴离子通过,电极为惰性电极)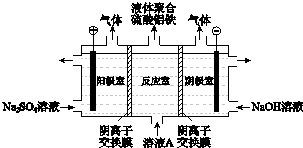
①阴极室的电极反应式是 .
②电解过程阳极室溶液pH的变化是(填“增大”、“减小”或“不变”).
③简述在反应室中生成液体聚合硫酸铝铁的原理 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向500mL稀硝酸中加入一定质量的铁粉,铁粉完全溶解后,放出NO气体5.6L(标准状况),同时溶液质量增加9.3g,下列判断正确的是( )
A.原溶液中投入铁粉物质的量是0.25mol
B.原溶液中的HNO3浓度是2.0mol/L
C.反应后的溶液中还可以溶解9.6g铜
D.反应后的溶液中c(Fe2+):c(Fe3+)=1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于1molL-1硫酸溶液的说法中正确的是( )
A. 1L水中含有1mol H2SO4
B. 1L溶液中含有1mol H+
C. 1L硫酸溶液中含有96g SO42-
D. 将98g H2SO4溶于1L水中配成上述溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 标准状况下,O2的体积约为22.4 L
B. 标准状况下,CO2的气体摩尔体积为22.4 L
C. 标准状况下,0.5 mol的H2O的体积约为11.2 L
D. 0℃,101kPa时,1 mol O2和N2的混合气体的总体积约为22.4 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过滤是水净化过程中的一道重要工序,它能( )
A. 给水消毒,达到饮用标准B. 将污水转化为纯水
C. 除去水中的异味D. 除去水中的不溶性杂质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com