
三氯化六氨合钴(Ⅲ)是一种重要的化工产品, 实验中采用H2O2作氧化剂,在大量氨和氯化铵存在下,选择活性炭作为催化剂将Co(Ⅱ)氧化为Co(Ⅲ),来制备三氯化六氨合钴(Ⅲ)配合物,反应式为:2CoCl2·6H2O + 10NH3 + 2NH4Cl + H2O2 活性炭2[Co(NH3)6]Cl3 +14H2O
已知:① 钴(Ⅱ)与氯化铵和氨水作用,经氧化后一般可生成三种产物:紫红色的二氯化一氯五氨合钴[Co(NH3)5 Cl]Cl2晶体、砖红色的三氯化五氨一水合钴[Co(NH3)5 H2O]Cl3晶体、橙黄色的三氯化六氨合钴[Co(NH3)6]Cl3晶体,控制不同的条件可得不同的产物(如温度不同产物也不同)。293K时,[Co(NH3)6]Cl3在水中的溶解度为0.26mol/L
②CoCl2、[Co(NH3)6]Cl3、[Co(NH3)5 Cl]Cl2在水中能完全电离
③制备三氯化六氨合钴(Ⅲ)粗产品的流程如下:

④三氯化六氨合钴(Ⅲ)粗产品的提纯流程如下:
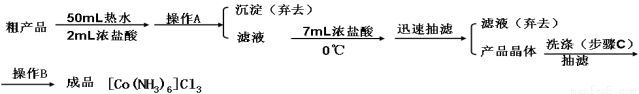
⑤制备过程中可能用到的部分装置如下:


请回答下列问题:
(1)操作B的名称是 ,操作A后所弃去的沉淀中一定有 。
(2)CoCl2在没有铵盐存在的情况下,遇氨水生成蓝色沉淀,该反应的离子方程式为 。原料NH4Cl的主要作用有:① ;②提供NH3。
(3)冷却至10℃后,步骤B中逐滴加入H2O2溶液的目的:① ;②使反应温和进行。
(4)操作A的名称为 ,进行该操作的装置是 (填序号)。
A.装置Ⅰ B.装置Ⅱ C.装置Ⅲ
若操作过程中,发现漏斗尖嘴处有少量晶体析出,处理方法是 。
装置Ⅱ中仪器A、B、C、D的名称分别是 、 、 、 。
(5)步骤C进行洗涤时要用到两种试剂,应该先用_____(填序号,下同)洗涤,后用 洗涤。
A. 饱和氯化钠溶液 B. 无水乙醇 C. 浓盐酸
(6)你认为本实验提高产率的关键步骤有哪些? 。
(7)与[Co(NH3)6]Cl3类似的产品还有[Co(NH3)5Cl]Cl2,请简述验证某晶体是[Co(NH3)6]Cl3 还是
[Co(NH3)5Cl]Cl2的实验方案: 。
(1)烘干;活性炭 (2)Co2++2NH3·H2O=Co(OH)2↓+ 2NH4+ ; 抑制 NH3·H2O的电离
(3)避免H2O2的分解 (4)趁热过滤;A;用滤液清洗;布氏漏斗;吸滤瓶;安全瓶;抽气泵
(5)C B (6)①煮沸20min,使反应完全 ②整个过程温度的控制,因为温度不同,产物不同
③最后加入的7mL浓盐酸,因为借助同离子效应使产品析出
(7)取等质量的晶体分别溶于水,室温下加足量的AgNO3溶液后,滤去沉淀,对滤液再进行加热,又能产生沉淀的是[Co(NH3)5 Cl]Cl2,不能再产生沉淀的是[Co(NH3)6 ]Cl3
【解析】
试题分析:(1)抽滤后得到的产品中含有水分,需要烘干,因此操作B的名称是烘干;反应中需要活性炭作催化剂,而活性炭不溶于水,所以操作A后所弃去的沉淀中一定有活性炭。
(2)CoCl2在没有铵盐存在的情况下,遇氨水生成蓝色沉淀,该蓝色沉淀是氢氧化钴,该反应的离子方程式为Co2++2NH3·H2O=Co(OH)2↓+ 2NH4+ ;在碱性条件下容易生成氢氧化钴沉淀,因此原料NH4Cl的主要作用除了提供NH3以外,还有抑制 NH3·H2O的电离,降低溶液的碱性。
(3)由于双氧水不稳定,受热易分解,因此冷却至10℃后,步骤B中逐滴加入H2O2溶液的目的是避免H2O2的分解,另外使反应温和进行。
(4)由于温度不同,产物也不同,因此操作A应该是趁热过滤;由于需要保持一定温度,所以选择装置I,即答案选A;若操作过程中,发现漏斗尖嘴处有少量晶体析出,处理方法是用滤液清洗;根据仪器的构造特点可知装置Ⅱ中仪器A、B、C、D的名称分别是布氏漏斗;吸滤瓶;安全瓶;抽气泵。
(5)增大氯离子浓度可以防止产品溶解而损失,因此三氯化六氨合钴首先应该用浓盐酸洗涤,最后再用有机溶剂乙醇洗涤,故答案为C、B。
(6)根据以上分析可知实验提高产率的关键步骤①煮沸20min,使反应完全;②整个过程温度的控制,因为温度不同,产物不同;③最后加入的7mL浓盐酸,因为借助同离子效应使产品析出。
(7)根据结构可知,氯离子作为配体的数目是不同的,且温度不同,产品不同,据此可以验证,即取等质量的晶体分别溶于水,室温下加足量的AgNO3溶液后,滤去沉淀,对滤液再进行加热,又能产生沉淀的是[Co(NH3)5 Cl]Cl2,不能再产生沉淀的是[Co(NH3)6 ]Cl3。
考点:考查物质制备实验方案设计、实验探究与评价等


科目:高中化学 来源:2013-2014浙江省高一下学期期末考试化学试卷(解析版) 题型:实验题
在实验室中可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。
图中: ①为氯气发生装置;②的试管里盛有15mL 30% KOH 溶液.并置于热水浴中; ③的试管里盛有15mL 8 % NaOH 溶液.并置于冰水浴中; ④的试管里加有紫色石蕊试液; ⑤为尾气吸收装置。
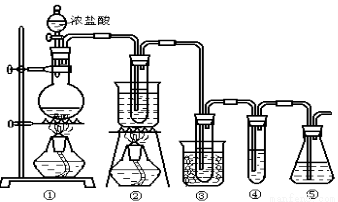
请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过______(填写仪器名称)向烧瓶中加入适量的浓盐酸。实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有_________(填写下列编号字母)的净化装置。
A.碱石灰 B.饱和食盐水 C.浓硫酸 D.饱和碳酸氢钠溶液
(2)比较制取氯酸钾和次氯酸钠的条件.二者的差异是 。反应完毕经冷却后,②的试管中有大量晶体析出。下图中符合该晶体溶解度曲线的是_______(填写编号字母);从②的试管中分离出该晶体的方法是 (填写实验操作名称)。

(3)本实验中制取次氯酸钠的离子方程式是: 。
(4)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白:
实验现象 | 原因 |
溶液最初从紫色逐渐变为 色 |
氯气与水反应生成的H+使石蕊变色 |
随后溶液逐渐变为无色 |
______________________________________ |
然后溶液从无色逐渐变为 色 |
_________________________________________ |
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省宁波市高二下学期期末考试化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列说法一定正确的是 ( )
A.常温下,1 L 0.1 mol/L的NH4NO3溶液中氧原子数为0.3NA
B.1 mol的羟基与1 mol的氢氧根离子所含电子数均为10NA
C.常温、常压下,4.6 g NO2和N2O4混合气体中含有的O原子数目为0.2NA
D.Fe与水蒸气在高温条件下反应,有1 mol Fe参与反应,则转移电子的数目为3NA
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省宁波市高一下学期期末考试化学试卷(解析版) 题型:选择题
下列说法错误的是( )
A.一般的水是由10个以上的水分子聚结组成一个水分子团,叫大分子团水,科学家能把大分子团水变成5-8个水分子组成的小分子团水,一次饮用125 mL可维持人体6小时正常需水量,这个转变过程改变了水分子间的结构和物理性质
B.离子化合物中可能有共价键
C.科学家在青藏高原深处发现了天然的氮化硼(BN,具有高熔点、高密度、高硬度等特性),它可能是原子晶体
D.用“撕裂”方法可从石墨材料中剥离出的单层碳原子面材料(石墨烯),用这种方法从C60、金刚石等碳原子中获得“只有一层碳原子厚的碳薄片”也将成为研究方向
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省宁波市高一下学期期末考试化学试卷(解析版) 题型:选择题
对于化学反应3W(g)+2X(g)===4Y(g)+3Z (g),下列反应速率关系中,正确的是( )
A.v(W)=3v(Z) B.2v(X)=3v(Z) C.2v(X)=v(Y) D.3v(W)=2v(X)
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省台州市路桥区高考理综化学模拟试卷二试卷(解析版) 题型:选择题
下列说法正确的是 ( )
A.用酸性高锰酸钾即可鉴别苯酚溶液,2,4-己二烯和甲苯
B. 按系统命名法化合物  的名称为:2,5,6-三甲基-3-乙基庚烷
的名称为:2,5,6-三甲基-3-乙基庚烷
C. 新型解热镇痛抗炎药贝诺酯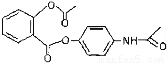 在酸性条件下完全水解可以得到3种有机物
在酸性条件下完全水解可以得到3种有机物
D.β—月桂烯的结构如图 ,一分子该物质与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种
,一分子该物质与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省台州市路桥区高考理综化学模拟试卷一试卷(解析版) 题型:填空题
(15分)氨是最重要的化工产品之一。
(1)合成氨用的氢气可以甲烷为原料制得:CH4(g)+H2O(g)  CO(g)+3H2(g)。有关化学反应的能量变化如下图所示。CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式为 。
CO(g)+3H2(g)。有关化学反应的能量变化如下图所示。CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式为 。



(2)CO对合成氨的催化剂有毒害作用,常用乙酸二氨合铜(Ⅰ)溶液来吸收原料气中CO,其反应原理为:[Cu(NH3)2CH3COO] (l)+CO(g)+NH3(g) [Cu(NH3)3] CH3COO·CO(l) △H<0。吸收CO后的乙酸铜氨液经过适当处理后又可再生,恢复其吸收CO的能力以供循环使用,再生的适宜条件是 。
[Cu(NH3)3] CH3COO·CO(l) △H<0。吸收CO后的乙酸铜氨液经过适当处理后又可再生,恢复其吸收CO的能力以供循环使用,再生的适宜条件是 。
(填写选项编号)
A.高温、高压 B.高温、低压 C.低温、低压 D.低温、高压
(3)用氨气制取尿素[CO(NH2)2]的反应为:2NH3(g)+CO2(g) CO(NH2)2(l)+H2O(g) △H<0
CO(NH2)2(l)+H2O(g) △H<0
某温度下,向容积为100L的密闭容器中通入4mol NH3和2molCO2,该反应进行到40 s时达到平衡,此时CO2的转化率为50%。该温度下此反应平衡常数K的值为_________。下图中的曲线表示该反应在前25 s内的反应进程中的NH3浓度变化。若反应延续至70s,保持其它条件不变情况下,请在图中用实线画出使用催化剂时该反应的进程曲线。

(4)将尿素施入土壤后,大部分是通过转化为碳酸铵或碳酸氢铵后才被作物所利用,尿素分子在微生物分泌的脲酶作用下,转化为碳酸铵。已知弱电解质在水中的电离平衡常数(25℃)如下表:
弱电解质 | H2CO3 | NH3·H2O |
电离平衡常数 | Ka1=4.30×10-7 Ka2=5.61×10-11 | 1.77×10-5 |
现有常温下0.1 mol·L-1的(NH4)2CO3溶液,
①你认为该溶液呈 性(填“酸”、“中”、“碱”),原因是 。
②就该溶液中粒子之间有下列关系式,你认为其中正确的是 。
A.c (NH4+)>c (CO32-)>c (HCO3-)>c (NH3·H2O)
B.c(NH4+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-)
C.c (CO32-) + c (HCO3-) +c (H2CO3)=0.1 mol·L-1
D.c (NH4+)+ c (NH3·H2O)=2 c (CO32-) + 2c (HCO3-) +2 c (H2CO3)
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省下学期第二次统练高二化学试卷(解析版) 题型:选择题
最近,美国LawreceLiremore国家实验室(LLNL)的V.Lota.C.S.Yoo和Cynn成功地在高压下将CO2转化为具有类似SiO2结构的原子晶体,下列关于CO2的原子晶体说法正确的是
A.CO2的原子晶体中存在范德华力,每1molCO2原子晶体中含有2NA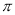 键
键
B.在一定条件下,CO2原子晶体转化为分子晶体CO2是物理变化
C.熔点:金刚石>氯化钠>原子晶体CO2
D.在CO2的原子晶体中,每个C原子周围结合4个O原子,每个O原子与两个C原子相结合
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省下学期第二次统练高一化学试卷(解析版) 题型:选择题
化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是
A.原子核内有10个中子的氧原子:18O B.乙烯的结构简式: CH2CH2
C.CH4 分子的比例模型: D.-CH3(甲基)的电子式为:
D.-CH3(甲基)的电子式为: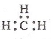
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com