
【题目】下列实验操作、现象和结论均正确的是( )
选项 | 实验操作 | 现象 | 结论 |
A | 植物油和溴水混合后振荡、静置 | 溶液分层,溴水褪色 | 植物油萃取了溴水中的Br2 |
B | 将硫酸酸化的H2O2滴入Fe(NO3)2溶液中 | 溶液变黄色 | H2O2的氧化性比Fe3+弱 |
C |
| 出现白色沉淀 | 氨气、二氧化碳与饱和食盐水反映生成碳酸钠 |
D | 将盛有铜与浓硫酸的试管加热,发现试管底部出现白色固体,倒去试管中液体,再加入适量水 | 白色固体溶解,溶液显蓝色 | 白色固体为无水硫酸铜 |
A. AB. BC. CD. D
科目:高中化学 来源: 题型:
【题目】将一定量氨基甲酸铵(NH2COONH4)加入密闭容器中,发生反应NH2COONH4(s)2NH3(g)+CO2(g)。该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示,下列说法错误的是
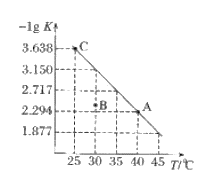
A. 该反应的△H>0
B. C点对应状态的平衡常数K(C)=103.638
C. NH3的体积分数不变时,该反应一定达到平衡状态
D. 30℃时,B点对应状态的![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z是第ⅠA~ⅦA族的三种非金属元素,它们在元素周期表中的位置如图所示,试回答下列问题。

(1)X元素单质的化学式是________。
(2)Y元素的原子结构示意图是____________,Y与Na所形成化合物的电子式为________________________。
(3)Z元素的名称是________,从元素原子得失电子的角度看,Z元素具有________性;若从Z元素在元素周期表中所处位置看,它具有这种性质的原因是_________________________,其价电子排布式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】妈妈教小鲁蒸馒头:先用酵头发面,面团发酵至两倍大后,再加纯碱调节酸性,然后将面团揉切后上锅蒸即可。小鲁查阅资料得知,酵头可使面团在微生物作用下产生CO2气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。
(1)下列关于纯碱的认识正确的是___。
A.受热易分解 B.水溶液显碱性 C.属于碱 D.可与酸反应
(2)小鲁探究用Na2CO3调节面团酸度,而不用NaHCO3的原因。
①Na2CO3与NaHCO3质量均为1g时,消耗H+的物质的量更多的是___。
②以Na2CO3或NaHCO3为例,计算消耗H+的物质的量,写出计算过程。___
(3)小鲁实际操作时,发现面团发得不好,面团内的气孔少,略有酸味。妈妈指导小鲁将Na2CO3改用NaHCO3,继续揉面,上锅蒸后果然蒸出了松软的馒头。解释NaHCO3的作用___。
(4)某品牌复合膨松剂的说明书如图所示。

其中葡萄糖酸-δ-内酯和淀粉是助剂,其作用是防止膨松剂吸潮结块而失效。焦磷酸二氢二钠的作用是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下VL氨气溶解在1L水中(水的密度近似为lg/ml),所得溶液的密度为ρg/ml,质量分数为W,物质浓度为cmol/L,则下列关系中不正确的是
A. W= 17V/(17V+22400) B. W= 17c/(l000ρ)
C. ρ= (17V+ 22400)/(22.4 + 22.4V) D. c=1000Vρ/(17V+22400)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.10molL1的NaOH溶液分别滴定20.00mL浓度均为0.10molL1的CH3COOH溶液和HCN溶液,所得滴定曲线如图所示,下列说法正确的是( )

A. 点①和点②所示溶液中:c(CH3COO)<c(CN)
B. 点④所示溶液中:c(Na+)>c(OH)>c(CH3COO)>c(H+)
C. 点①和点②所示溶液中:c(CH3COO)c(CN)=c(HCN)c(CH3COOH)
D. 点③所示溶液中:c(CH3COO)+c(OH)=c(CH3COOH)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分氧化的铁铜合金样品(氧化产物为Fe2O3、CuO)共5.76g,经如下处理:

下列说法正确的是( )
A. 滤液A中的阳离子为Fe3+、Fe2+、H+ B. 样品中Fe元素的质量为2.24g
C. 样品中CuO的质量为4.0g D. V=896
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:

(1)该“84消毒液”的物质的量浓度约___mol·L-1(小数点后保留一位)。
(2)某同学取100mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=___mol·L-1。
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。需要称量NaClO固体的质量为__g。下列为打乱了的操作示意图,其正确排序为____。

(4)配制过程中下列各项操作对消毒液物质的量浓度有和影响(填“偏小”、“偏大”或“无影响”)
A.用托盘天平称量NaClO固体时,砝码生锈___。
B.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水____。
C.定容时,俯视容量瓶刻度线进行定容____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com