
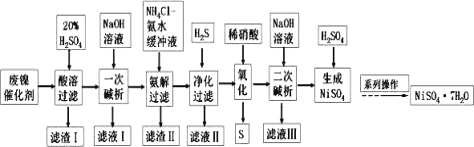
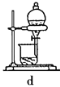
【题目】硫酸镍是一种重要的化工中间体,是镍行业研究的热点。一种以石油化工中废镍催化剂(主要成分为NiCO3和SiO2,含少量Fe2O3、Cr2O3)为原料制备硫酸镍的工业流程如图:
已知:①NiS、Ni(OH)2、Cr(OH)3均难溶于水,Cr(OH)3是两性氢氧化物。
②Fe(OH)3不溶于NH4Cl—氨水的混合液,Ni(OH)2溶于NH4Cl—氨水的混合液生成[Ni(NH3)6]2+。
③离子浓度≤10-5mol·L-1时,离子沉淀完全。请回答下列问题:
(1)为提高“酸溶”时镍元素的浸出率,所采取的的措施为____(写1种)。
(2)“一次碱析”时,加入的NaOH溶液需过量,则含铬微粒发生反应的离子方程式为_______。
(3)“氨解”的目的为__ “氨解”时需要控制低温原因是______。
(4)“氧化”时发生反应的化学方程式为_____。
(5)“二次碱浸”时,若使溶液中的Ni2+沉淀完全,则需维持c(OH-)不低于_____。(已知:Ni(OH)2的Ksp=2×10-15,![]() ≈1.4)。
≈1.4)。
(6)若在流程中完成“系列操作”。则下列实验操作中,不需要的是____(填下列各项中序号)。
【答案】废镍催化剂粉碎、增大硫酸浓度、升温一种合理即可 ![]() 实现镍元素和铁元素的分离或除去铁元素 防止氨水分解生成氨气,脱离反应体系,不利于生成[Ni(NH3)6]2+ 3NiS+8HNO3(稀)=3Ni(NO3)2+2NO↑+3S↓+4H2O 1.42×10-5mol·L-1 cd
实现镍元素和铁元素的分离或除去铁元素 防止氨水分解生成氨气,脱离反应体系,不利于生成[Ni(NH3)6]2+ 3NiS+8HNO3(稀)=3Ni(NO3)2+2NO↑+3S↓+4H2O 1.42×10-5mol·L-1 cd
【解析】
废镍催化剂(主要成分为NiCO3和SiO2,含少量Fe2O3、Cr2O3)经酸溶得到硫酸镍、硫酸铁、硫酸铬溶液,二氧化硅不溶于硫酸为滤渣I的主要成分;向滤液中加入过量氢氧化钠溶液得到氢氧化镍沉淀、氢氧化铁沉淀、偏铬酸钠溶液,偏铬酸钠溶液为滤液I的主要成分;向沉淀中加入NH4Cl-氨水的混合液,氢氧化铁沉淀不溶于此溶液,为滤渣II的主要成分,氢氧化镍沉淀溶于此溶液得到[Ni(NH3)6]2+溶液;向溶液中通入H2S,生成NiS沉淀;向沉淀中滴入稀硝酸得到硝酸镍;向硝酸镍中加入氢氧化钠溶液得到氢氧化镍沉淀;向沉淀中加入硫酸得到硫酸镍;在经过系列操作得到NiSO4·7H2O,据此解答本题。
(1)为提高“酸溶”时镍元素的浸出率,可将废镍催化剂粉碎增加反应接触表面积、增大硫酸浓度、升温等措施,
故答案为:废镍催化剂粉碎、增大硫酸浓度、升温一种合理即可;
(2)根据信息可知,Cr(OH)3是两性氢氧化物,性质类似于氢氧化铝,铬离子与少量氢氧化钠反应生成氢氧化铬,若氢氧化钠过量,则过量的氢氧化钠与氢氧化铬反应生成偏铬酸钠,故“一次碱析”时,加入的NaOH溶液需过量,则含铬微粒发生反应的离子方程式为:![]() ,
,
故答案为:![]() ;
;
(3)废镍催化剂中的铁元素在“一次碱析”时转化为氢氧化铁,由于Fe(OH)3不溶于NH4Cl-氨水的混合液,Ni(OH)2溶于NH4Cl-氨水的混合液生成[Ni(NH3)6]2+,则“氨解”的目的是实现镍元素和铁元素的分离或除去铁元素;加热条件下,氨会挥发,因此控制低温的原因是:防止氨水分解生成氨气,脱离反应体系,不利于生成[Ni(NH3)6]2+,
故答案为:实现镍元素和铁元素的分离或除去铁元素;防止氨水分解生成氨气,脱离反应体系,不利于生成[Ni(NH3)6]2+;
(4)“氧化”时发生的反应是稀硝酸和NiS的反应,根据流程图反应生成S,则稀硝酸中氮元素由+5价降低到+2价生成NO,NiS中的硫元素由-2价升高到0价生成S单质,根据得失电子守恒和原子守恒,反应的化学方程式为:3NiS+8HNO3(稀)=3Ni(NO3)2+2NO↑+3S↓+4H2O,
故答案为:3NiS+8HNO3(稀)=3Ni(NO3)2+2NO↑+3S↓+4H2O;
(5)氢氧化镍中存在溶解平衡,Ka=c(Ni2+)×c2(OH-),根据信息,离子浓度≤10-5mol·L-1时,离子沉淀完全,则2×10-15=10-5×c2(OH-),解得c(OH-)=1.4×10-5mol/L,则若使溶液中Ni2+沉淀完全,需维持c(OH-)不低于1.4×10-5mol/L,
故答案为:1.42×10-5mol·L-1;
(6)“系列操作”的目的是从NiSO4溶液中得到NiSO4·7H2O,其操作包括:蒸发浓缩、冷却结晶、过滤,故不需要的操作为cd,
故答案为:cd。


科目:高中化学 来源: 题型:
【题目】373K时,某 1L密闭容器中加入2mol NH3发生如下可逆反应:2NH3(g)![]() N2(g)+3H2(g)。其中物质H2的物质的量变化如下图所示。
N2(g)+3H2(g)。其中物质H2的物质的量变化如下图所示。
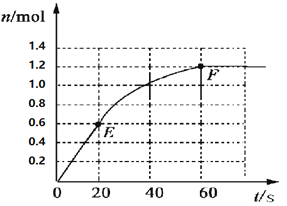
(1)前20 s内NH3(g)的平均反应速率为___________;
(2)373K时该反应的平衡常数的值为______________;
(3)若在此平衡体系中再加入1mol的NH3,与原平衡比较,新平衡时NH3的转化率______(填“增大”或“减小”,下同),NH3的平衡浓度_________。
(4)将原平衡升温至473K,重新达平衡时(其他条件不变),H2的平衡浓度为NH3的2倍,该反应的正反应为_________(填“放热反应”或“吸热反应”),为增大平衡体系中H2的物质的量,下列措施正确的是(其它条件相同)______。
a.升高温度 b.扩大容器的体积 c.加入合适的催化剂 d.再充入N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外兴趣小组对H2O2的分解速率做了如下实验探究。
(1)下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:用10mL H2O2制取150mLO2所需的时间(秒)
| 30% H2O2 | 15% H2O2 | 10% H2O2 | 5% H2O2 |
无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
无催化剂、加热 | 360 | 480 | 540 | 720 |
MnO2催化剂、加热 | 10 | 25 | 60 | 120 |
①该研究小组在设计方案时。考虑了浓度、___________、____________等因素对过氧化氢分解速率的影响。
②从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对分解速率有何影响?_______________________。
(2)将质量相同但聚集状态不同的MnO2分别加入到5mL 5%(密度为1.0g/cm3)的双氧水中,并用带火星的木条测试。测定结果如下:
实验 序号 | 催化剂(MnO2) | 操作 情况 | 观察结果 | 反应完成 所需的时间 |
A | 粉末状 | 混合不振荡 | 剧烈反应,带火星的木条复燃 | 5span>分钟 |
B | 块状 | 反应较慢,火星红亮但木条未复燃 | 30分钟 |
① 写出H2O2发生分解的化学反应方程式________________。求出实验A中H2O2在5分钟内的平均反应速率________________。(结果保留小数点后两位数字)
② 实验结果说明催化剂作用的大小与____________________有关。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】稀氨水中存在着下列平衡:NH3·H2O![]() NH4++OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入的物质或采取的措施是
NH4++OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入的物质或采取的措施是
①NH4Cl固体;②硫酸;③NaOH固体;④水;⑤加热;⑥加入少量MgSO4固体。
A.①②③B.③⑥C.③D.③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释事实的方程式不正确的是
A. 焊接铁轨:2Fe+Al2O3![]() 2Al+Fe2O3
2Al+Fe2O3
B. 人工固氮:N2+3H2![]() 2NH3
2NH3
C. 用纯碱除油污:CO32-+H2O![]() HCO3-+OH-
HCO3-+OH-
D. 用湿润的淀粉KI试纸检验Cl2:Cl2+2I-=2Cl-+I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上曾经通过反应“3Fe+4NaOH ![]() Fe3O4+2H2↑4Na↑”生产金属钠,己知铁的熔点1535℃、沸点3000℃。下列有关说法正确的是
Fe3O4+2H2↑4Na↑”生产金属钠,己知铁的熔点1535℃、沸点3000℃。下列有关说法正确的是
A.增大铁的量可以使反应速率加快
B.将生成的气体在空气中冷却可获得钠
C.每生成1molH2,转移的电子数约为4×6.02×1023
D.该反应条件下铁的金属性比钠强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1 g氢气完全燃烧生成水蒸气时放出热量121 kJ。且氧气中1 mol O=O键完全断裂时吸收热量496 kJ,水蒸气中1 mol H-O键形成时放出热量463 kJ,则氢气中1mol H-H键断裂时吸收热量为( )
A.920 kJB.557 kJC.188 kJD.436 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“侯氏制碱法”是我国化工专家侯德榜为世界制碱工业作出的突出贡献。某实验小组模拟“侯氏制碱法”的工艺流程及实验装置(部分夹持装置省略)如图:下列叙述正确的是( )
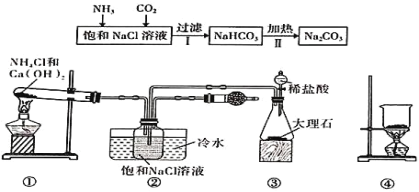
A.实验时先打开装置③中分液漏斗的旋塞,过一段时间后再点燃装置①的酒精灯
B.装置②的干燥管中可盛放碱石灰,作用是吸收多余的NH3
C.向步骤 I 所得滤液中通入氨气,加入细小的食盐颗粒并降温可析出NH4Cl
D.用装置④可实现步骤Ⅱ的转化,所得CO2可循环使用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与我们日常生活中的吃、穿、住、行、医关系密切:
(1)油脂、淀粉、蛋白质是我们食物中提供能量的主要物质,在人体内都能发生水解。
①油脂在酸性条件下水解的最终产物是_________和_________;
②上述三种物质不属高分子化合物的是_________,若要检验淀粉在淀粉酶作用下已经发生了水解,可取少量水解实验的溶液加入_________(填试剂的名称),加热后再根据实验现象判断;若要检验淀粉没有完全水解的,可取少量水解溶液加入几滴________,应观察到出现蓝色;
③蛋白质在人体内水解的最终产物是氨基酸.写出氨基酸共同含有的官能团的结构简式分别为_________和﹣COOH;
(2)现在越来越多的自行车采用铝合金作材料,它不仅轻便美观,而且也很耐久.它能长期使用的原因是_________,橡胶是制造轮胎的重要原料,天然橡胶通过硫化措施使其分子转变为_________分子结构可增大强度和弹性;
(3)聚丙烯腈﹣合成腈纶又称人造羊毛,丙烯腈为CH2=CHCN,请写出聚丙烯腈的结构简式_________,生活中除常用的氯系消毒剂外,过氧乙酸是另一种常见消毒剂,主要是因为其结构中含有_________而表现出强氧化性;
(4)_________形成的合金被称为“亲生物金属”,广泛作为人造骨的材料.为防止工业生产过程产生的悬浮颗粒物进入大气,可以将混有悬浮颗粒物的气体通过沉降进行处理;
(5)居室装修所用的有些石材会释放出一种放射性物质,长期接触可能引起癌症,免疫功能异常,该放射性物质主要是_________(填写该物质的名称);
(6)氢氧化铝、碳酸镁都可用于治疗胃酸过多引起的不适,请分别写出相关反应的离子方程式:①_________②_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com