
工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)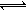 Si(s)+4HCl(g);△H=+QkJ/mol(Q>0) 某温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是 ( )
Si(s)+4HCl(g);△H=+QkJ/mol(Q>0) 某温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是 ( )
A. 反应过程中,若增大压强能提高SiCl4的转化率
B. 若反应开始时SiCl4为1mol,则达平衡时,吸收热量为QkJ
C. 在温度、体积不变的情况下,若按照起始充入比例再向容器中充入反应物 ,重新达平衡后,HCl的体积分数不变
D. 当反应吸收热量为0.025QkJ时,生成的HCl通入100mL 1mol/L的NaOH溶液恰好反应
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
有效地利用现有能源和开发新能源已受到各国的普遍重视。
(1)可用改进汽油组成的办法来改善汽油的燃烧性能。
例如,加入CH3OC(CH3)3来生产“无铅汽油”。
CH3OC(CH3)3分子中必存在的原子间连接形式有 (填编号)。
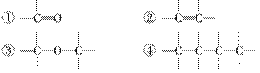
(2)天然气的燃烧产物无毒、热值高,而且管道输送方便,将成为我国西部开发的重点之一。天然气常和石油伴生,其主要的成分是 。能说明它是正四面体而非正方形平面结构的理由是 (填编号)。
①其一氯取代物不存在同分异构体 ②其二氯取代物不存在同分异构体 ③甲烷极难溶于水 ④它的四个氢原子完全相同
(3)新型燃氢汽车已研发多年,它清洁卫生、噪声低、启动快、行驶稳等,但是昂贵的氢气让人买得起车用不起气,看来有效开发利用氢能源,将成为能源领域的新热点,你认为以下可供开发又较经济的制氢方法是 (填编号)。
①电解水 ②锌和稀硫酸反应 ③光解海水
其次,制得纯氢气后还需要解决的问题是 (写出其中一个)。
查看答案和解析>>
科目:高中化学 来源: 题型:
高温下,某反应达到平衡,平衡常数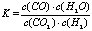 。恒容时,温度升高,H2浓度减小。下列说法正确的是 ( )
。恒容时,温度升高,H2浓度减小。下列说法正确的是 ( )
A. 该反应的焓变为正值
B. 恒温恒容下,通入He,H2浓度一定减小

 C. 升高温度,逆反应速率减小
C. 升高温度,逆反应速率减小
D. 该反应化学方程式为CO+H2O CO2+H2
查看答案和解析>>
科目:高中化学 来源: 题型:
反应4A(g)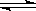 2B(g)+E(g) ΔH>0,达平衡时,要使正反应速率降低,A的浓度增大,应采取的措施是 ( )
2B(g)+E(g) ΔH>0,达平衡时,要使正反应速率降低,A的浓度增大,应采取的措施是 ( )
A.加压 B.减压 C.减少E的浓度 D.降温
查看答案和解析>>
科目:高中化学 来源: 题型:
 在一密闭体系中发生下列反应:
在一密闭体系中发生下列反应:
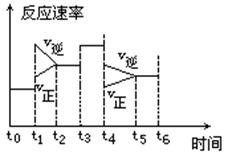
N2 +3H2  2NH3 ΔH<0 ,下图是某一时间段中反应速率与反应进程的曲线关系图:
2NH3 ΔH<0 ,下图是某一时间段中反应速率与反应进程的曲线关系图:
回答下列问题:
(1)处于平衡状态的时间段是______.
(2)t1、t3、t4时刻体系中分别对应的条件变化为:
, , ;
(3)下列各时间段时,氨的百分含量最高的是______.
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6
(4)对于上述反应,起始时加入1mol N2和3mol H2,在恒温恒压条件下反应达到平衡时生成a mol NH3,在恒温恒容条件下,达到平衡时生成b mol NH3,则a和b的大小关系为( )
(5)对于上述反应,在恒温恒容条件下,起始时充入2mol N2和3mol H2,达到平衡时生成b mol NH3,若相同条件下,起始时充入x mol N2,y mol H2, z mol NH3, 达到平衡时混合物中各组分的百分含量不变,则x y z 取值必须满足的一般条件为: , ;
(一个只含x, z;另一个只含y, z)
查看答案和解析>>
科目:高中化学 来源: 题型:
下面列举的是某化合物的组成和性质,能说明该物质肯定是有机物的是( )
A.仅由碳、氢两种元素组成
B.仅由碳、氢、氧三种元素组成
C.在氧气中燃烧只生成二氧化碳
D.熔点低而且难溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
已知芳香烃A、B的结构模型如下图所示,相关叙述正确的是( )
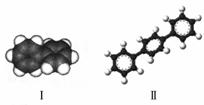
A.Ⅰ的结构简式为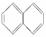 ,其一氯代物有2种
,其一氯代物有2种
B.Ⅰ和Ⅱ中都含碳碳单键和双键
C.Ⅰ与Ⅱ互为同系物,通式为CnH4n+2(n为苯环数)
D.与Ⅱ互为同类别物质的同分异构体共有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
 关于食物的酸碱性,下列说法正确的是( )
关于食物的酸碱性,下列说法正确的是( )
 A.食物溶于水后的溶液中pH < 7,则为酸性食物
A.食物溶于水后的溶液中pH < 7,则为酸性食物
 B.由C、N、S、P等元素组成的蛋白质是酸性食物
B.由C、N、S、P等元素组成的蛋白质是酸性食物
 C.蔬菜、水果多含钾、钠、钙、镁等盐类及果酸,习惯称为酸性食物
C.蔬菜、水果多含钾、钠、钙、镁等盐类及果酸,习惯称为酸性食物
 D.柠檬酸是酸性食物
D.柠檬酸是酸性食物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com