
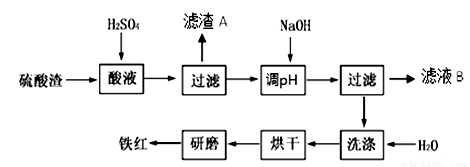
��16�֣���ˮ��Һ��ۺ���������������κ����ε�˫���������ԣ�һ����������Ϊ��������Ϊ�������õ�����������Ҫ�ɷ���Al2O3��������������Fe2O3��SiO2���������ʺ��Բ��ƣ����Ʊ��þ�ˮ�����乤���������£�
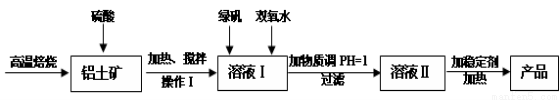
��1��H2SO4Ũ�ȵ����˷�Χ��45%~50%����Ӧ�������¶���100�棬��Ŀ���ǣ� ��Al2O3��H2SO4��Ӧ�Ļ�ѧ��Ӧ����ʽ��__________��
��2������IΪ����ȴ���á� ��ϴ�ӣ����õ�����ҺI�еĽ�����������_______���ѧʽ����
��3����ҺI�м����̷���FeSO4��7H2O����˫��ˮ��Ŀ���ǣ� ���漰�ķ�Ӧ���ӷ���ʽΪ _ _��
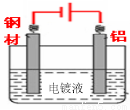
��4���ֲĶ��������γɵ�����������Ĥ�ܷ�ֹ�ֲĸ�ʴ�����ڴ������ɸֲĶ�����װ��ʾ��ͼ��������Ӧ��ע��
(16��)��1������������Ľ����ʣ�2�֣��������֣���Al2O3 + 3H2SO4 ��Al2(SO4)3 + 3H2O��3�֣� ��
��2�����ˣ�2�֣���Al3+��Fe3+��2�֣�
��3������n(Fe3+)��2�֣���H2O2 + 2Fe2+ +2H+ ��2H2O + 2Fe3+��3�֣�
��4������ͼ��ʾ��2�֣��缫��ע��ȷ1�֣���Դ��ע��ȷ1�� ��
��������
�����������1���ʵ���������Ũ�Ⱥ��¶ȣ����Լӿ췴Ӧ���ʣ�����������Ľ����ʣ�Al2O3��H2SO4��Ӧ�Ļ�ѧ��Ӧ����ʽ��Al2O3 + 3H2SO4 ��Al2(SO4)3 + 3H2O��
��2����ȴ���ú��й���������������һ�������ǹ��ˣ����������������������ᷴӦ���������õ�����ҺI�еĽ�����������Al3+��Fe3+��
��3��˫��ˮ���������ԣ��������Ӿ��л�ԭ�ԣ����߷�Ӧ���������ӣ����������Һ�������ӵ����ʵ������������Ʊ�����������Ӧ�����ӷ���ʽΪH2O2 + 2Fe2+ +2H+ ��2H2O + 2Fe3+��
��4�����ʱ���ƽ������������Ʋ���������������Դ����������������ڸֲĶ�������װ��ͼ�ɱ�ʾΪ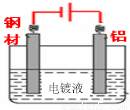 ��
��
���㣺���������Ʊ���������ͼ���������ԭ��Ӧ�õ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014�^����ʡ�߶���һѧ�����п����Ŀƻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
������������������
A����������Ҫ�ɷ�����֬
B����֬���ɸ�֬������������ɵ���
C��øҲ��һ�ֵ�����
D�������ʵ���Է�������ͨ���ܴ��е������ﵽ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�^����ʡ�߶���ѧ�ڵ�һ�νβ��Ի�ѧ��B���Ծ��������棩 ���ͣ�ѡ����
���ڷ��ȷ�Ӧ ������˵����ȷ����
������˵����ȷ����
A������H20�����е����������ڷ�Ӧ��H2��O2�����е�������
B����Ӧ��H2��O2�����е����������ڲ���H2O�����е�������
C����Ӧ��H2��O2�����е����������ڲ���H2O�����е�������
D����Ӧ��H2��02���е��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��㶫ʡ�����и���һģ���ۻ�ѧ�Ծ��������棩 ���ͣ������
��16�֣���Ԫ�صĻ�����Ӧ��ʮ�ֹ㷺����ش�
��1�����ȼ��Һ̬ƫ�����£�C2H8N2������Һ̬N2O4�������������߷�Ӧ�ų��������ȣ�������������Ⱦ�������ˮ����֪�����£�1 gȼ����ȫȼ���ͷų�������Ϊ42.5kJ����÷�Ӧ���Ȼ�ѧ����ʽΪ ��
��2��298 Kʱ����2L�̶�������ܱ������У��������淴Ӧ��2NO2(g) N2O4(g) ��H��-a kJ��mol��1 (a>0) ��N2O4�����ʵ���Ũ����ʱ��仯��ͼ����ƽ��ʱ��N2O4��Ũ��ΪNO2��2�����ش��������⣺
N2O4(g) ��H��-a kJ��mol��1 (a>0) ��N2O4�����ʵ���Ũ����ʱ��仯��ͼ����ƽ��ʱ��N2O4��Ũ��ΪNO2��2�����ش��������⣺

��298kʱ���÷�Ӧ��ƽ�ⳣ��Ϊ L ��mol��1����ȷ��0.01����
������������Ǵ���ƽ��״̬���� ��
A.���������ܶȱ��ֲ��䣻 B.����������ɫ���ٱ仯�� C.��ѹ�㶨ʱ��
������Ӧ��398K���У�ijʱ�̲��n(NO2)=0.6 mol n(N2O4)=1.2mol�����ʱV������ V���棩���>������<����=������
��3��NH4HSO4�ڷ����Լ���ҽҩ�����ӹ�ҵ����;�㷺������100 mL 0.1 mol��L��1NH4HSO4��Һ�еμ�0.1 mol��L��1NaOH��Һ���õ�����ҺpH��NaOH��Һ����Ĺ�ϵ������ͼ��ʾ��

�Է���ͼ��a��b��c��d��e����㣬
��b��ʱ����Һ�з���ˮ�ⷴӦ��������______��
����c�㣬��Һ�и�����Ũ���ɴ�С������˳���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��㶫ʡ�����и���һģ���ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��д��ȷ����
A����CaCl2��Һ��ͨ��������CO2�� Ca2��+CO2+H2O==CaCO3��+2H��
B����̼�������Һ�м����������������Һ��HCO3�� + OH��==CO32��+ H2O
C����AlCl3��Һ�м��������Ũ��ˮ��Al3++4NH3��H2O=A1O2-+4NH4++2H2O
D����Ba(OH)2��Һ�м���������NaHSO3��Һ��HSO3��+Ba2��+OH-==BaSO3��+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��㶫ʡտ���б�ҵ����в������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͼ��ʵ�����о���ˮ����բ��ͬ��λ��ʴ���������ͼ������˵����ȷ����
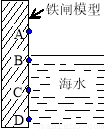
A���õ绯��ʴΪ���ⸯʴ
B��ͼ����������������C����
C��A�����B�������ʴ
D����բ�еĸ����ĵ缫��Ӧ��Fe-2e�� = Fe2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��㶫ʡտ���и�����һ���¿����ۻ�ѧ�Ծ��������棩 ���ͣ������
�Ի�����Ϊԭ��������������������к�Fe2O3��SiO2��Al2O3��MgO�ȡ�ʵ����ģ�ҵ���������Ʊ�����(Fe2O3)���������£�
��1���������ijɷ�������������������� �� д�����ܹ���Fe2O3��ϡ���ᷴӦ�����ӷ�Ӧ����ʽ�� ��
��2�����������У�Ϊ��ȷ������Ĵ��ȣ�����������Ҫ������Һ��pH�ķ�Χ��_________��������������������������ʽ����ʱ��Һ��pH���±���
������ | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
��ʼ���� | 2.7 | 3.8 | 7.5 | 9.4 |
��ȫ���� | 3.2 | 5.2 | 9.7 | 12.4 |
��3������A����Ҫ�ɷ�Ϊ ����ҺB���Ի��յ�������Na2SO4��MgSO4��___________��
��4����֪����������Ϊw kg�����������Ʊ������У���Ԫ�����25%�����յõ����������Ϊm kg����ԭ������������Ԫ����������Ϊ ��������������ʽ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��㶫ʡտ���и�һ��һѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NA��ʾ����ӵ�����������˵����ȷ����
A��1 mol Cl2��Ϊ�������õ��ĵ�����ΪNA
B����0�棬101 kPaʱ��22.4 L�����к���NA����ԭ��
C��14 g�������7NA������
D��NA��һ����̼���Ӻ�0.5 mol�����������Ϊ7��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�γ��С��������и�һ��ѧ������������ѧ�Ծ��������棩 ���ͣ�ѡ����
���������У������������ȵ���
A������ƿ B�������� C��������ƿ D���Թ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com