
(15分)下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
|
族 周期 |
IA |
|
0 |
|||||
|
1 |
|
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
|
2 |
|
|
|
① |
⑧ |
② |
|
|
|
3 |
③ |
④ |
⑤ |
⑥ |
⑦ |
|
|
|
(1)②、④、⑤的原子半径由大到小的顺序为____________________。
②、④、⑤的离子半径由大到小的顺序为____________________。
(2)①②⑥⑦四种元素所对应的气态氢化物最稳定的是________,最不稳定的是_____(填化学式)。
(3) ②、③可形成既含离子键又含共价键的化合物,其阳离子和阴离子的个数比为_____。
(4)③、⑤两元素最高价氧化物对应水化物发生反应的离子方程式为__________________________。
(5)工业上用①单质大量生产⑥单质,反应的化学方程式为_______________________________。
(6)④⑤两元素相比较,金属性较强的是 (填名称),用原子结构知识解释 ,可以验证该结论的实验是 (填编号)。
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将形状、大小相同的这两种元素的单质分别和同浓度的盐酸反应
(c)将形状、大小相同的这两种元素的单质分别和热水作用,并滴入酚酞溶液
(d)分别往氯化镁溶液、氯化铝溶液中逐滴滴入氢氧化钠溶液直到过量。
(7)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
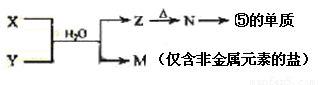
X溶液与Y溶液反应的离子方程式为____________ _________,
(1)(各1分) Mg Al O, O2- Mg2+ Al3+(2)(各1分) H2O ,SiH4
(3)(1分)2:1(4)(2分) Al(OH)3+OH-=[Al(OH)4]-
(5)(2分) C+SiO2
 2CO↑+Si
2CO↑+Si
(6)(1+1 +2分)镁 ,镁原子半径比铝原子半径大,原子核对外层电子吸引能力较弱,失电子能力较强,bcd(7)(2分) Al3++3NH3·H2O=Al(OH)3↓+3NH4+
【解析】各种元素分别为C 、O 、 Na、Mg、Al、Si、P,金属性最强的为钠,非金属性最强的为氧。同一周期中从前到后原子半径逐渐变小,最外层排布相同的核电荷数越多半径越小。Al(OH)3+OH-=[Al(OH)4]-
(2分) C+SiO2  2CO↑+Si
2CO↑+Si


科目:高中化学 来源: 题型:
| a | |||||||||||||||||
| f | y | h | i | ||||||||||||||
| b | e | j | |||||||||||||||
| c | d | g | l | ||||||||||||||




查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 族 周期 |
IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||





查看答案和解析>>
科目:高中化学 来源: 题型:



查看答案和解析>>
科目:高中化学 来源: 题型:
| 族周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |


查看答案和解析>>
科目:高中化学 来源: 题型:
| 第一周期 | 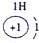 |
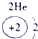 | ||||||
| 第二周期 | 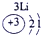 |
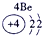 |
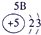 |
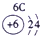 |
 |
 |
 |
 |
| 第三周期 | 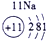 |
 |
 |
 |
 |
 | ||
 表示的是
表示的是查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com