
【题目】下列各组中的物质均既能发生加成反应又能发生取代反应的是( )
A.乙烷与乙烯B.苯和油酸甘油酯
C.乙醇和乙酸D.聚乙烯和溴乙烷
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
【题目】(1)丁烯是一种重要的化工原料,可由丁烷催化脱氢制备。回答下列问题:
正丁烷(C4H10)脱氢制1-丁烯(C4H8)的热化学方程式如下:
①C4H10(g)= C4H8(g)+H2(g) ΔH1
已知:②C4H10(g)+![]() O2(g)= C4H8(g)+H2O(g) ΔH2=119 kJ·mol1
O2(g)= C4H8(g)+H2O(g) ΔH2=119 kJ·mol1
③H2(g)+ ![]() O2(g)= H2O(g) ΔH3=242kJ·mol1
O2(g)= H2O(g) ΔH3=242kJ·mol1
反应①的ΔH1为________kJ·mol1。
(2)检验硫酸铁溶液中是否存在Fe2+的方法是_______________________________。
(3)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2= 2Na2FeO4+2Na2O+2Na2SO4+O2↑
该反应中的还原剂是_____________,每生成l mol Na2FeO4转移________mol电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液的物质的量浓度的计算正确的是( )
A. V L Fe2(SO4)3 溶液中含Fe3+ m g,溶液中c(SO42—) 是![]() mol·L-1
mol·L-1
B. 将100 mL 1.5 mol·L-1的NaCl溶液与200 mL 2.5 mol·L-1的NaCl溶液混合(忽略溶液体积变化),得到溶液的物质的量浓度为2 mol·L-1
C. 实验室配制480 mL 0.1 mol·L-1的硫酸铜溶液,应选取500 mL容量瓶,称取12.5 g胆矾配成500 mL溶液
D. 标准状况下,a L NH3溶于1000 g水中,得到的溶液密度为b g·cm-3,则该溶液的物质的量浓度为![]() mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数。已知C2H4和C3H6的混合物的质量为a g,则该混合物中
(1)所含共用电子对数目为____。
(2)所含碳氢键数目为_______。
(3)燃烧时消耗的O2标准状况下体积_______________ L。
(4)所含原子总数为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C、D在周期表中位置如图所示,其中元素D原子最外层有3个电子。请用相应的化学用语回答:
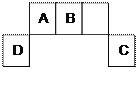
(1)A与氢元素可以形成很多化合物,在这些化合物中都含有_________(选填“共价”或“离子”)键;与C相邻且最外层电子比C少1个的离子结构示意图为 _________________。B在元素周期表中位于____________________。B、C、D形成的离子的半径由大到小依次为 _________________。(填相应的离子符号)
(2)元素A形成的最简单氢化物和氧气在KOH溶液中可构成燃料电池,该电池工作时正极的电极反应式为 ___________________________________。
(3)D的最高价氧化物的水化物与NaOH反应的化学方程式是:
________________________________________。
(4)由A与S形成的液态化合物AS2 0.2mol在O2中完全燃烧,生成两种气态氧化物,298K时放出热量215 kJ。 该反应的热化学方程式为_________________________________。
(5)已知298K时,Fe(s) + ![]() O2(g) == FeO(s) ; ΔH= -272.0 kJ · mol-1
O2(g) == FeO(s) ; ΔH= -272.0 kJ · mol-1
2D(s) + ![]() O2(g) == D2O3(s) ; ΔH= -1675.7 kJ · mol-1
O2(g) == D2O3(s) ; ΔH= -1675.7 kJ · mol-1
写出D单质和FeO反应的热化学方程式是_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应3H2 + N2 2NH3的叙述不正确的是( )
A. 该反应是可逆反应
B. 反应方程式中 “”表示在相同条件下,反应可以同时向正逆两个方向进行
C. 1mol的N2与3mol的H2混合反应,可生成2molNH3
D. 在该反应中H2作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+.为了减少污染变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜.请根据流程图,填写物质名称(或主要成分的化学式)或操作方法,完成回收硫酸亚铁和铜的简单实验方案.

(1)A是______B是_______
(2)操作Ⅱ是_____操作Ⅲ是______。
Ⅱ.松花蛋于明朝初年问世,其腌制配方有多种,但主要配料为生石灰、纯碱和食盐。将一定比例的配料用水和黏土调成糊状,敷于蛋上,密封保存,数日后可食用。
(1)腌制松花蛋的配料用水调制时,主要发生的化学反应的方程式有(不考虑黏土中物质可能参与的反应)___________________、_____________________。
(2)松花蛋外的糊状物经溶解、过滤后,滤液中肯定含有的溶质为________和_______,可能含有的溶质为Ca(OH)2或Na2CO3。
(3)某同学设计下表的实验方案,探究(2)所得滤液中可能含有的物质是否存在,请你帮他完善实验方案。
实验步骤 | 实验现象 | 实验结论 |
①取少量滤液,滴加适量K2CO3溶液 | 若出现白色沉淀 | 滤液中含Ca(OH)2 |
若无白色沉淀 | 滤液中无Ca(OH)2 | |
②取少量滤液,________ | 若出现________ | 滤液中含Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,某溶液中由水电离出来的c(H+)=1×10-4mol/L,该溶液可能是
①二氧化硫水溶液;②氯化铵水溶液;③醋酸钠水溶液;④氢氧化钠水溶液
A.①④B.①②C.②③D.③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com