
| A. | Ag+→Ag | B. | Fe3+→Fe2+ | C. | H+→H2 | D. | Fe(OH)2→Fe(OH)3 |
分析 A、银离子与铁粉发生氧化还原反应;
B、铁离子与单质铁发生归中反应;
C、铁与非氧化性的酸发生氧化还原反应;
D、氢氧化亚铁转化为氢氧化铁是发生氧化反应,而铁是还原剂,所以氢氧化亚铁与铁不反应.
解答 解;A、银离子与铁粉发生氧化还原反应,如铁与硝酸银溶液反应生成单质银,故A不选;
B、铁离子与单质铁发生归中反应,铁与氯化铁反应生成氯化亚铁,故B不选;
C、铁与非氧化性的酸发生氧化还原反应,铁与盐酸反应生成氯化亚铁与氢气,故C不选;
D、氢氧化亚铁转化为氢氧化铁是发生氧化反应,而铁是还原剂,所以氢氧化亚铁与铁不反应,所以不能实现,故D选;
故选D.
点评 本题考查氧化还原反应和铁的化学性质,学生要清楚氢氧化亚铁转化为氢氧化铁是发生氧化反应,应添加氧化剂,而 铁是还原剂,比较容易.


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:推断题
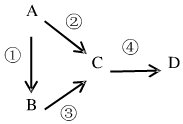 A、B、C、D均为中学化学常见物质,且均含有同一种元素,它们之间有如图转化关系,其中A是单质.
A、B、C、D均为中学化学常见物质,且均含有同一种元素,它们之间有如图转化关系,其中A是单质.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化铁通常用作红色油漆和涂料 | |
| B. | 用铝制餐具长期存放碱性食物 | |
| C. | 过氧化钠可以用作潜水艇里氧气的来源 | |
| D. | 硅可用于制作电脑芯片 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 28% | B. | 56% | C. | 72% | D. | 80% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化剂为KMnO4,其中Cl元素被还原 | |
| B. | 若有0.8molH2O生成,则反应中有NA个电子转移 | |
| C. | 浓HCl在反应中起酸性和还原性的作用 | |
| D. | 由此反应可以大胆推测氧化性强弱关系:KMnO4>MnO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 原子半径:A<B<C | |
| B. | A的氢化物的稳定性大于C的氢化物的稳定性 | |
| C. | A的最高价氧化物与B的单质可以发生置换反应 | |
| D. | C的氧化物的熔点比A的氧化物熔点低 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
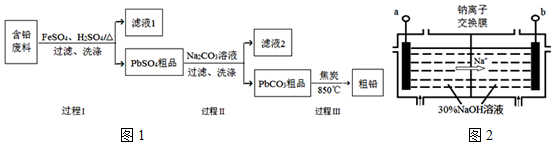
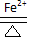 2PbSO4+2H2O.
2PbSO4+2H2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com