
| A. | 铜属于重金属,但其盐有毒,所以铜质器皿不安全,应该禁用 | |
| B. | 燃煤中加入生石灰可以减少二氧化硫的排放 | |
| C. | 明矾和漂白粉常用于自来水的处理,两者的作用原理相同 | |
| D. | 钠在空气和氯气中燃烧,火焰颜色和生成固体颜色都不 |
分析 A.可溶性铜盐能够使蛋白质变性,铜单质无毒;
B.二氧化硫能够与生石灰反应生成亚硫酸钙,亚硫酸钙氧化生成硫酸钙;
C.明矾水解生成的氢氧化铝胶体具有吸附性,漂白粉中次氯酸根离子具有氧化性;
D.焰色反应属于元素物理性质.
解答 解:A.可溶性铜盐能够使蛋白质变性,铜单质无毒,所以铜质器皿安全,故A错误;
B.燃煤中加入生石灰可以使燃烧产生的二氧化硫转化为硫酸钙,减少二氧化硫的排放,故B正确;
C.明矾只能净水,漂白粉能够杀菌消毒,二者原理不同,故C错误;
D.焰色反应属于元素物理性质,钠在钠在空气和氯气中燃烧,火焰颜色相同,在空气中生成淡黄色固体,在氯气中生成白色固体,故D错误;
故选:B.
点评 本题考查物质的性质和用途,为高频考点,性质决定用途,把握物质的性质及化学与生活的联系为解答的关键,注重学科知识的综合及化学知识应用,注意焰色反应为元素的性质,题目难度不大.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对因胃酸过多而导致胃部严重溃疡的病人不可使用含有碳酸氢钠的药物治疗 | |
| B. | 淀粉、纤维素水解的最终产物都是葡萄糖 | |
| C. | 误食了重金属离子,应立即喝大量牛奶来缓解毒性 | |
| D. | R表示非处方药,OTC表示处方药 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热 | |
| B. | 滴加少量的CuSO4溶液 | |
| C. | 不用稀硫酸,改用更多的18mol/L硫酸溶液 | |
| D. | 不用铁片,改用铁粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
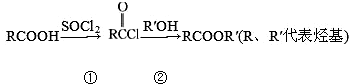 ,①②两步的产率均可达到90%以上,而RCOOH直接转化为RCOOR′产率在 60%左右,则下列说法不正确的是( )
,①②两步的产率均可达到90%以上,而RCOOH直接转化为RCOOR′产率在 60%左右,则下列说法不正确的是( )| A. | ①②两步均为取代反应 | |
| B. | ①②总产率比羧酸直接与醇反应产率高 | |
| C. | SOCl2若与足量羧酸反应产物除了 外,还有硫酸 外,还有硫酸 | |
| D. | SOCl2可以和水反应,故①反应不能用醋酸水溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能加大反应速率、促进平衡向三氧化硫的方向移动 | |
| B. | 能提高二氧化硫的利用率、使原料不被浪费 | |
| C. | 能提高三氧化硫的平衡浓度 | |
| D. | 加大正逆反应速率,缩短达到平衡的时间 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com