
【题目】现取m克铝镁合金与一定浓度的稀硝酸恰好完全溶解(假定硝酸的还原产物只有NO),向反应后的混合溶液中滴加bmol/LNaOH溶液,当滴加到VmL时,得到沉淀质量恰好为最大值n克,则下列有关该实验的说法中不正确的是 ( )
A. 沉淀中氢氧根的质量为(n-m)克
B. 恰好溶解后溶液中的NO3-离子的物质的量为![]() mol
mol
C. 生成标准状况下NO气体的体积为![]() L
L
D. 与合金反应反应的硝酸的物质的量为(![]() +
+![]() )mol
)mol
【答案】C
【解析】A、沉淀为氢氧化铝和氢氧化镁,沉淀质量等于铝镁合金质量与氢氧根质量之和,所以沉淀中氢氧根的质量为(n-m)克,A正确;B、恰好溶解后溶液中的NO3-离子的物质的量等于沉淀质量最大时溶液中NO3-离子的物质的量,当沉淀量最大时,溶液中的溶质只有硝酸钠(NaNO3),硝酸根离子与钠离子的物质的量相等,n(NO3-)=n(Na+)=n(NaOH)=![]() mol,B正确;C、根据以上分析可知沉淀中,氢氧根的物质的量等于Mg2+、Al3+所带电荷的物质的量,也等于合金失去电子的物质的量,即为反应过程中转移的电子,n(e-)=n(OH-)=
mol,B正确;C、根据以上分析可知沉淀中,氢氧根的物质的量等于Mg2+、Al3+所带电荷的物质的量,也等于合金失去电子的物质的量,即为反应过程中转移的电子,n(e-)=n(OH-)=![]() mol,根据电子守恒原理,生成NO时,HNO3中+5价的N原子得3个电子,因此生成NO的物质的量应该是转移电子的三分之一,即
mol,根据电子守恒原理,生成NO时,HNO3中+5价的N原子得3个电子,因此生成NO的物质的量应该是转移电子的三分之一,即![]() mol×
mol×![]() =
=![]() mol,其体积在标准状况下为
mol,其体积在标准状况下为![]() L,C错误;D、参加反应的硝酸有两种作用,起酸和氧化剂作用,作为酸的硝酸(生成硝酸盐)的物质的量等于硝酸钠的物质的量为
L,C错误;D、参加反应的硝酸有两种作用,起酸和氧化剂作用,作为酸的硝酸(生成硝酸盐)的物质的量等于硝酸钠的物质的量为![]() mol,作氧化剂的硝酸的物质的量等于NO的物质的量为
mol,作氧化剂的硝酸的物质的量等于NO的物质的量为![]() mol,所以与合金反应的硝酸的物质的量为(
mol,所以与合金反应的硝酸的物质的量为(![]() +
+![]() )mol,D正确;答案选C。
)mol,D正确;答案选C。


科目:高中化学 来源: 题型:
【题目】某新型电池,以NaBH4(B的化合价为+3价)和H2O2作原料,负极材料采用Pt,正极材料采用MnO2(既作电极材料又对该极的电极反应具有催化作用),该电池可用作卫星、深水勘探等无空气环境电源,其工作原理如图所示。下列说法不正确的是

A. 每消耗3mol H2O2,转移6mol e﹣
B. 电池工作时Na+从b极区移向a极区
C. a极上的电极反应式为:BH4﹣+8OH﹣﹣8e﹣═BO2﹣+6H2O
D. b极材料是MnO2,该电池总反应方程式:NaBH4 + 4H2O2===NaBO2 + 6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验装置的说法中正确的是( )
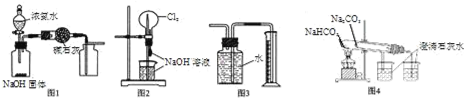
A. 图1装置可制取、收集干燥纯净的NH3
B. 图2装置可以完成“喷泉”实验
C. 图3装置可测量Cu 与浓硝酸反应产生气体的体积
D. 图4装置可用比较NaHCO3和Na2CO3的热稳定性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲苯是有机化工生产的基本原料之一。利用乙醇和甲苯为原料,可按下列路线合成分子式均为C9H10O2的有机化工产品E和J。
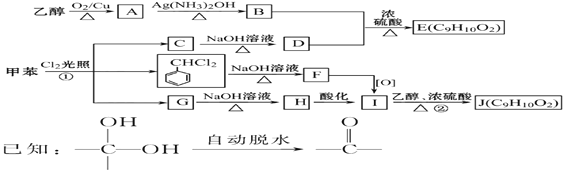
请回答:
(1)①的反应类型为_________________; J的官能团名称是_______________;
(2)D的化学名称是_________________________, F的结构简式为__________________________。
(3)写出下列反应方程式
①乙醇→A: ________________________________________________________。
② C→D:________________________________________________________。
③B+D→E: _____________________________________________________。
④G→H:________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设阿伏加德罗常数的值为NA,下列结论错误的是 ( )
A. 完全电解2 mol H2O断裂的σ键键数为4NA
B. 标准状况下,11.2 L CO2中含有的π键键数为2NA
C. 60 g SiO2晶体中含有的Si—O键键数为4NA
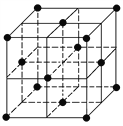
D. 128 g金属铜中含有如图所示的晶胞数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关从海带中提取碘的实验原理和装置能达到实验目的的是
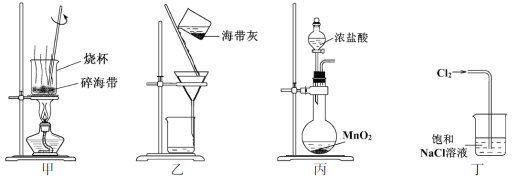
A. 用装置甲灼烧碎海带
B. 用装置乙过滤海带灰的浸泡液
C. 用装置丙制备用于氧化浸泡液中I的Cl2
D. 用装置丁吸收氧化浸泡液中I后的Cl2尾气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ某溶液中只可能含有Fe2+、Mg2+、Cu2+、NH4+、Al3+、Cl-、OH-、CO32-。当加入一种淡黄色固体并加热时,有刺激性气体放出和白色沉淀产生,加入淡黄色固体的物质的量(横坐标)与析出的沉淀和产生气体的物质的量(纵坐标)的关系如下图所示。该淡黄色物质做焰色反应实验显黄色。可知溶液中含有的离子是________________;所含离子的物质的量浓度之比为____________;所加的淡黄色固体是______________。
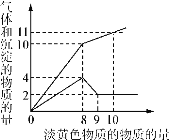
Ⅱ.实验室采用滴定法测定某水样中亚硫酸盐含量:

(1)滴定时,KIO3和KI作用析出I2,完成并配平下列离子方程式:__IO3-+____I-+____===____I2+____H2O。
(2)反应(1)所得I2的作用是_________________________。
(3)滴定终点时,100mL的水样共消耗x mL标准溶液。若消耗1mL标准溶液相当于SO32-的质量1g,则该水样中SO32-的含量为________mg·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质能满足如图所示转化关系的是(图中箭头表示进一步转化)
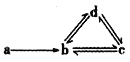
a | b | c | d | |
① | Si | SiO2 | H2SiO3 | Na2SiO3 |
② | Al | AlCl3 | NaAlO2 | Al(OH)3 |
③ | Cu | CuO | Cu(OH)2 | CuSO4 |
④ | Fe2O3 | FeCl3 | FeCl2 | Fe |
A. ①② B. ②③ C. ③④ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从某些反应看,NH3和H2O、NH4+和H3O+、NH![]() 和OH-、N3-和O2-两两类似。据此判断下列反应正确的是
和OH-、N3-和O2-两两类似。据此判断下列反应正确的是
①CaO+2NH4Cl===CaCl2+2NH3↑+H2O ②2Na+2NH3===2NaNH2+H2↑
③3Mg(NH2)2===Mg3N2+4NH3↑ ④NH4Cl+NaNH2===NaCl+2NH3↑
A. 只有③ B. 只有① C. ①和② D. 都正确
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com