
 ��1����ҵ�Ͽ�����CO2��H2�����״�������ʽ���£�
��1����ҵ�Ͽ�����CO2��H2�����״�������ʽ���£����� ����1����CO2��g��+3H2��g��?CH3OH��l��+H2O ��g����H=Q1kJ•mol-1
��CH3OH��l��+$\frac{1}{2}$O2��g��?CO2��g��+2H2��g����H=Q2kJ•mol-1
��H2O��g��=H2O��l����H=Q3kJ•mol-1�����ݸ�˹���ɢ١�2+�ڡ�3+�ۡ�2����õ���
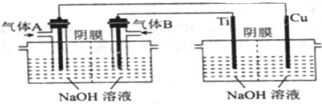
��2���ٵ�����ͭΪ������AΪԭ��ص�������
��ԭ����У����������ƶ������ص�������ͭ�缫���������ɸ���������Χ�ļ��Ի���������������д�缫��Ӧʽ��
�۵����з������ܷ�ӦʽΪ2Cu+H2O$\frac{\underline{\;���\;}}{\;}$Cu20+H2�������ݵ��ʲô��ʲô��ԭ��֪��Ҫ��������ʣ�
��ȼ�ϵ�����ĵ����������������������ܽ�ͭ��ͬʱ�õ���������֪��ѭ�����õ�����Ϊ������
��� �⣺��1����CO2��g��+3H2��g��?CH3OH��l��+H2O ��g����H=Q1kJ•mol-1
��CH3OH��l��+$\frac{1}{2}$O2��g��?CO2��g��+2H2��g����H=Q2kJ•mol-1
��H2O��g��=H2O��l����H=Q3kJ•mol-1�����ݸ�˹���ɢ١�2+�ڡ�3+�ۡ�2�õ���
��ʾ�״���ȼ���ȵ��Ȼ�ѧ����ʽΪ��CH3OH��l��+$\frac{3}{2}$O2��g���TCO2��g��+2H2O��l����H=��2Q1+3Q2+2Q3�� kJ•mol-1��
��2����ȼ�ϵ��ͨ�����ļ�Ϊ���������ӵ���������ͭ�缫���ļ�Ϊ��ȷ����֪����AΪ�������ʴ�Ϊ��O2��
��ԭ��������������ƶ�����ȼ�ϵ����OH-���ƶ�����Ϊ�������ң�����������ͭ���������缫��ӦʽΪ2Cu+2OH--2e-=Cu2O+H2O���ʴ�Ϊ���������ң�2Cu+2OH--2e-=Cu2O+H2O��
�۵����ڷ������ܷ�ӦʽΪ2Cu+H2O$\frac{\underline{\;���\;}}{\;}$Cu20+H2������֪��Ҫ�����������ˮ���ʴ�Ϊ��H2O��
�ܵ��������õ��������ɲ���ȼ�ϵ�����ĵ��������ɼ���ѭ��������Ϊ�������ʴ�Ϊ��H2��
���� ���⿼���˹���ɡ��绯ѧ���ۣ���Ŀ�Ѷ��еȣ���ȷ��Ӧ�����ǽ���Ĺؼ����������ȡ��ַ���𣬼�����̣�ע����ѧϰ�й����ܽᣮ


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ΪNA��NO2��CO2��������к��е���ԭ����Ϊ2NA | |
| B�� | 100g��������Ϊ98%��Ũ������������ԭ����Ϊ4NA | |
| C�� | ���³�ѹ�£�92gNO2N2O4�Ļ�����庬�е�ԭ����Ϊ6NA | |
| D�� | 44gN2O��CO2��ɵĻ�������к���NA������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ư�۵���Ч�ɷ���CaCl2 | |
| B�� | Ư�ۺ�������������ˮ��ԭ������ͬ�� | |
| C�� | Ư������������Ի�����ʹ�� | |
| D�� | Ư�������ڿ������������ܷⱣ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
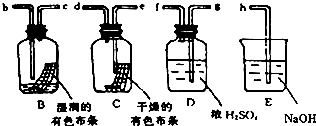
| ����� | �ܵ�������� | ����� | �ܵ����H+������ |
| ���ڸ�������� | a��g��h | b��c��e��f��h | b��c��g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Pt�缫���������MgCl2��Һ��2H2O+2Cl-$\frac{\underline{\;���\;}}{\;}$H2��+Cl2��+2OH- | |
| B�� | H${\;}_{2}^{18}$O��Ͷ��Na2O2���壺2H${\;}_{2}^{18}$O+2O${\;}_{2}^{2-}$�T4OH-+18O2�� | |
| C�� | Ca��HCO3��2��Һ������NaOH��Һ��Ӧ��HCO3-+Ca2++OH-�TCaCO3��+H2O | |
| D�� | FeSO4��Һ�м�H2O2��Һ��Fe2++2H2O2+4H+�TFe3++4H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| 25��ƽ����ϵ | HA��ʼ��Ũ�� |
| ��ˮ�У�HA�TH++A- | 4.0��10-3mol•L-1 |
| �ڱ��У�2HA�T��HA��2 | 5.0��10-3mol•L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com