
工业上为了使原料和能量得到充分的利用,常常采用循环操作。
Ⅰ、利用热化学循环制氢能缓解能源矛盾。最近研究发现,复合氧化物铁酸锰(MnFe2O4)可用于热化学循环分解水制氢。
MnFe2O4的制备:
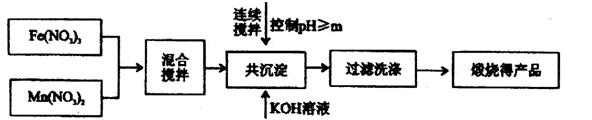
| 开始沉淀 | 完全沉淀 | |
| Fe3+ | 2.7 | 3.7 |
| Mn2+ | 8.3 | 10.4 |
已知Fe3+、Mn2+沉淀的pH如右表所示。
(1)此工艺中理论上投入原料Fe(NO3)3和Mn(NO3)2的物质
的量之比应为 __________。
(2)控制pH的操作中m的值为 。
Ⅱ、用MnFe2O4热化学循环制取氢气:
![]()
![]()
(3)由上可知,表示H2燃烧热的热化学方程式是__________________________ 。
(4)该热化学循环制取氢气的优点是_______________(填字母编号)。
A.过程简单、无污染
B.物料可循环使用
C.氧气和氢气在不同步骤生成,安全且易分离
Ⅲ、工业上可用H2、HCl在一定条件下通过下图的循环流程制取太阳能材料高纯硅。

(5)上图中,假设在每一轮次的投料生产中,硅元素没有损失,反应①中HCl的利用率和反应②中H2的利用率均为75%。则在下一轮次的生产中,需补充投入HCl和H2的体积比是___________________。
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
未来的交通工具将采用新一代无机非金属材料制成的无水冷发动机。这类材料中研究得较多的是化合物G。
(1)化合物G的相对分子质量为140,G中硅元素的质量分数为60%,另有元素Y。G可以由化合物E(含两种元素)与NH3反应而生成,同时产生HCl气体。请推断:①化合物G的化学式为__________________。②由1 mol NH3和0.75 mol E恰好完全反应,化合物E的分子式为_______________________。
(2)粉末状G能够与空气中的氧气和水作用,所得产物中都有一种酸性氧化物,它是工业上生产玻璃、水泥、陶瓷的主要原料。与氧反应所得的产物还有一种单质;与水反应生成另一种产物是该种单质元素的氢化物。请写出化合物G与水反应的化学方程式_______________________________________________________________________________。
(3)为了使化合物G能成为新一代汽车发动机材料,现采用常压下在G中添加氧化铝,经高温烧结制成一种高强度、超硬度、耐磨损、抗腐蚀的陶瓷材料,它的商品名叫“赛伦”,化学通式可表示为Si6-xAlxOxY8-x。在接近于1 700 ℃时x的极限值约为4.0,在1 400 ℃时x为2.0,以保持整个化合物呈电中性。试问:①赛伦中各元素的化合价为Si_________,Al_________,O_________,Y_________。赛伦的晶体类型为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
甲醇被称为2l世纪的新型燃料,工业上通过下列反应Ⅰ和Ⅱ,用CH4和H2O为原料来制备甲醇。
(1)将1.0 mol CH4和2.0 molH2O(g)通入反应室(容积为100L),在一定条件下发生反应:
CH4(g)+H2O(g)CO(g)+3H2(g)……Ⅰ,CH4的转化率与温度、压强的关系如右图。
已知100℃时达到平衡所需的时间为5min,
①则用H2表示的平均反应速率为_ 。
②图中的P1_ _P2(填“<”、“>”或“=”),100℃时平衡常数为_ _。
③在其它条件不变时降低温度,逆反应速率将 _ _(填“增大” “减小”或“不变”)。
(2)在压强为0.1 MPa条件下,将a mol CO与 3a mol H2的混合气体在催化剂作用下能自发反应生成甲醇:CO(g)+2H2(g) CH3OH(g) ……Ⅱ。
④该反应的△H_ _0,△S_ _0(填“<”、“>”或“=”)。
⑤若容器容积不变,下列措施可增加甲醇产率的是_ _。
A.升高温度
B.将CH3OH(g)从体系中分离出来
C.充入He,使体系总压强增大
D.再充入1mol CO和3mol H2
⑥为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计的表中。
| l 实验编号 | l T(℃) | l n (CO)/n(H2) | l P(MPa) |
| l ⅰ | l 150 | l 1/3 | l 0.1 |
| l ⅱ | l _ _ | l _ _ | l 5 |
| l ⅲ | l 350 | l _ _ | l 5 |
A.请在上表空格中填入剩余的实验条件数据。
B.根据反应Ⅱ的特点,在给出的坐标图中,画出其在0.1MPa和5MPa条件下CO的转化率随温度变化的趋势曲线示意图,并标明各条曲线的压强。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
甲醇被称为2l世纪的新型燃料,工业上通过下列反应Ⅰ和Ⅱ,用CH4和H2O为原料来制备甲醇。
(1)将1.0 mol CH4和2.0 mol H2O(g)通入反应室(容积为100L),在一定条件下发生反应:
CH4(g)+H2O(g)CO(g)+3H2(g)……Ⅰ,CH4的转化率与温度、压强的关系如右图。
①已知100℃时达到平衡所需的时间为5min,
②则用H2表示的平均反应速率为_ 。图中的P1_ _P2(填“<”、“>”或“=”),
100℃时平衡常数为_ _。
③在其它条件不变时降低温度,逆反应速率将_ _(填“增大” “减小”或“不变”)。
(2)在压强为0.1 MPa条件下, 将a mol CO与 3a mol H2的混合气体在催化剂作用下能自发反应生成甲醇:CO(g)+2H2(g) CH3OH(g) ……Ⅱ。
④该反应的△H_ _0,△S_ _0(填“<”、“>”或“=”)。
⑤若容器容积不变,下列措施可增加甲醇产率的是_ _。
A.升高温度
B.将CH3OH(g)从体系中分离出来
C.充入He,使体系总压强增大
D.再充入1mol CO和3molH2
⑥为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计的表中。
| l 实验编号 | l T(℃) | l n (CO)/n(H2) | l P(MP) |
| l ⅰ | l 150 | l 1/3 | l 0.1 |
| l ⅱ | l __ | l __ | l 5 |
| l ⅲ | l 350 | l __ | l 5 |
A.请在上表空格中填入剩余的实验条件数据。
B.根据反应Ⅱ的特点,在给出的坐标图中,画出其在0.1MPa和5MPa条件下CO的转化率随温度变化的趋势曲线示意图,并标明各条曲线的压强。
查看答案和解析>>
科目:高中化学 来源:2010年江苏省高三第四次模拟考试化学试题 题型:填空题
(12分)甲醇被称为2l世纪的新型燃料,工业上通过下列反应Ⅰ和Ⅱ,用CH4和H2O为原料来制备甲醇。
(1)将1.0 mol CH4和2.0 mol H2O(g)通入反应室(容积为100L),在一定条件下发生反应:
CH4(g)+H2O(g) CO(g)+3H2(g)……Ⅰ,CH4的转化率与温度、压强的关系如右图。
CO(g)+3H2(g)……Ⅰ,CH4的转化率与温度、压强的关系如右图。

①已知100℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率为 。
②图中的P1 P2(填“<”、“>”或“=”),100℃时平衡常数为 。
③在其它条件不变的情况下降低温度,逆反应速率将 (填“增大”、“减小”或“不变”)。
(2)在压强为0.1 MPa条件下, 将a
mol CO与 3a mol H2的混合气体在催化剂作用下能自发反应生成甲醇:CO(g)+2H2(g)  CH3OH(g) ……Ⅱ。
CH3OH(g) ……Ⅱ。
④该反应的△H 0,△S 0(填“<”、“>”或“=”)。
⑤若容器容积不变,下列措施可增加甲醇产率的是 。
A.升高温度 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.再充入1mol CO和3mol H2
⑥为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
|
实验编号 |
T(℃) |
n (CO)/n(H2) |
P(MPa) |
|
ⅰ |
150 |
1/3 |
0.1 |
|
ⅱ |
|
|
5 |
|
ⅲ |
350 |
|
5 |
A.请在上表空格中填入剩余的实验条件数据。
B.根据反应Ⅱ的特点,在给出的坐标图中,画出其在0.1MPa和5MPa条件下CO的转化率随温度变化的趋势曲线示意图,并标明各条曲线的压强。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com