
一元中强酸次磷酸(H3PO2)是一种精细化工产品,下列说法正确的是()
A. 次磷酸的电离方程式为H3PO2⇌3H++PO23﹣
B. 次 磷酸中P的化合价为+1
磷酸中P的化合价为+1
C. NaH2PO2是酸式盐
D. NaH2PO2溶液显弱酸性
考点: 弱电解质在水溶液中的电离平衡.
专题: 电离平衡与溶液的pH专题.
分析: A、一元中强酸只能电离出一个氢离子;
B、根据化合价的代数和为零计算;
C、一元酸没有酸式盐;
D、NaH2PO2属于强碱弱酸盐,水解显碱性.
解答: 解:A、一元中强酸只能电离出一个氢离子,则次磷酸的电离方程式为H3PO2⇌H++H2PO2﹣,故A错误;
B、次磷酸(H3PO2)中O为﹣2价,H为+1价,则P的化合价为+1,故B正确;
C、次磷酸属于一元酸,一元酸没有酸式盐,所以NaH2PO2是正盐,故B错误;
D、NaH2PO2是次磷酸的正盐,在溶液中不能电离出氢离子,NaH2PO2属于强碱弱酸盐,水解显碱性,故D错误.
故选B.
点评: 本题以次磷酸为知识背景,考查了一元酸的电离方程式、化合价的计算、酸式盐的含义、盐的水解,题目涉及的知识点较多,侧重于基础知识应用的考查,题目难度不大.


科目:高中化学 来源: 题型:
我国第五套人民币中的一元硬币材料为钢芯镀镍,依据你所掌握的电镀原理,你认为在硬币制作时,钢芯应做()
A. 阴极 B. 阳极 C. 正极 D. 负极
查看答案和解析>>
科目:高中化学 来源: 题型:
将标准状况下的a L HCl(g)溶于1000g水中,得到的盐酸密度为b g•cm﹣3,则盐酸的物质的量浓度是()
A. 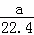 mol•L﹣1 B.
mol•L﹣1 B. 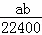 mol•L﹣1
mol•L﹣1
C. 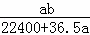 mol•L﹣1 D.
mol•L﹣1 D. 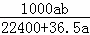 mol•L﹣1
mol•L﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
用18mol•L﹣1 浓硫酸配制100mL 3.0mol•L﹣1 稀硫酸的实验步骤如下:
①计算所用浓硫酸的体积②量取一定体积的浓硫酸 ③溶解④转移、洗涤⑤定容、摇匀
完成下列问题:
(1)所需浓硫酸的体积是 ,量取浓硫酸所用的量筒的规格是 (从下列中选用A.10mLB.25mLC.50mLD.100mL).
(2)下列情况对所配制的稀硫酸浓度有何影响?(用“偏大”“偏小”“无影响”填写)
A.所用的浓硫酸长时间放置在密封不好的容器中
B.容量瓶用蒸馏洗涤后残留有少量的水
C.所用过的烧杯、玻璃棒未洗涤
D.定容时俯视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
除去下列物质中少量杂质的方法不正确的是()
A. 除去FeCl2溶液中混有的FeCl3:加入过量铁粉,过滤
B. 除去CO2中混有的HCl:用饱和NaHCO3溶液洗气
C. 除去BaCO3固体中混有的BaSO4:加入过量的盐酸、过滤、洗涤
D. 除去甲烷中混有的乙炔:通过溴水溶液后,洗气
查看答案和解析>>
科目:高中化学 来源: 题型:
根据表中信息判断,下列选项不正确的是()
序号 反应物 产物
① KMnO4、H2O2、H2SO4 K2SO4、MnSO4
② Cl2、FeBr2 FeCl3、FeBr3
③ MnO4﹣ Cl2、Mn2+
A. 第①组反应的 其余产物为H2O和O2
其余产物为H2O和O2
B. 第②组反应中参加反应的Cl2与 FeBr2的物质的量之比为1:2
C. 第③组反应中生成1mol Cl2,转移电子2mol
D. 氧化性由强到弱顺序为MnO4﹣>Cl2>Fe3+>Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈.发生的反应体系中共有六种物质:NH4C1、FeC13、N2、Fe2O3、Fe 和X.
(1)根据题意,可判断出X是 (写化学式).
(2)写出并配平该反应的化学方程式:
(3)发生氧化反应的物质是 ,反应中4mol的氧化剂能 (填“失去”或“得到”) mol电子.
(4)反应中被氧化产生了11.2L(标准状况)的气体时,被还原的物质的质量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
一种新型燃料电池,它是用两根金属做电极插入KOH溶液中,然后向两极上分别通甲烷和氧气,下列关于此燃料电池的有关说法中错误的是()
A. 通过甲烷的电极X为电池的负极,通过氧气的电极Y为电池正极
B. 放电一段时间后,电解质溶液中KOH的物质的量改变
C. 在标准状况下,通过5.6L氧气,完全反应后有1.0mol的电子发生转移
D. 放电时,通过甲烷的一极附近的pH升高
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上合成氨气,已知通入1mol N2和3mol H2,反应过程中共放出a kJ的热量.经测定反应中N2的转化率为20%(已知:N2的转化率=实际反应的N2的量/初始充入N2的总量),则合成氨气的热化学方程式可表示为()
A. N2(g)+3H2(g)⇌2NH3 (g)△H=a kJ/mol
B. N2(g)+3H2(g)⇌2NH3 (g)△H=﹣a kJ/mol
C. N2(g)+3H2(g)⇌2NH3 (g)△H=5a kJ/mol
D. N2(g)+3H2(g)⇌2NH3(g)△H=﹣5a kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com