

 ��E��H�����������ŵ����Ʒֱ����ǻ���̼̼˫����
��E��H�����������ŵ����Ʒֱ����ǻ���̼̼˫���� +CH3CH2OH$��_{��}^{Ũ����}$
+CH3CH2OH$��_{��}^{Ũ����}$ +H2O��n
+H2O��n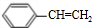 $\stackrel{����}{��}$
$\stackrel{����}{��}$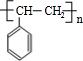 ��
�� ��д������һ�ֵĽṹ��ʽ����
��д������һ�ֵĽṹ��ʽ���� ���� C��Cl2�ڹ������������ɵ�G��GΪ±������G��NaOH��Һ���ȷ���ȡ����Ӧ����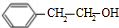 ����GΪ
����GΪ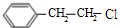 ��G������ȥ��Ӧ����HΪ
��G������ȥ��Ӧ����HΪ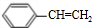 ��H�����Ӿ۷�Ӧ���ɸ߾���IΪ
��H�����Ӿ۷�Ӧ���ɸ߾���IΪ �����ƿ�֪CΪ
�����ƿ�֪CΪ ��C����������Ӧ����DΪ
��C����������Ӧ����DΪ ����A��B���ת����֪BΪ±��������B�뱽������Ӧ����C����BΪCH3CH2Br����AΪCH2=CH2��EΪCH3CH2OH��E��D����������Ӧ����FΪ
����A��B���ת����֪BΪ±��������B�뱽������Ӧ����C����BΪCH3CH2Br����AΪCH2=CH2��EΪCH3CH2OH��E��D����������Ӧ����FΪ ����Է�������Ϊ150���ݴ˽��
����Է�������Ϊ150���ݴ˽��
��� �⣺C��Cl2�ڹ������������ɵ�G��GΪ±������G��NaOH��Һ���ȷ���ȡ����Ӧ����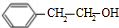 ����GΪ
����GΪ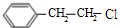 ��G������ȥ��Ӧ����HΪ
��G������ȥ��Ӧ����HΪ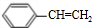 ��H�����Ӿ۷�Ӧ���ɸ߾���IΪ
��H�����Ӿ۷�Ӧ���ɸ߾���IΪ �����ƿ�֪CΪ
�����ƿ�֪CΪ ��C����������Ӧ����DΪ
��C����������Ӧ����DΪ ����A��B���ת����֪BΪ±��������B�뱽������Ӧ����C����BΪCH3CH2Br����AΪCH2=CH2��EΪCH3CH2OH��E��D����������Ӧ����FΪ
����A��B���ת����֪BΪ±��������B�뱽������Ӧ����C����BΪCH3CH2Br����AΪCH2=CH2��EΪCH3CH2OH��E��D����������Ӧ����FΪ ����Է�������Ϊ150��
����Է�������Ϊ150��
��1��������Ӧ���У��漰��Ӧ�����У�ȡ����Ӧ����ȥ��Ӧ��������Ӧ���ӳɷ�Ӧ���Ӿ۷�Ӧ��
�ʴ�Ϊ��ȡ����Ӧ����ȥ��Ӧ��������Ӧ���ӳɷ�Ӧ���Ӿ۷�Ӧ������3�֣���
������Ӧ��ȡ����Ӧ����Ϊȡ����Ӧ����Ϊȡ����Ӧ����Ϊ��ȥ��Ӧ��
��2��������������֪��C�Ľṹ��ʽΪ ��EΪCH3CH2OH�������ǻ���HΪ
��EΪCH3CH2OH�������ǻ���HΪ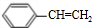 ������̼̼˫����
������̼̼˫����
�ʴ�Ϊ�� ���ǻ���̼̼˫����
���ǻ���̼̼˫����
��3����Ӧ���DZ��������Ҵ���Ӧ���ɱ�������������Ӧ����ʽΪ�� +CH3CH2OH$��_{��}^{Ũ����}$
+CH3CH2OH$��_{��}^{Ũ����}$ +H2O��
+H2O��
��Ӧ���DZ���ϩ�����Ӿ۷�Ӧ���ɾ۱���ϩ����ѧ����ʽΪ��n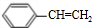 $\stackrel{����}{��}$
$\stackrel{����}{��}$ ��
��
�ʴ�Ϊ�� +CH3CH2OH$��_{��}^{Ũ����}$
+CH3CH2OH$��_{��}^{Ũ����}$ +H2O��
+H2O��
n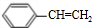 $\stackrel{����}{��}$
$\stackrel{����}{��}$ ��
��
��4��GΪ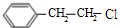 ����֤G�к�����Ԫ�صķ����ǣ�ȡ����G��NaOH��Һ��У��ټ���ϡ��������Һ�����ԣ��μ�AgNO3��Һ�����а�ɫ�������ɣ���֤��G�к�����Ԫ�أ���������Ԫ�أ�
����֤G�к�����Ԫ�صķ����ǣ�ȡ����G��NaOH��Һ��У��ټ���ϡ��������Һ�����ԣ��μ�AgNO3��Һ�����а�ɫ�������ɣ���֤��G�к�����Ԫ�أ���������Ԫ�أ�
�ʴ�Ϊ��ȡ����G��NaOH��Һ��У��ټ���ϡ��������Һ�����ԣ��μ�AgNO3��Һ�����а�ɫ�������ɣ���֤��G�к�����Ԫ�أ���������Ԫ�أ�
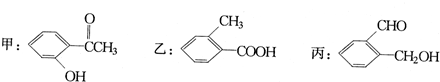
��5��F�� ����ͬ���칹���У����Ϻ��б����ṹ�����ܺ�NaHCO3��Һ��Ӧ�ų����壬˵������-COOH��������һ������Ϊ-CH2CH2COOH��-CH��CH3��COOH�����Ժ���2��������Ϊ-CH3��-CH2COOH����
����ͬ���칹���У����Ϻ��б����ṹ�����ܺ�NaHCO3��Һ��Ӧ�ų����壬˵������-COOH��������һ������Ϊ-CH2CH2COOH��-CH��CH3��COOH�����Ժ���2��������Ϊ-CH3��-CH2COOH����
-CH2CH3��-COOH�������ڡ��䡢�����֣�������3��������2��-CH3��1��-COOH��2��-CH3���ڣ�-COOH��2��λ�ã�2��-CH3��䣬-COOH��3��λ�ã�2��-CH3��ԣ�-COOH��1��λ�ã��ʷ���������ͬ���칹�干��2+6+2+3+1=14�֣����к˴Ź�����������4��壬�������Ϊ6��2��1��1���� ��
��
�ʴ�Ϊ��14�� ��
��
���� ���⿼���л����ƶϡ��л���Ӧ���͡���ѧ����ʽ����д��ʵ�鷽����ơ���������ͬ���칹�����д�ȣ�ע�����G�ķ�Ӧ�����������Ʒ������ƶϣ���Ҫѧ���������չ����ŵ�������ת������5����ͬ���칹�����Ŀ�ж�Ϊ�״��㡢�ѵ㣬�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
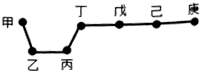 ������Ԫ�ؼס��ҡ����������졢�����������ڱ��е����λ����ͼ���ײ�һ���ڶ������������ϣ����졢���ֱ��ǿ������ؿ��к�������Ԫ�أ������ж���ȷ���ǣ�������
������Ԫ�ؼס��ҡ����������졢�����������ڱ��е����λ����ͼ���ײ�һ���ڶ������������ϣ����졢���ֱ��ǿ������ؿ��к�������Ԫ�أ������ж���ȷ���ǣ�������| A�� | ��һ���ǽ���Ԫ�� | |
| B�� | ��̬�⻯����ȶ��ԣ����������� | |
| C�� | ��������������ˮ����������ǿ | |
| D�� | �ҡ�������������������ˮ������������Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
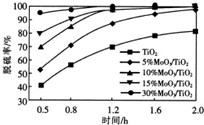 ��TiO2����MoO3����ʹ�л���R��������MoO3�����Է�Ӧ�����ʵ�Ӱ����ͼ������˵����ȷ���ǣ�������
��TiO2����MoO3����ʹ�л���R��������MoO3�����Է�Ӧ�����ʵ�Ӱ����ͼ������˵����ȷ���ǣ�������| A�� | ����MoO3����Խ��ƽ�ⳣ��Խ�� | |
| B�� | ����Ӧʱ��С��0.5h��������Ϊ0 | |
| C�� | 1.6h����MoO3����Ϊ10%��15%����������� | |
| D�� | 0.5��1.2hʱ������MoO3����Խ����������Խ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �縺�� | ���� | ���ļ��� | �е㣨ͬѹ�� |
| C��N | C=C��C-C | N-H��O-H | �״������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��ͨ������������$\frac{C��{H}^{+}��}{C��Cl{O}^{-}��}$��С | |
| B�� | ͨ������SO2����ҺƯ������ǿ | |
| C�� | ������������NaOH����Һ������ʱ��c��Na+��=c��Cl-��+c��ClO-�� | |
| D�� | ��������ˮ��ˮ�ĵ���ƽ��������Ӧ�����ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
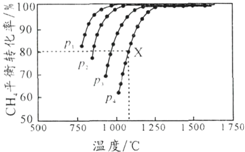 ���ܱ������г������ʵ���Ũ�Ⱦ�Ϊ 0.1mol/L��CH4�� CO2����һ�������·�����ӦCH4��g��+CO2��g��?2CO��g��+2H2��g�������CH4��ƽ��ת�������¶ȼ�ѹǿ�Ĺ�ϵ��ͼ��ʾ������˵������ȷ���ǣ�������
���ܱ������г������ʵ���Ũ�Ⱦ�Ϊ 0.1mol/L��CH4�� CO2����һ�������·�����ӦCH4��g��+CO2��g��?2CO��g��+2H2��g�������CH4��ƽ��ת�������¶ȼ�ѹǿ�Ĺ�ϵ��ͼ��ʾ������˵������ȷ���ǣ�������| A�� | ƽ��ʱCO��H2�����ʵ�����Ϊ1��1 | |
| B�� | p1��p2��p3��p4��С�����˳��Ϊp1��p2��p3��p4 | |
| C�� | 1100�棬p4�����£��÷�Ӧ10 minʱ�ﵽƽ���X����ͣ�CO2��=0.008 mol•L-1•min-1 | |
| D�� | �����¶����ߣ��÷�Ӧ��ƽ�ⳣ����С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com