
【题目】能源、环境与生产生活和社会发展密切相关。
一定温度下,在两个容积均为2 L的密闭容器中,分别发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH = -49.0 kJ·mol-1。相关数据如下:
CH3OH(g)+H2O(g) ΔH = -49.0 kJ·mol-1。相关数据如下:
容器 | 甲 | 乙 |
反应物投入量 | 1 mol CO2(g)和3 mol H2(g) | 32g CH3OH(g)和18g H2O(g) |
平衡时c(CH3OH) | c1 | c2 |
平衡时能量变化 | 放出29.4 kJ | 吸收a kJ |
(1)c1____(填“>”、“<”或“=”)c2,a=____。
(2)该反应的平衡常数表达式为K=____;若甲中反应10 s 时达到平衡,则0~10 s内甲中的平均反应速率v(H2)=______。
(3)下列情况能说明该反应一定达到平衡状态的是____(填字母)。
a. v(CO2)消耗=v(CH3OH)生成 b. 气体的密度不再随时间改变
c. CO2和CH3OH的浓度之比不再随时间改变 d. 气体的平均相对分子质量不再随时间改变
【答案】 = 19.6 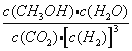 0.09 mol·L-1·s-1 cd
0.09 mol·L-1·s-1 cd
【解析】本题主要考查化学平衡的移动。
(1)容器甲、乙建立相同平衡状态,故c1=c2,a=49.0-29.4=19.6。
(2)该反应的平衡常数表达式为K=![]() ;若甲中反应10s时达到平衡,则0~10s内甲中的平均反应速率v(H2)=3mol×29.4/49.0/2.0L/10s=0.09 mol·L-1·s-1。
;若甲中反应10s时达到平衡,则0~10s内甲中的平均反应速率v(H2)=3mol×29.4/49.0/2.0L/10s=0.09 mol·L-1·s-1。
(3)a. v(CO2)消耗、v(CH3OH)生成都是正反应速率,故a不能说明该反应一定达到平衡状态;b. 气体的质量、体积不变,所以气体的密度一直保持不变,故b不能说明该反应一定达到平衡状态;c. CO2和CH3OH的浓度之比随着反应进行而改变,当CO2和CH3OH的浓度之比不再随时间改变时,说明反应达到平衡状态,故c能说明该反应一定达到平衡状态;d. 该反应气体物质的量有变化,气体质量守恒,气体的平均相对分子质量随着反应进行而改变,当气体的平均相对分子质量不再随时间改变时,说明反应达到平衡状态,故d能说明反应该反应一定达到平衡状态。故选cd。


科目:高中化学 来源: 题型:
【题目】研究化学反应的热效应有利于更好的利用化学能。下列说法正确的是( )
A.放热反应任何条件下一定能自发进行
B.升高温度可以增加分子的活化能
C.生成物总能量高于反应物总能量的反应为放热反应
D.生成物的键能总和大于反应物的键能总和的反应为放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将氢氧化钠溶液和硫酸铜溶液加入某病人的尿液中,加热时如果发现有砖红色的沉淀产生,说明该尿液中可能含有下列物质中的( )
A.醋酸B.酒精C.食盐D.葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学方程式为____________________。利用反应6NO2+8NH3![]() 7N2+12H2O也可处理NO2。当转移1.2 mol电子时,消耗的NH3在标准状况下是____L。
7N2+12H2O也可处理NO2。当转移1.2 mol电子时,消耗的NH3在标准状况下是____L。
(2)已知:2SO2(g)+O2(g)![]() 2SO3(g) ΔH = -196.6 kJ·mol-1
2SO3(g) ΔH = -196.6 kJ·mol-1
2NO(g)+O2(g)![]() 2NO2(g) ΔH = -113.0 kJ·mol-1
2NO2(g) ΔH = -113.0 kJ·mol-1
①则反应NO2(g)+SO2(g)![]() SO3(g)+NO(g)的ΔH = ____ kJ·mol-1。
SO3(g)+NO(g)的ΔH = ____ kJ·mol-1。
②一定条件下,将NO2与SO2以体积比1∶2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是____(填字母)。
A.体系压强保持不变 B.混合气体颜色保持不变
C.SO3和NO的体积比保持不变 D.每消耗1 mol SO3的同时生成1 mol NO2
③测得上述反应平衡时NO2与SO2的体积比为1∶6,则平衡常数K=____。
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)![]() CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图所示。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图所示。
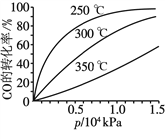
该反应的ΔH ____(填“>”或“<”)0。实际生产条件控制在250 ℃、1.3×104 kPa左右,选择此压强的理由是________________。
(4)煤燃烧产生的烟气也含氮的氧化物,用CH4催化还原NOx,可以消除氮氧化物的污染。
已知:CH4(g)+2NO2(g) ═ N2(g)+CO2(g)+2H2O(g) ΔH = -867 kJ·mol-1
2NO2(g)![]() N2O4(g) ΔH = -56.9 kJ·mol-1
N2O4(g) ΔH = -56.9 kJ·mol-1
H2O(g)![]() H2O(l) ΔH = -44 kJ·mol-1
H2O(l) ΔH = -44 kJ·mol-1
写出CH4 催化还原N2O4(g) 生成N2(g)、CO2(g) 和H2O(l)的热化学方程式:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】10g Mg、Al合金与足量100mL NaOH溶液反应,产生H2的体积为6.72L(标准状况下),求:
①合金中Al的质量分数;
②生成物NaAlO2的物质的量浓度(假设溶液体积不变)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH4++6HCHO =3H++6H2O+(CH2)6N4H+[滴定时,1 mol (CH2)6N4H+与 l mol H+相当],然后用NaOH标准溶液滴定反应生成的酸。某兴趣小组用甲醛法进行了如下实验:
步骤I 称取样品1.500 g。
步骤II 将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤III 移取25.00 mL样品溶液于250 mL锥形瓶中,加入10 mL 20%的中性甲醛溶液,摇匀、静置5 min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。
(1)根据步骤III 填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数________(填“偏高”、“偏低”或“无影响”)。
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积_______(填“偏大”、“偏小”或“无影响”)。
③滴定时边滴边摇动锥形瓶,眼睛应观察____________。
(A)滴定管内液面的变化 (B)锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由_________色变成_________色。
(2)滴定结果如下表所示:
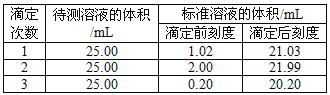
若NaOH标准溶液的浓度为0.1010 mol·L-1,则该样品中氮的质量分数为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A. Na与CuSO4溶液反应:2Na+Cu2+=2Na++Cu
B. 新制氯水中:Cl2+H2O ![]() 2H++ClO-+Cl-
2H++ClO-+Cl-
C. 200 mL 2 mol/L的FeBr2溶液中通入11.2L标准状况下的氯气:4Fe2++6Br-+5Cl2=4Fe3++3Br2+10Cl-
D. 向碳酸氢钙溶液中加入过量氢氧化钠溶液:Ca2++HCO3-+OH-= CaCO3↓+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com