
【题目】(1)在碱金属元素中,锂的金属性最弱,其原因是_______________________________________。锂在氧气中燃烧所得产物的化学键类型是________________。
(2)在周期表中,锂的性质与镁相似,预测锂在氮气中燃烧的化学方程式:__________________________。碳酸锂、硫酸锂的溶解性依次为__________、__________(填“易溶”“微溶”或“难溶”)。
(3)锂在自然界中存在的主要形式为锂辉石(LiAlSi2O6)、锂云母[Li2F2Al2(SiO3)3]等。锂辉石(LiAlSi2O6)中化合价最高的元素和锂云母[Li2F2Al2(SiO3)3]中非金属性最强的元素组成的化合物的电子式_________,它是____________(填“离子化合物”或“共价化合物”)。常温常压下,它呈_____态,原因是_____________________。
(4)四氢硼锂(LiBH4)、四氢铝锂(LiAlH4)都是重要还原剂,在有机合成中用途广泛。比较半径:r(Li+)_____r(H—),(填“>”“<”或“=”)理由是_____________________________。
【答案】在碱金属中锂原子的电子层数最少,半径最小,锂失电子能力最弱 离子键 6Li+N2![]() 2Li3N 微溶 易溶
2Li3N 微溶 易溶 ![]() 共价化合物 气 分子间作用力小 < 虽然Li+和H—的核外电子数相等,但是锂离子的质子数大于氢负离子
共价化合物 气 分子间作用力小 < 虽然Li+和H—的核外电子数相等,但是锂离子的质子数大于氢负离子
【解析】
(1)在碱金属元素中,锂的金属性最弱,其原因是在碱金属中锂原子的电子层数最少,半径最小,锂失电子能力最弱;锂为金属,与氧气反应生成氧化锂,化学键类型是离子键;
(2)锂的性质与镁相似,则与氮气反应时生成氮化锂,化学方程式为6Li+N2![]() 2Li3N;碳酸镁微溶,硫酸镁易溶,所以碳酸锂、硫酸锂的溶解性依次为微溶、易溶;
2Li3N;碳酸镁微溶,硫酸镁易溶,所以碳酸锂、硫酸锂的溶解性依次为微溶、易溶;
(3)锂辉石(LiAlSi2O6)中化合价最高的元素是Si,锂云母[Li2F2Al2(SiO3)3]中非金属性最强的元素是F,组成的化合物是SiF4,其电子式为![]() ;因为Si和F都是非金属,所以它是共价化合物;常温常压下,呈气态,原因是该物质属于分子晶体,分子间作用力小;
;因为Si和F都是非金属,所以它是共价化合物;常温常压下,呈气态,原因是该物质属于分子晶体,分子间作用力小;
(4)r(Li+)< r(H—),理由是:虽然Li+和H—的核外电子数相等,但是锂离子的质子数大于氢负离子,核电荷数越大,对核外电子吸引能力越大,半径越小。


科目:高中化学 来源: 题型:
【题目】下列离子方程式中正确的是
A. FeBr2溶液中加入等物质的量的Cl2:2Fe2+ + 2Br- + 2Cl2 = 2Fe3++Br2+4Cl-
B. 用氢氟酸在玻璃上“刻字”:SiO2 + 4H+ + 4F- = SiF4↑+ 2H2O
C. 将铜丝投入稀硝酸中:Cu + 4H+ + 2NO3-= Cu2+ + 2NO2↑+ 2H2O
D. NaOH与NH4Cl溶液混合加热:NH4+ + OH- ![]() NH3·H2O
NH3·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用图示装置制备KC1O溶液,再与KOH、Fe(NO3)3溶液反应制备髙效净水剂K2FeO4。

<査阅资料>O2与KOH溶液在20℃以下反应生成KC1O,在较高温度下则生成KC1O3;K2FeO4易溶于水,微溶于浓KOH溶液,在0℃~5℃的强碱性溶液中较稳定。
(1)仪器a的名称是___________;装置A中反应的离子方程式为___________________。
装置C中三颈烧瓶置于冰水浴中的目的是_______________。
(2)装置B吸收的气体是___________,装置D的作用是____________________。
(3)C中得到足量KC1O后,将三颈烧瓶上的导管取下,依次加入KOH溶液、Fe(NO3)3溶液,水浴控制反应温度为25℃,搅拌1.5 h,溶液变为紫红色(含K2FeO4),该反应的离子方程式为________________。再加入饱和KOH溶液,冷却至0℃~5℃析出紫黑色晶体,过滤,得到K2FeO4粗产品。
(4)K2FeO4粗产品含有Fe(OH)3、KC1等杂质,其提纯步骤为:
①将一定量的K2FeO4粗产品溶于冷的3 mol/LKOH溶液中。
②过滤。
③____________________。
④搅拌、静置、过滤,用乙醇洗涤2~3次,
⑤在真空干燥箱中干燥。
(5)称取提纯后的K2FeO4样品0.2200 g于烧杯中,加入强碱性NaCr(OH)溶液,反应后再加稀H2SO4调节溶液呈强酸性,配成250 mL溶液,取出25.00 mL放入锥形瓶,用0.01000 mol/L的(NH4)2Fe(SO4)2溶液滴定至终点,重复操作2次,平均消耗(NH4)2Fe(SO4)2溶液30.00 mL。涉及主要反应为:
Cr(OH)4-+FeO42- =Fe(OH)3↓+CrO42-+OH-
2CrO42-+2H+![]() Cr2O72-+H2O
Cr2O72-+H2O
Cr2O72-+6Fe2++14H+=6Fe3++2Cr3++7H2O
则该K2FeO4样品的纯度为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2mol金属钠和1mol氯气反应的能量关系如图所示,下列说法不正确的是

A. 相同条件下,K(s)的(ΔH2′+ΔH3′)<Na(s)的(ΔH2+ΔH3)
B. ΔH4的值数值上和Cl-Cl共价键的键能相等
C. ΔH5<0,在相同条件下,2Br(g)的ΔH5′>ΔH5
D. ΔH7<0,且该过程形成了分子间作用力
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用0.1 mol·L-1的HCl溶液逐滴滴入10.00 mL0.1 mol·L-1的NH3·H2O溶液中,其AG值变化的曲线如图所示。已知AG=![]() ,下列分析错误的是
,下列分析错误的是
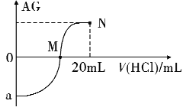
A. 滴定前HC1溶液的AG =12;图中a<0
B. M点为完全反应点,V( HCl) =10 mL,且c(Cl-) >c(NH4+)
C. 从M点到N点水的电离程度先增大后减小
D. N点溶液中:c(Cl-) =2c(NH3·H2O) +2c(NH4+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若在加入铝粉能放出氢气的溶液中,分别加入下列各组离子,一定能大量共存的是
A. NH4+、SO42-、CO32-、K+ B. Na+、Ba2+、Ca2+、HCO3-
C. Mg2+、SO42-、K+、Cl- D. K+、Cl-、Na+、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钙,化学式为CaO2,微溶于水,溶于酸,可用作分析试剂、医用防腐剂、消毒剂。现有一种制备过氧化钙的实验方案,流程如下图,其主要反应的化学方程式为:CaCl2+2NH3·H2O+H2O2=CaO2↓+2NH4Cl+2H2O表示。回答下列问题:
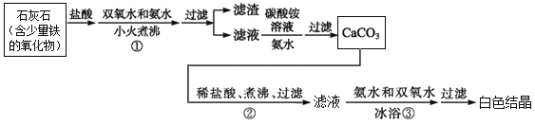
(1)步骤①中,加入氨水的目的是_____________,小火煮沸的作用是________________________。
(2)步骤②的具体操作为逐滴加入稀盐酸,至溶液中尚存有少量固体;再将溶液煮沸,趁热过滤。此过程中,将溶液煮沸的作用是________________________________________。
(3)制备过氧化钙的另一种方法是:将石灰石煅烧后,直接加入双氧水反应,过滤后可得到产品。此法工艺简单、操作方便,但是得到的产品纯度较低,往往CaCO3、Ca(OH)2等杂质含量较高。若实验室只提供稀盐酸和澄清石灰水两瓶试剂,以及试管、小烧杯、胶头滴管、药匙各1个,请设计实验检验所得产品中含有CaCO3。_____________________________(简要描述方案即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某二元化合物X是锂硫电池的电极材料,为探究其组成进行了如下实验:
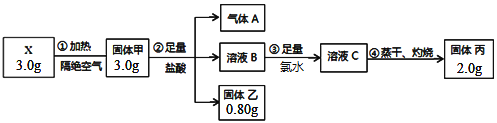
固体乙是一种单质,固体丙呈红棕色,将气体A通入溶液C中也能生成固体乙。
请回答:
(1)X的化学式是_________________,步骤①的化学方程式是_________________________。
(2)气体A通入溶液C发生反应的离子方程式是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物M是二苯乙炔类液晶材料的一种,最简单的二苯乙炔类化合物是![]() 。以互为同系物的单取代芳香烃A、G为原料合成M的一种路线(部分反应条件略去)如下:
。以互为同系物的单取代芳香烃A、G为原料合成M的一种路线(部分反应条件略去)如下:
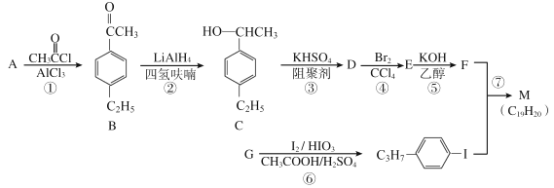
已知: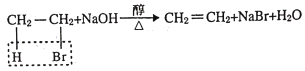
回答下列问题:
(1)A的结构简式为_______;G的分子式为_______。
(2)D中含有的官能团名称是______________。
(3)反应①的反应类型是________,反应④的反应类型是___________。
(4)反应⑤的化学方程式为____________________________。
(5)能同时满足下列条件的B的同分异构体有______种(不考虑立体异构),其中核磁共振氢谱为5组峰,且峰面积之比为6:2:2:1:1的是_________(写结构简式)。
①苯环上有两个取代基 ②能发生银镜反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com