
| A. | 位于周期表中同一周期的元素,原子具有相同的电子层数 | |
| B. | 凡是位于周期表中同一周期的元素,都是按从左到右的顺序原子核外最外层电子数由1递增至8 | |
| C. | 凡是位于周期表中同一主族的元素,原子具有相同的最外层电子数 | |
| D. | 凡是位于周期表中同一主族的元素,都是按从上到下的顺序原子核外电子层数逐渐递增 |
分析 A.电子层数=周期数;
B.短周期中第一周期只有2种元素,长周期含副族元素;
C.主族元素的最外层电子数相同;
D.同一主族的元素,从上到下原子序数增大,电子层数增多.
解答 解:A.电子层数=周期数,则位于周期表中同一周期的元素,原子具有相同的电子层数,故A正确;
B.短周期中第一周期只有2种元素,长周期含副族元素,二、三周期的元素,都是按从左到右的顺序原子核外最外层电子数由1递增至8,故B错误;
C.主族元素的最外层电子数相同,则凡是位于周期表中同一主族的元素,原子具有相同的最外层电子数,故C正确;
D.同一主族的元素,从上到下原子序数增大,电子层数增多,则凡是位于周期表中同一主族的元素,都是按从上到下的顺序原子核外电子层数逐渐递增,故D正确;
故选B.
点评 本题考查元素周期表的结构及应用,为高频考点,把握原子结构与元素周期表的关系为解答的关键,侧重分析与应用能力的考查,注意选项B中结合实例分析,题目难度不大.


 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源: 题型:选择题
| A. | 1.5 mol | B. | 1.25 mol | C. | 1.6 mol | D. | 2.5 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24L苯含有的分子数为0.1NA | |
| B. | 标准状况下,11.2L乙烷中含有共价键的数目为3NA | |
| C. | 常温下,1mol羟基中含有的电子数为9NA | |
| D. | 1mol冰醋酸和lmo1乙醇在浓硫酸加热下充分反应生成H2O个数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 一定温度下,反应 MgCl2(1)=Mg(1)+Cl2(g)的△H>0,△S>0 | |
| B. | 常温下,pH均为5的盐酸与氯化铵溶液中,水的电离程度相同 | |
| C. | 0.1mol•L-1CH3COOH溶液加水稀释,溶液的pH和CH3COOH的电离度均增大 | |
| D. | 将BaCl2溶液滴入含酚酞的Na2CO3溶液,红色逐渐褪去,说明BaCl2溶液显酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用食醋可以洗水垢{主要成分为CaCO3和Mg(OH)2)} | |
| B. | 少量的钠保存在煤油中 | |
| C. | 氢氧化钠溶液用带橡胶塞的细口试剂瓶贮存 | |
| D. | 氯水保存在白色细口试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有机物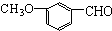 ,有多种同分异构体,其中属于酯且含有苯环结构的共有4种 ,有多种同分异构体,其中属于酯且含有苯环结构的共有4种 | |
| B. | 除去乙烯中混有的甲烷,可将混合气体通过酸性高锰酸钾溶液 | |
| C. | 甲酸分子中有醛基,因此无法区别甲醛溶液和甲酸溶液 | |
| D. | 苯乙烯分子中所有原子可能在一个平面上 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液A和溶液B均可以是盐酸或NaOH溶液 | |
| B. | 实验室中方案Ⅱ更便于实施 | |
| C. | 若溶液B选用浓硝酸,测得铜的质量分数偏大 | |
| D. | 方案一可能产生氢气,方案二可能剩余铜 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com