
【题目】下列关于自然界中氮循环(如图)的说法不正确的是( )
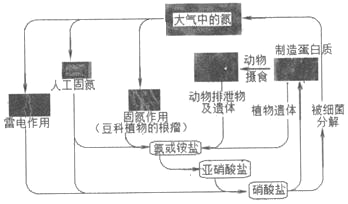
A. 人工固氮可以得到硝酸盐
B. 雷电作用可将氮气直接转化为铵盐
C. 细菌对氮元素的循环有重要作用
D. 亚硝酸盐转化为硝酸盐的过程中,氮元素被氧化
科目:高中化学 来源: 题型:
【题目】下列有关甲苯的实验事实中,能说明苯环对侧链性质产生影响的是( )
A. 甲苯燃烧产生带浓烟的火焰
B. 甲苯能使酸性KMnO4溶液褪色
C. Cl2既能取代甲苯中苯环上的氢原子,也能取代甲基上的氢原子
D. 甲苯能与H2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有CH4、C2H4、C2H6三种有机化合物:
(1)等质量的以上物质完全燃烧时耗去O2的量最多的是__________。
(2)同状况、同体积的以上三种物质完全燃烧时耗去O2的量最多的是__________。
(3)等质量的以上三种物质燃烧时,生成二氧化碳最多的是__________,生成水最多的是__________。
(4)在120℃、1.01×105Pa时,有两种气态烃和足量的氧气混合点燃,相同条件下测得反应前后气体体积没有发生变化,这两种气体是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在三支试管中分别加入2 mL 5%H2O2溶液,再在其中两支试管中分别滴加0.1 mol/L FeCl3溶液和0.1 mol/L CuSO4溶液,试管中发生反应的化学方程式__________,后两支试管中能观察到的共同的明显现象是__________。该实验说明催化剂能加快化学反应速率,还能得出的结论是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】前两年华北地区频繁出现的雾霾天气引起了人们的高度重视,化学反应原理可用于治理环境污染,请回答以下问题。
(1)一定条件下,可用CO处理燃煤烟气生成液态硫,实现硫的回收。
①已知:2CO(g) + O2(g) = 2CO2(g) ΔH = 566 kJ·mol1
S(l) + O2(g) = SO2(g) ΔH = 296 kJ·mol1
则用CO处理燃煤烟气的热化学方程式是________________________。
②在一定温度下,向2 L 密闭容器中充入 2 mol CO、1 mol SO2发生上述反应,达到化学平衡时SO2的转化率为90%,则该温度下该反应的平衡常数K = _________________。
(2)SNCR─SCR是一种新型的烟气脱硝技术(除去烟气中的NOx),其流程如下:

已知该方法中主要反应的热化学方程式:
4NH3(g) + 4NO(g) + O2(g) 4N2(g) + 6H2O(g) ΔH = 1646 kJ·mol1,在一定温度下的密闭恒压的容器中,能表示上述反应达到化学平衡状态的是__________________(填字母)。
a.4υ逆(N2) = υ正(O2)
b.混合气体的密度保持不变
c.c(N2):c(H2O):c(NH3)=4:6:4
d.单位时间内断裂4 mol N─H键的同时断裂4 mol N≡N键
(3)如图所示,反应温度会直接影响SNCR技术的脱硝效率。
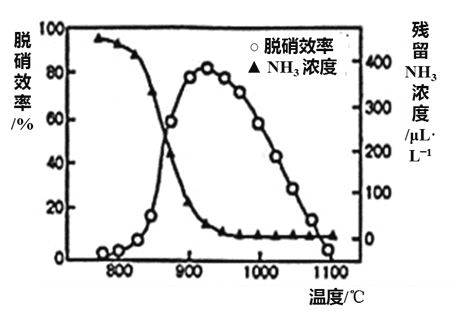
①SNCR技术脱硝的温度选择925 ℃的理由是___________________。
②SNCR与SCR技术相比,SNCR技术的反应温度较高,其原因是____________________________________;但当烟气温度高于1000℃时,SNCR脱硝效率明显降低,其原因可能是_____________________。
(4)一种三室微生物燃料电池可用于污水净化、海水淡化,其工作原理如图所示:
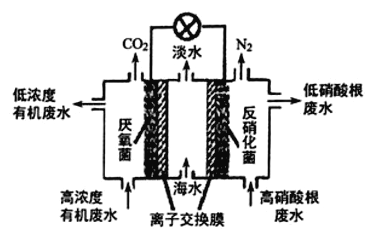
①中间室的Cl 移向_________(填“左室”或“右室”),处理后的含硝酸根废水的pH__________(填“增大”或“减小”)
②若图中有机废水中的有机物用C6H12O6表示,请写出左室发生反应的电极反应式:______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的定容容器中,当下列哪些项不再发生变化时,表明反应A(g)+2B(g)![]() C(g)+D(g)已达到平衡状态①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度④混合气体的总物质的量 ⑤混合气体的平均相对分子质量⑥v(C)与v(D)的比值 ⑦混合气体的总质量 ⑧混合气体的总体积
C(g)+D(g)已达到平衡状态①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度④混合气体的总物质的量 ⑤混合气体的平均相对分子质量⑥v(C)与v(D)的比值 ⑦混合气体的总质量 ⑧混合气体的总体积
A. ①②③④⑤⑥⑦⑧ B. ①②③④⑤⑦
C. ①③④⑤ D. ①③④⑤⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铈是地壳中含量最高的稀土元素,二氧化铈(CeO2)是其重要的化合物。平板液晶显示屏生产过程中产生大量的废玻璃粉末,其中含CeO2、SiO2、Fe2O3等物质,某实验小组以此粉末为原料回收铈,设计流程如图所示:
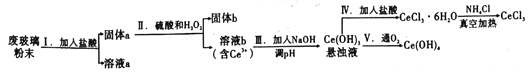
(1)步骤Ⅰ加入过量盐酸后,溶液a中的阳有离子___________________。
(2)步骤Ⅱ中反应的氧化剂和还原剂的物质的量之为___________。
(3)为了使步骤Ⅲ所得悬浊液中的Ce3+浓度为1×10-6mol·L-1,则加入NaOH调节溶液的pH应为____________[已知:Ce(OH)3的Ksp=8.0×10-21,lg2=0.3]。
(4)将NH4Cl固体与CeCl3·6H2O混合真空加热可得无水CeCl3,其中加入NH4Cl的作用是__________。
(5)第Ⅴ步反应的化学方程式是____________________;用反应得到的悬浊液制备纯净的Ce(OH)4需进行的实验操作为______________。
(6)对CeCl3样品纯度进行测定的方法:准确称取样品wg配成100mL溶液,取25.00mL置于锥形瓶中,加入稍过量的过二硫酸铵[(NH4)2S2O8]溶液将Ce3+氧化为Ce4+,然后用萃取剂[用(HT2)表示]萃取Ce4+,再用cmol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点(其离子反应方程式为Ce4++Fe2+=Ce3++Fe3+),重复2~3次,平均消耗VmL标准溶液。
①“萃取”时存在反应:Ce4++n(HT)2![]() Ce(H2n-4)+4H+,若要提高滴定的准确率,应使溶液呈______性(填“酸”“中”或“碱”)。
Ce(H2n-4)+4H+,若要提高滴定的准确率,应使溶液呈______性(填“酸”“中”或“碱”)。
②经计算,CeCl3样品的纯度为________________。 [M(CeCl3)=246.5g·mol-1]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com