
�������ֱ����뷴Ӧ����ʽ��Ӧ����ȷ���ǣ�������
| �� | A�� | ��Ũ������4﹣��﹣1﹣�������ȷ�����ȥ��Ӧ��BrCH2CH2CH2CH2OH |
| �� | B�� | �ǻ���������۵�PGA��nHOCH2COOH |
| �� | C�� | ˮ���ᣨ |
| �� | D�� | ��ϩ��HCl�ӳɲ�������������л��� |
���㣺
�л���Ľṹ�����ʣ�
ר�⣺
�л���Ӧ��
������
A���ȴ���Ӧ�ڼ�Ĵ���Һ�з�����ȥ��Ӧ��
B����Ӧ����ˮ��
C��Ӧ����CO2��HCO3﹣��
D����ϩ��HCl�����ӳɷ�Ӧ����CH3CHClCH3��CH3CH2CH2Cl��
���
�⣺A���ȴ���Ӧ�ڼ�Ĵ���Һ�з�����ȥ��Ӧ����Ӧ�ķ���ʽΪBrCH2CH2CH2CH2OH BrCH2CH2CH=CH2��+H2O����A����
BrCH2CH2CH=CH2��+H2O����A����
B������ʽӦΪnHOCH2COOH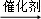 HO
HO +��n﹣1��H2O����B����
+��n﹣1��H2O����B����
C��Ӧ����CO2��HCO3﹣������ʽΪ2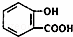 +3CO32﹣��2
+3CO32﹣��2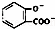 +CO2��+2HCO3﹣+H2O����C����
+CO2��+2HCO3﹣+H2O����C����
D����ϩ��HCl�����ӳɷ�Ӧ����CH3CHClCH3��CH3CH2CH2Cl����D��ȷ��
��ѡD��
������
���⿼���л���Ľṹ�����ʣ��ѶȲ���ע���л�������ŵ����ʣ��״���ΪCѡ�ע����ǻ������Ա�̼�������ص㣮
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
Ϊ����0.1mol/L��NaOH��Һ������˵������ȷ���ǣ�������
| �� | A�� | ȡ4g NaOH��������1Lˮ�� |
| �� | B�� | ȡ0.4g NaOH��������ˮ���1L��Һ |
| �� | C�� | ȡ4g NaOH��������ˮ���1L��Һ |
| �� | D�� | ȡ0.4g NaOH��������1Lˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������������ԭ����Ŀ��93g Na2O����ԭ����һ����ȵ��ǣ�������
| �� | A�� | 67.2L CO2 | B�� | 33g CO2 | C�� | 80g SO3 | D�� | 98g H2SO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ʰ���ͱ������Ϻ���һ�������·�����Ӧ���ɵĶ����У�������
| �� | A�� | 4�� | B�� | 3�� | C�� | 2�� | D�� | 1�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��������Ԫ��A��B��C��D��E��F��ԭ��������������A��B����������C��D�������ӵĵ����Ų�ʽ��Ϊls22s22p6��Aԭ�Ӻ�����2��δ�ɶԵ��ӣ�C���ʿ�����ˮ��Ӧ����������ˮ��Ӧ��E��Fԭ���ڻ�̬ʱ�����ӵĹ����9������Eԭ�Ӻ�����3��δ�ɶԵ��ӣ�F����A�γ���ͬ��̬�������ӣ���A���Ӱ뾶С��F���ӣ��ش�
��1��д����Ԫ�صķ��ţ�A������B������C������D������E������F������
��2��д��B��C�γɵĻ�����ĵ���ʽ������
��3����д����̬ԭ��F�ļ����Ų�ʽ������
��4����������Ԫ�ذ��縺�Դ�С�����������������дԪ�ط��ţ���
��5��C��D��E��FԪ�ص�һ�����ܴ�С�����������������дԪ�ط��ţ���
��6��A��B��C��D����Ԫ�صļ����Ӱ��뾶��С�����˳��Ϊ�������ӷ��ű�ʾ��������
��7��C��D��E��F����Ԫ���У��γɵ�����������Ӧˮ�����У�д��ѧʽ����������ǿ�������� ������ǿ���������������Ե�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ӷ���ʽ����ȷ���ǣ��� ��
A����Na2FeO4��Һ�м���ϡ�������������4FeO42����20H+ = 4Fe3+��3O2����10H2O
B��10mL0.5mol/L��������Һ��20mL0.5mol/LBa(OH)2��Һ��Ϸ�Ӧ��
3Ba2+ + 6OH- +2Al3+ +3SO42- = 3BaSO4����2Al(OH)3��
C��ͭ����63%�����ᷴӦ��Cu +4H++2NO3- =Cu2��+2 NO2��+ 2H2O
D����ҵ���ô���Һ����SO2��CO32-+SO2=CO2+SO32-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����������Ϣ�����й�֮����������š��������������������ٴ�����Ϯ�ž��ȵأ����ֵ������е��ض������������������Ҫ��ѧ֪ʶ����ѧ��������ϵ���ܣ�����˵����ȷ����
A���ҹ��ص���н������ѷ��������������ձ�������CO2��NO2�Ϳ�������������������Ҫ��Ⱦ��
B��PM 2.5����ֱ��ԼΪ2.5��10��6m����ɢ�ڿ������γ����ܽ�
C�����������������ȼú����������β����������������߿�������
D����ɫ��ѧ�ĺ��������û�ѧԭ���Ի�����Ⱦ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ȡ���캽�չ�ҵ���ϡ����ѺϽ����Ҫԭ�ϡ�����������Ҫ�ɷ���FeTiO3���Ʊ�TiCl4�Ȳ�Ʒ��һ�ֹ�������ʾ�����£�
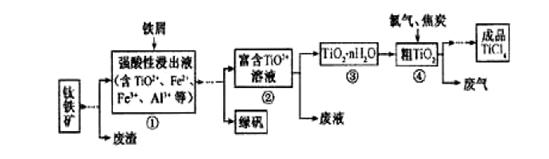
�ش��������⣺
��1�������м�����м������Һ����ɫ����ʱ��Һ�Գ�ǿ���ԡ��ù����������·�Ӧ������
2Fe3����Fe === 3Fe2��
2TiO2��(��ɫ) ��Fe��4H�� === 2Ti3��(��ɫ) ��Fe2����2H2O
Ti3��(��ɫ) ��Fe3����H2O === TiO2��(��ɫ) ��Fe2����2H��
�������������____________��
��2���ڢڡ��۹�������Ҫ�����������γ�TiO2��n H2O�ܽ����÷�ɢ�ʿ���ֱ����С��_____________��Χ��
��3�����Ѣ����ƵõĹ���TiO2��n H2O������ϴ��ȥ���е�Fe (OH)3���ʣ������Ƶ��Ѱۡ���֪25��ʱ��Ksp[Fe(OH)3]��2.79��10-39,���¶��·�ӦFe (OH)3��3H�� Fe3�� ��H2O��
Fe3�� ��H2O�� ƽ�ⳣ��K=_____________��
ƽ�ⳣ��K=_____________��
��4����֪��TiO2 (s) ��2 Cl2 (g)=== TiCl4(l) ��O2(g) ��H=+140KJ��mol-1
2C(s) ��O2(g)=== 2CO(g) ��H=��221KJ��mol-1
д������TiO2�ͽ�̿��������Ӧ����Һ̬TiCl4��CO������Ȼ�ѧ����ʽ��_____________��
��5���������վ��гɱ��͡����õ�Ʒλ����Ϊԭ�ϵ��ŵ㡣������ɫ��ѧ����ù��������д��ڵIJ���֮����_____________��ֻҪ��д��һ���
��6�������±���Ϣ��Ҫ���ƺ�����SiCl4���ʵ�TiCl4 ���ɲ���_____________������
| TiCl4 | SiCl4 | |
| �۵�/�� | ��25.0 | ��68.8 |
| �е�/�� | 136.4 | 57.6 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com