
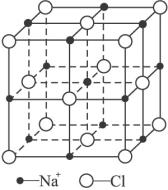
NaCl的晶体结构
解析:在氯化钠晶体中,一个Na+位于晶胞的中心,12个Na+分别位于晶胞的12条棱上,则属于该晶胞的Na+相当于3个(![]() ×12=3,棱边上的每个Na+同时被4个晶胞共用,属于该晶胞的Na+仅占1/4),因此一个晶胞中共含有4个Na+,8个Cl-分别位于晶胞的8个顶点上,则属于该晶胞的Cl-相当于1个(
×12=3,棱边上的每个Na+同时被4个晶胞共用,属于该晶胞的Na+仅占1/4),因此一个晶胞中共含有4个Na+,8个Cl-分别位于晶胞的8个顶点上,则属于该晶胞的Cl-相当于1个(![]() ×8=1,顶点上的每个Cl-同时被8个晶胞共用,属于该晶胞的Cl-仅占1/8),6个Cl-分别位于晶胞的6个面心上,则属于该晶胞的Cl-相当于3个(
×8=1,顶点上的每个Cl-同时被8个晶胞共用,属于该晶胞的Cl-仅占1/8),6个Cl-分别位于晶胞的6个面心上,则属于该晶胞的Cl-相当于3个(![]() ×6=3,面心上的每个Cl-同时被2个晶胞共用,属于该晶胞的Cl-仅占1/2),所以一个晶胞中共含有4个Cl-。可见NaCl晶体中Na+、Cl-的个数比为1∶1。图中位于晶胞中心的Na+实际上共有3个平面通过它,通过中心Na+的每个平面都有4个Na+位于平面的四角,这4个Na+与中心Na+距离最近且距离相等。
×6=3,面心上的每个Cl-同时被2个晶胞共用,属于该晶胞的Cl-仅占1/2),所以一个晶胞中共含有4个Cl-。可见NaCl晶体中Na+、Cl-的个数比为1∶1。图中位于晶胞中心的Na+实际上共有3个平面通过它,通过中心Na+的每个平面都有4个Na+位于平面的四角,这4个Na+与中心Na+距离最近且距离相等。
所以在NaCl晶体中,每个Na+周围与它距离最近且距离相等的Na+共有12个,按相似的方法可推出每个Cl-周围与它最近且距离相等的Cl-也共有12个。
答案:6 6 4 4 12


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
 (2013?辽宁一模)[化学--选修3物质结构与性质]
(2013?辽宁一模)[化学--选修3物质结构与性质]| 417×1030 |
| a3NA |
| 417×1030 |
| a3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
X-射线衍射法是通过X-射线衍射仪测出离子化合物中离子间的间隔,进而测出阿伏加德罗常数的值。已知: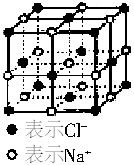 X-射线衍射仪测出的NaCl晶体中相邻Na+和Cl-的间距为2.819×10-8cm。相对原子质量为:Na:22.99,Cl:35.45。NaCl晶体模型如右图所示。
X-射线衍射仪测出的NaCl晶体中相邻Na+和Cl-的间距为2.819×10-8cm。相对原子质量为:Na:22.99,Cl:35.45。NaCl晶体模型如右图所示。
为了测定阿伏加德罗常数,某同学做了下列实验:用分析天平称取研细的一定质量的NaCl固体,装入25mL容量瓶中,然后用滴定管向容量瓶中滴加苯,并不断振荡,使苯和NaCl晶体充分混合,加至刻度。其实验数据记录于下表:
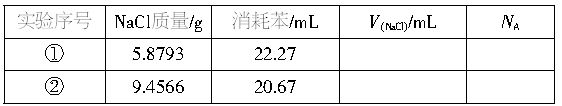
请根据实验数据填写出两次实验中未完成的空格(阿伏加德罗常数NA项只要求写出计算表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
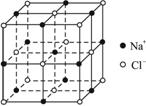
图3-23
查看答案和解析>>
科目:高中化学 来源:2013年辽宁省东北三校联考高考化学一模试卷(解析版) 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com