
| A. | Na+ | B. | NO3- | C. | Mg2+ | D. | OH- |
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:选择题
 铅蓄电池是典型的可充电电池,它的正负极隔板是惰性材料,电池总反应式为:Pb+PbO2+4H++2SO42-$?_{充电}^{放电}$2PbSO4+2H2O(如图),则下列说法正确的是( )
铅蓄电池是典型的可充电电池,它的正负极隔板是惰性材料,电池总反应式为:Pb+PbO2+4H++2SO42-$?_{充电}^{放电}$2PbSO4+2H2O(如图),则下列说法正确的是( )| A. | 放电时负极反应是:Pb-2e-═Pb2+,充电是阴极反应是:PbSO4+2H2O-2e-═PbO2+4H++SO42- | |
| B. | 闭合K断开K1,电流的流动方向是从B到A | |
| C. | 放电过程中,溶液的pH不断减小 | |
| D. | 放电时,线路上若有1mole-通过,则消耗硫酸也是1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  根据图可判断反应的△H<0 | |
| B. |  根据图,除去CuSO4溶液中的Fe3+,可加入CuO调节pH至3~5 | |
| C. |  图可表示压强(p)对反应2A(g)+2B(g)?3C(g)+D(s)的影响,且p1>p2 | |
| D. |  图 可表示向醋酸溶液中通入氨气时,溶液导电性随氨气量的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 11.2L甲烷含有的氢原子数为2NA | |
| B. | 1mol氧气在化学反应中得到的电子数一定为4NA | |
| C. | 28g丙烯中含有的碳氢键的数目为4NA | |
| D. | 1mol/L的硝酸中含有的硝酸根离子的数目为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2、D2和T2互称为同素异形体 | B. | 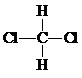 和 和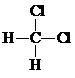 互称为同分异构体 互称为同分异构体 | ||
| C. | 35Cl和37Cl 互称为同位素 | D. | C2H4与C4H8一定能互称为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性高锰酸钾与少量双氧水反应:2MnO4-+3H2O2+6H+═2Mn2++3O2↑+6H2O | |
| B. | 向次氯酸钙溶液通入SO2:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | |
| C. | 氢氧化钙溶液与碳酸氢镁溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| D. | 向NaClO溶液中通入过量CO2;CO2+ClO-+H2O═HCO3-+HClO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com